沪教第六章溶解现象单元质量检测
(45分钟,100分)
相对原子质量:H:1 C:12 O:16 Cl:35.5 S: 32 Na-23 Ca:40 Cu:64 Fe:56
一、选择题 (每小题4分,共40分。每小题只有一个答案符合题意,把符合题意的选项填在下面的表格中)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 |
1、下列有关溶液的说法错误的是
A、碘酒中的溶剂是酒精
B、改变条件,饱和溶液与不饱和溶液可以相互转化
C、氢氧化钙的饱和溶液一定是浓溶液
D、析出晶体后的溶液是该温度下的饱和溶液
2、20℃时NaCl的溶解度为36g,20℃时把40gNaCl放入100g水中,充分溶解后所得溶液的溶质质量分数为
A、28.6% B、26.5%
C、40% D、无法计算
3、用氯化钠固体配制一定质量分数的氯化钠溶液,必须使用的一组仪器是
A、天平 烧杯 量筒 玻璃棒 药匙
B、天平 烧杯 量筒 铁架台 药匙
C、天平 烧杯 漏斗 蒸发皿 玻璃棒
D、天平 集气瓶 漏斗 蒸发皿 玻璃棒
4、某溶液甲,经过若干操作,析出10g晶体后变成乙溶液(甲、乙两溶液为同种溶质),下列关于两种溶液的溶质质量分数的说法中,正确的是
A、乙一定小于甲 B、乙一定等于甲
C、乙一定大于甲 D、乙溶液一定是饱和溶液
5、将m克硝酸钾饱和溶液从500C冷却到100C,溶液中保持不变的是:
A、溶液质量 B、溶液浓度
C、溶质质量 D、溶剂质量
6、把10mL溶质质量分数为35%的浓盐酸稀释100倍,则稀释后的溶液中所含溶质的质量
A、减少99% B、增大100倍
C、增大1倍 D、不变
7、要使接近饱和的KNO3溶液变成饱和溶液, 下列措施错误的是
A、降低温度 B、蒸发水,再恢复到室温
C、加KNO3固体 D、加水
 8、一瓶接近饱和的硝酸钾溶液,逐渐加入硝酸钾固体,下面的图像中符合溶液中溶质质量变化的是
8、一瓶接近饱和的硝酸钾溶液,逐渐加入硝酸钾固体,下面的图像中符合溶液中溶质质量变化的是
9、下列说法正确的是
A、可利用降低海水温度的方法获得大量氯化钠晶体
B、溶解度是指100g水中最多能溶解某种溶质的质量
C、干冰可用于人工降雨
D、同种物质的饱和溶液一定比不饱和溶液浓
10、有100g5%的氯化钠溶液,若将其溶质的质量分数增大一倍,可采用的做法是
A、把溶剂蒸发掉一半 B、加入5g氯化钠固体
C、把溶剂蒸发掉50g D、加入100g5%氯化钠溶液
二、填空与简答(11-14每空3分,其余每空2分,共33分)
11、我们已经知道这样的事实:①食盐易溶于水,难溶于植物油;②硝酸钾易溶于水,碳酸钙难溶于水;③蔗糖在热水中溶解的质量比在等质量的冷水中溶解的多。请你回答下列问题:
(1)以上事实表明,固体物质的溶解能力与_______________、________________、_________________________三个因素有关。
(2)请你举出上述三个因素中的一个应用实例(要求与上面所列事实不同)____
______________________________________________。
12、氢氧化钙溶液中通入适量二氧化碳,反应完全后,溶液的质量 (增加或减少),从混合物中分离出碳酸钙用 法。
13、医院化验室为了检验糖尿病患者尿液中葡萄糖的存在,常需要10%的NaOH溶液和5%的CuSO4溶液。现需要配制500g5%的CuSO4溶液。计算:(1)所需CuSO4的质量是______________;(2)所需蒸馏水的质量是________________。
14、盛夏,当天气又闷又热时,大气压较低,鱼池中常常出现“鱼儿浮头”现象(鱼缺氧,浮上水面呼吸),其原因是___________________________________。
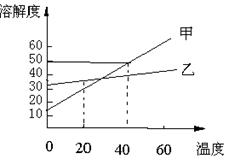 15、甲和乙两种物质的溶解度曲线如图所示:
15、甲和乙两种物质的溶解度曲线如图所示:
(1)20℃时,甲的溶解度比乙的溶解度_________
(填“大”或“小”)
(2)40℃时,在100g水中加入80g甲固体,充分搅拌
所得溶液的质量是______________
(3)50℃时,某溶液所溶解的甲和乙物质都已饱和。把
该溶液冷却到室温,有晶体析出,经检验发现析出的晶体主要是甲,其原因是______(填编号)
①50℃时,甲的溶解度更大
②50℃时,乙的溶解度更大
③甲的溶解度受温度变化的影响比乙大
三、实验探究题(16分)
16、下图是某同学配制一定质量的0.9%生理盐水的全过程:
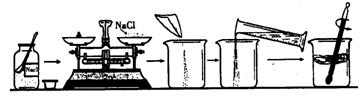
⑴请找出上图中的错误:
①____________ __ _____;②_________ ___________;
③______ ______ ________。
⑵如果配制的生理盐水中NaCl的质量分数小于0.9%,则可能造成误差的原因有(至少举出三点):
①__________ __________;②________ __ __________;
③_____ _____ __________。
四、计算题(11分)
17、某化学兴趣小组为测定空气中二氧化硫的含量,用NaOH溶液吸收SO2。现用NaOH溶液充分吸收1000L已除去CO2的空气样品中的SO2,溶液质量增重了0.64g,已知此时空气的密度约为1.3g/L,求:
(1) 被吸收的SO2的质量;
(2) 参加反应的NaOH的质量;
(3) 空气中SO2的质量分数(计算结果精确至0.01%)。
参考答案
一、选择题(每小题4分,共40分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | C | B | A | D | D | D | D | D | C | C |
二、填空与简答(11-14每空3分,其余每空2分,共33分)
11、(1)溶质的性质、溶剂的性质、温度(2)衣服上的油污用水洗不掉,用汽油很容易洗去。
12、减少、过滤
13、25g,474g
14、天气闷热时(气温高,气压低),水中氧气含量低
15、小;150g;③
三、实验探究题( ⑴小题6分,⑵小题10分,共16分)
16、⑴①广口瓶塞放反了(或瓶塞放反了)②砝码和药物放反了③温度计用来搅拌
⑵计算错误:①水算多了;②氯化钠算少了。称量氯化钠时操作错误如:③天平读数有误;④氯化钠和砝码放反了;⑤左盘放了纸片右盘未放纸片;⑥天平未调零等。用量筒量取水时
错误如:⑦水量多了(或取水读数时仰视)。⑧氯化钠中混有杂质。⑨烧杯中有水。其它答案只要合理皆可。
四、计算题(11分)
17、(1)0.64g (2)0.8g (3)0.05%