江苏省南通市如东县初三化学模拟考试
(总分100分 答卷时间100分钟)
可能用到的相对原子质量:H-1;O-16;C-12;Ca-40;S-32;Fe-56;Zn-65;Cu-64
一、选择题(每小题只有一个选项符合题意,将这一选项的序号填入相应的括号内。每题2分,本题共30分)
1.下列各组变化中属于化学变化的一组是 ( )
A.碘的升华 B.铜绿分解 C.胆矾研碎 D.水受热变成水蒸气
2.下列物质中,属于纯净物的是 ( )
A.医用消毒酒精 B.生理盐水 C.清新的空气 D.蔗糖
3.为了预防缺铁性贫血,人体必须保证足够的铁摄入,这里的铁是指 ( )
A.铁单质 B.铁元素 C.氢氧化铁 D.氧化铁
4.一些食物的PH如下,其中碱性最强的是 ( )
A.苹果2.9-3.3 B.牛奶6.3-6.6 C.鸡蛋清7.6-8.0 D.番茄4.0-4.4
5.下列基本反应类型中,一定有单质生成的是 ( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
6.下列做法容易发生危险的是 ( )
A.用石灰沙浆抹墙 B.用干冰制造舞台上的云雾现象
C.到溶洞探险用火把照明 D.掏沼气池前先进行灯火试验
7.麦收时节,某些地方仍有就地焚烧麦秸秆陈规陋习。焚烧麦秸秆可能导致的后果有:①引发火灾②能见度降低,引发交通事故③诱发呼吸道疾病④造成部分肥力损失等。其中主要因焚烧麦秸秆污染了空气而造成的后果是 ( )
A.①④ B.②③ C.①③ D.②④
8.配制90g10%的氯化钠钠溶液后,再向其中加入10g氯化钾并搅拌至完全溶解,则所得溶液中氯化钠的质量分数是 ( )
A.19% B.10% C.9% D.无法计算
9.下列物质露置于空气中一段时间后,其质量增加且变质的是 ( )
A. 浓硫酸 B.氢氧化钠 C. 浓盐酸 D.大理石
10.下列转化不能一步实现的是 ( )
A.CaO→CaCl2 B.Cu→CuO C. CaCO3→Ca(OH)2 D.BaCl2→Ba(NO3)2
11.现榨的苹果汁在空气中会由淡绿色变为棕黄色。你猜测其中可能的原因是
A.苹果汁中的Fe2+变成Fe3+ B.苹果汁中含有Cu2+‑ ( )
C.苹果汁中含有OH- D.苹果汁中含有Na+
12.在下列溶液中放入锌片,一段时间后将锌片取出溶液质量增加的是( )
A.氯化镁溶液 B.氯化钠溶液 C.硫酸铜溶液 D.硝酸银溶液
13.诺贝尔化学奖获得者艾哈迈德・泽为维尔开创了“飞秒(10-15)化学”的新领域,使运用激光光谱技术观测化学反应时分子中原子的运动成为可能。你认为该技术不可能观测到的是 ( )
A.化学变化中反应物分子的分解 B.反应中原子的运动
C.化学变化中生成物分子的形成 D.原子核的内部结构
14.若不用指示剂,要把含有盐酸的氯化钡溶液由酸性变为中性的氯化钡溶液,最好选用下列试剂中的 ( )
A.氢氧化钡溶液 B.氧化钡粉末 C.碳酸钡粉末 D.碳酸钙粉末
15.关于实验室制取氢气并用氢气还原氧化铜的实验,下列叙述正确的是
A.可选用锌和稀硝酸来制取氢气 ( )
B.盛氧化铜的试管应向上倾斜
C.在氢气通入盛有氧化铜的试管前,要先检验其纯度。
D.在氢气还原氧化铜的实验结束时,应先撤去通氢气的导管
二、选择题(每小题只有一至两个选项符合题意,将符合题意选项的序号填入相应题首的括号内。每题2分,本题共10分)
16.下列说法错误的是 ( )
A.原子一定比分子小 B.同种溶质的饱和溶液不一定比不饱和溶液浓
C.质子数相同的粒子一定属于同种元素 D.析出晶体后的溶液是该温下的饱和溶液
17.某同学想证明硫酸铜溶液的颜色是由铜离子造成的,而不是硫酸根离子引起的,他设计的下列实验中没有意义的是 ( )
A.在酒精灯的火焰上加热铜丝,铜丝由红色变为黑色,且质量增加
B.观察硫酸钾溶液无色,表明溶液中硫酸根离子无色
C.在硫酸钾溶液中加入适量的锌振荡,静置后未见明显变化,表明锌与硫酸根离子不反应
D.在硫酸铜溶液中加入适量的锌振荡,静置后颜色褪去,表明溶液的颜色是由铜离子造成的
18.下列实验方案中能达到预期目的的是 ( )
A.用氢氧化钠溶液除去二氧化碳中混有的氯化氢气体
B.用点燃的方法除去一氧化碳中混有的少量二氧化碳
C.用稀盐酸除去热水瓶胆中的水垢(主要成分是碳酸钙和氢氧化镁)
D.用氯化钡溶液除去硝酸钾溶液中混有的少量硫酸钠,得到较纯净的硝酸钾溶液
19.往CaCl2、CuCl2、MgCl2、HCl的混合溶液中加入锌粉,充分反应后过滤,滤液中含有的离子组可能是 ( )
A.H+、Ca2+、Zn2+、Cl- B.Ca2+、Mg2+、Zn2+、Cl-
C.Ca2+、Cu2+、Zn2+、Mg2+、H+、Cl- D.Ca2+、Mg2+、Cl-
20.某气体可能由初中化学中常见的一种或多种气体组成,经测定其中只含有碳和氧两种元素,碳氧元素的质量比为1:2,则关于该气体的说法正确的是 ( )
A. 一定是纯净物 B.一定是一氧化碳、二氧化碳的混合物
C.该气体中所含物质最多两种 D.该气体的组成情况最多三种
三、填空题(每空1分,本题共28分)
21.最近上海建成了我国第一条磁悬浮列车。磁悬浮的核心技术是利用超导体的反磁性。高温超导物质(Y2Ba4Cu6O13)是以YmOn、BaCO3和CuO为原料,经研磨烧结合而成(此过程中所有元素的化合价不变)。
(1)高温超导材料(Y2Ba4Cu6O13)由 种元素组成,其中Y呈 价,YmOn的化学式是 。
(2)在合成该高温超导材料的同时,还生成了一种物质,该物质是 。
22.人们在利用物质某些性质时,可能有利也可能带来危害。请你仿照示例,选择两种气体填写下表。
| 物质 | 有利的一面(用途) | 不利的一面(危害) |
| 示例:氢气 | 可以作火箭推进剂 | 使用不当容易引起爆炸 |
23.某兴趣小组同学改进了还原氧化铜的实验:在用少量水润湿的木炭上均匀洒少许氧化铜粉末,接着在酒精灯火焰上灼烧,木炭表面会附着红色的固体。试写出该过程中可能发生的有关反应的化学方程式(至少写出三个)。
(1) ;
(2) ;
(3) 。
24.向一定量的硝酸银溶液中加入一定量的氯化钠溶液,充分反应后过滤。你认为滤液中溶质的组成最多有 种情况,根据你的猜想,选择其中一种可能的情况,设计下列实验方案进行探索,将有关内容填写在下列表中(简述或图示):
| 滤液中的溶质(一种猜想) | 验证的实验方法 | 可能观察到的实验现象 | 结论及化学方程式 |
25.有一包粉末,可能是由NaCl、Na2SO4、Na2CO3、FeCl3、MgCl2的一种或几种组成。现做如下实验:①取少量粉末,加水溶解,得无色透明溶液;②取①中所得溶液少许加氢氧化钠溶液,无明显现象;③另取少量粉末滴加稀盐酸,也无明显现象。请问:
(1)由实验①可知,原粉末中没有 ;实验②可证明原粉末中没有 ;实验③证明原粉末中没有 。
(2)根据上述实验,可得原粉末中可能含有的物质是 。
(3)为进一步确定原粉末的成分,按下图所示进行实验:(在AgNO3、Ba(NO3)2、BaCl2中选择两种作为A、B试剂,且A、B阳离子不同)。
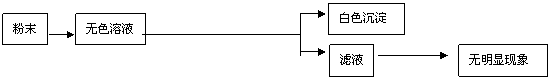 |
H2O 无色 加入过量A和稀硝酸
过滤 加入试剂B
用化学式填写:粉末 ;试剂A ;试剂B 。
四、简答题(26、27题各3分,本题共6分)
26.下面是家庭中一些日用品的近似PH:醋-3;牙膏-9;食盐水-7;肥皂水-10。蚂蚁的分泌物的PH比醋小,人被蚂蚁螫伤后会有灼痛感,在伤口上涂上适当的日用品能减轻这种灼痛。你认为可选用那种用品?其依据是什么?
27.通过学习,我们知道了下列反应:①C+O2==CO2,②2CO+O2==2CO2,③CH4+2O2==CO2+2H2O,④C2H5OH+3O2==2CO2+3H2O。通过上述四个反应的化学方程式分析,你能总结出哪些规律性的的结论?(写出三点)
五、实验题(30题第3问2分,其余每空1分,本题共14分)
28.化学实验基本操作在化学学习和研究中具有重要作用。我们在进行化学实验时,若遇到下列情况,应如何操作。
(1)洗涤试管内壁附有的油脂 。
(2)蒸发溶剂的过程中有液滴向外飞溅 。
(3)连接橡皮塞和玻璃管,玻璃管不容易插入橡皮塞内 。
29.下列两个实验操作中要注意操作的先后顺序,请在横线上填入“先”或“后”字。
(1)实验室制备气体时, 检验气密性, 放(注)入药品。
(2)实验室制氧气结束前, 停止加热, 将导管从水槽中取出。
30.用如图所示装置的序号回答下列问题(装置可以重复使用,尾气处理装置未画
![]()
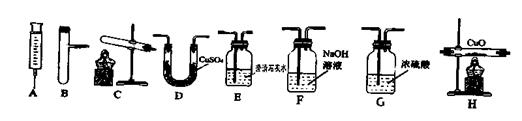
(1)实验室用氯酸钾与二氧化锰混合加热制取氧气的反应装置是 。过氧化氢与二氧化锰混合时发生的如下反应:2H2O2==2H2O+O2↑。利用此反应制取氧气的反应装置应选 和
。
(2)检验CO中混有的CO2的装置是 装置。除去CO中较多的CO2,最好选用 装置。
(3)水煤气含有CO、H2、CO2、H2O。证明水煤气中含有CO、H2的实验装置连接顺序是 。
六、计算题(31题4分,32题8分,本题共12分)
31.“骨质疏松症”是由人体缺钙引起的,可服用补钙剂来治疗。乳酸钙(CaC6H10O6・5H2O)是一种常见的补钙剂,市售乳酸钙片剂每片含乳酸钙200mg,一个成年缺钙病人每天服用20片乳酸钙剂可达到补钙目的。计算(计算结果保留整数):
(1)乳酸钙中各元素的质量比。
(2)该成年人缺钙病人改用喝牛奶(每100ml牛奶中含钙≥0.104g)来补钙,每天至少需要喝多少升牛奶。
32. 某课外兴趣小组对一批铁样品(含杂质,杂质不溶于水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,其中一位同学所取用的稀硫酸与铁样品恰好完全反应。实验数据如下:
| 甲 | 乙 | 丙 | |
| 烧杯+稀硫酸 | 200g | 150g | 150g |
| 加入铁样品 | 9g | 9g | 14g |
| 充分反应后烧杯+剩余物 | 208.7g | 158.7g | 163.7g |
请你认真分析数据,回答下列问题:(烧杯的质量为25.4g,计算结果精确到1%)
(1)哪位同学所取用的稀硫酸与铁样品恰好完全反应;
(2)计算样品中铁的质量分数;
(3)计算恰好完全反应后所得溶液中溶质的质量分数。
参考答案
一、选择题(每题2分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| 得分 | B | D | B | C | C | D | B | C | B | C | A | C | D | C | C |
二、选择题(每题2分)
| 题号 | 16 | 17 | 18 | 19 | 20 |
| 得分 | A、C | A | C | B、C | D |
三、填空题(其余每空1分,共28分)
21.四;+3;Y2O3;二氧化碳
22.一氧化碳;可以用作燃料(冶炼金属);使用不当容易引起中毒。
二氧化碳;可以用来灭火;含量过多会造成温室效应。
![]()
![]()
![]() 23.(1)2CuO+C==2Cu+CO2↑;(2)C+H2O==H2+CO;(3)CuO+H2=Cu+H2O(写CO与CuO的反应也对)。
23.(1)2CuO+C==2Cu+CO2↑;(2)C+H2O==H2+CO;(3)CuO+H2=Cu+H2O(写CO与CuO的反应也对)。
24.三种情况。(1)滤液中有硝酸银、硝酸钠;取样,滴加氯化钠溶液,看到滤液中出现白色沉淀。(2)滤液中只有硝酸钠;取两份样品,向其中一份滴加氯化钠溶液,向另一份滴加硝酸银溶液,均看不到明显现象。(3)滤液中有氯化钠、硝酸钠;取样,滴加硝酸银溶液,看到滤液中有白色沉淀。(化学方程式略)
25.(1)FeCl3;MgCl2;Na2CO3。(2)NaCl、Na2SO4。(3)Na2SO4;Ba(NO3)2;AgNO3。
四、简答题(每题3分,共6分)
26.(1)可选用牙膏或肥皂水(1分)。(2)因为牙膏或肥皂水都呈碱性,能中和蚂蚁分泌物中的酸性物质(2分)。
27.(1)可燃物的燃烧一般都需要满足点燃的条件;(2)C、CO、CH4、C2H5OH都具有可燃性;(3)可燃物中如果含有碳元素,其完全燃烧的过程中一定产生CO2;(4)上述四个反应都属于氧化反应等。
五、实验题(除30题第3问2分外,其余每空1分,共14分)
28.(1)先用热的纯碱溶液洗,再用水洗;(2)用玻棒不断搅拌液体;(3)用水将玻璃管湿润一下。
29.(1)先;后(2)后;先。
30.(1)C、A、B。(2)E、F。(3)FEGDHDE
六、计算题(32题4分,33题7分,共11分)
31.(1)钙:碳:氢:氧=10:18:5:44;(2)500mL
32.(1)乙(1分);(2)93%;(3)17%