创新题(物质构成的奥秘)
一、单项选择题
1、质子数(核电荷数)相等的微粒是( )
A、同种分子 B、同种原子 C、同种离子 D、以上都不对
2、保持物质化学性质的微粒,肯定不包括( )
A、原子 B、分子 C、电子 D、离子
3、下列说法正确的是( )
A、酸的组成中可能含氢元素 B、碱的组成中一定含金属元素
C、盐的组成中可能含氢元素 D、同种元素组成的物质一定是单质
4、元素化合价变化最大的是( )
A、![]() B、
B、![]()
C、![]() D、
D、![]()
5、用分子的间隔、不断运动、体积很小很小等特征,不能解释的是( )
A、刮风下雨现象 B、许多物质混合时总体积减小
C、物质相对分子质量显著改变 D、衣柜里的樟脑卫生球在不断变小
6、化学式常用元素符号左下角数字表示原子的质子数,左上角数字表示原子的质子数与中子数之和,则![]() 和
和![]() ( )
( )
A、属于同种元素 B、原子中所含质子数不同
C、原子中所含中子数相同 D、原子的核外电子数不同
7、下图是表示气体分子的示意图,图中“○”和“●”分别表示两种不同的原子,其中表示化合物的是( )
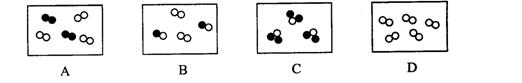
8、下列实验的最终现象,不能证明分子总是在不断运动着的是( )
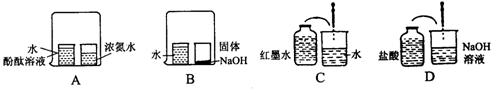
9、已知两种不同原子,一种原子核内有8个质子、8个中子,另一种原子核内有8个质子、9个中子,则它们不相等的是( )
A、核外电子数 B、原子的核电荷数
C、原子的质量 D、原子的带电量
10、下列物质中,属于纯净物的是( )
A、人体呼出的气体 B、经过净化处理的自来水
C、含有冰块的水 D、澄清的石灰水
11、下列变化中,能说明分子是可以再分的是( )
A、硫酸铜晶体研磨成粉 B、分离空气制取氧气
 C、蒸发食盐水得到食盐
D、加热氧化汞得到汞和氧气
C、蒸发食盐水得到食盐
D、加热氧化汞得到汞和氧气
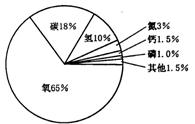
12、右图表示生物细胞里所含各种元素的质量分数,生物细胞中含量最多的元素是( )
A、Ca B、C
C、O D、N
13、人体内含量度到万分之一、质量总和低于千分之一的20多种元素称为微量元素。这些元素虽然含量很低,但对人体的正常代谢和健康却有着重要作用。下列元素肯定不是人体微量元素的是( )
A、铁 B、锌 C、氧 D、氯
14、用分子的观点分析下列变化,其中属于化学变化的是( )
A、分子运动速度加快 B、分子间的间隔变小
C、分子改变,变成其他物质的分子
D、一种物质的分子运动到另一种物质的分子之间去
15、科学研究发现七氧化二氯(![]() )是一种酸性氧化物,它跟NaOH溶液恰好完全反应生成盐和水,溶液中存在的阴离子为( )
)是一种酸性氧化物,它跟NaOH溶液恰好完全反应生成盐和水,溶液中存在的阴离子为( )
A、![]() B、
B、![]() C、
C、![]() D、
D、![]()
二、不定项选择题(每题1~2个正确答案)
16、某研究所发布一则消息:他们研究出一种激光材料,其化学式为![]() (Y:钇)。下列有关评价错误的是( )
(Y:钇)。下列有关评价错误的是( )
A、![]() 是一种盐
B、在此化合物中Y元素化合价为+3价
是一种盐
B、在此化合物中Y元素化合价为+3价
C、![]() 可能与盐酸反应生成
可能与盐酸反应生成![]()
D、不可能有该物质,因为金属元素不可能形成酸根
17、下列有关数量关系的判断中,错误的是( )
A、a克镁和b克氧气恰好完全反应,生成c克氧化镁,则a+b=c
B、m克锌放入n克稀硫酸中,充分反应后,溶液为w克,则n<w
C、h克铁放入s克硫酸铜中,充分反应后,溶液为e克,则s>e
D、m克氯化钡溶液加入p克硫酸钠溶液中,生成q克溶液,则m+p=q
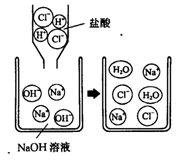 18、右图是盐酸滴入氢氧化钠溶液中,有关粒子之间反应的示意图。下列说地错误的是( )
18、右图是盐酸滴入氢氧化钠溶液中,有关粒子之间反应的示意图。下列说地错误的是( )
A、盐酸溶液中含有氢离子和氯离子
B、氢氧化钠溶液中含有钠离子和氢氧根离子
C、两种溶液混合时,氢离子与氢氧根离子结合生成了水分子
D、两种溶液混合时,钠离子与氯离子结合生成了氯化钠分子
19、下列物质中,属于氧化物的是( )
A、钢瓶中的氧气 B、高锰酸钾受热分解后和剩余固体
C、液态空气
D、氯酸钾和二氧化锰受热完全分解后溶于水,过滤,分离出的黑色固体
二、填空题
20、写出除去下列物质中的少量杂质所用试剂的名称或化学式:
铜粉中混有氧化铜__________;氢气中混有氯化氢_________;
硫酸亚铁溶液中混有硫酸铜__________。
21、反物质是由反粒子组成的物质,所有的粒子都有相应的反粒子,反粒子的特点是质量、寿命等与相应的粒子相同,但电荷、磁矩等与之相反,反粒子一旦与相应的粒子相撞,如电子碰到正电子,就会立即“湮灭”为其他物质。据最新报导,欧洲核子研究中心近日已成功地制造出约5万个低能量状态的反氢离子,这是人类首次在受控条件下大量制得的反物质,试回答下列问题:
⑴你认为反氢离子的结构示意图可表示为________,图中代表各微粒的符号表示的意义分别是________表示_________;_________表示_______________。
⑵质子与反质子相碰撞而“湮灭”是化学变化吗?______,理由是___________________
_______________。
三、简答题(共16分)
22、(4分)材料一:近年来兴起了补锌热,“真‘锌’关爱孩子的健康”。孩子的食欲不好就应该考虑可能是锌引起的。
材料二:微量的锌作为生长元素的功能有:促进身体发育、增进智力、增强肌体免疫功能、促进细胞的生长、分裂与再生等等。鉴于锌与生命结下的“不解之缘”和对智力发展所具有的极其关键的作用,人们称誉锌为“生命之花”、“智力之源”。
既然锌如此重要,给每个少年儿童配个锌碗用于饮食,配个锌杯用于喝水,是否可行?为什么?
23、(4分)原子是由原子核和核外电子构成的,原子核在原子中所占体积极小,其半径约为原子半径的十万分之一,因此,相对而言,原子里有很大的空间。![]() 粒子是带两个单位正电荷的氦原子。1911年,科学家用一束平行高速运动的
粒子是带两个单位正电荷的氦原子。1911年,科学家用一束平行高速运动的![]() 料子轰击金箔时(金原子的核电荷数为79,相对原子质量为197),发现三种实验现象:
料子轰击金箔时(金原子的核电荷数为79,相对原子质量为197),发现三种实验现象:
⑴有一小部分![]() 粒子改变了原来的运动路径,原因是
粒子改变了原来的运动路径,原因是![]() 粒子经过金原子核附近时,受到斥力而稍微改变了运动方向。
粒子经过金原子核附近时,受到斥力而稍微改变了运动方向。
⑵大多数![]() 粒子不改变原来的运动方向,原因是_______________________________。
粒子不改变原来的运动方向,原因是_______________________________。
⑶极少数![]() 粒子被弹了回来,原因是_________________________________________。
粒子被弹了回来,原因是_________________________________________。
24、(8分)下表中填入的是核电荷数从1―18的部分元素的原子结构示意图。
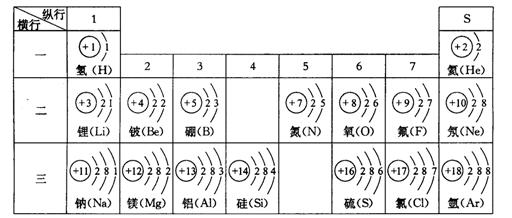
⑴在下列提供的四种元素中,选择适当元素填入上表的空格内(填序号)

⑵阅读下列短文,回答问题。
实验证明,在上表同一横行中,从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强,在同一纵行中,从上到下,原子失去电子的能力逐渐增强,得到电子能力逐渐减弱。实验还证明,失去电子能力越强的元素,其最高价氧化物的水化物(氢氧化物)碱性就越强;得到电子能力越强的元素,其最高价氧化物的水化物(含氧酸)的酸性越强,它跟氢气化合形成的氢化物也更稳定。
①在上表元素中,失去电子能力最强的原子是_________,得到电子能力最强的原子是___________。
②下列判断正确的是( )
A、碱性:![]() B、酸性:
B、酸性:![]() (高氯酸)
(高氯酸)
C、氢化物的稳定性:![]() D、得电子能力:
D、得电子能力:![]()
⑶某元素原子结构示意图为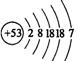 ,则该元素的化学性质跟随上表中第________纵行的元素的化学性质相似。
,则该元素的化学性质跟随上表中第________纵行的元素的化学性质相似。
四、计算题
25、2003年我国部分地区突发的“非典型肺炎”威胁着人们的身体健康。过氧乙酸可以起到消毒作用,其分子结构如右下图所示(注:●――表示碳原子;![]() ――表示氧原子;○――表示氢原子)。
――表示氧原子;○――表示氢原子)。
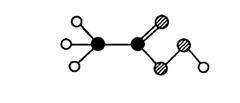 ⑴过氧乙酸分子的化学式为_____________;
⑴过氧乙酸分子的化学式为_____________;
⑵其相对分子质量为__________;
⑶C、H、O三种元素的质量比为__________;
⑷其氧元素质量分数为____________。
26、尿素是一处肥效高、土壤适应性好的常用氮肥,其化学式为![]() 。现有一尿素样品,测得氮元素的质量分数为43.5%,试通过计算说明这份尿素样品是纯净物还是混合物。
。现有一尿素样品,测得氮元素的质量分数为43.5%,试通过计算说明这份尿素样品是纯净物还是混合物。
参考答案
一、1、D 2、C 3、C 4、B 5、C 6、A 7、C 8、D 9、C 10、C 11、D 12、C 13、C 14、C 15、A
二、16、D 17、D 18、D 19、D
![]()
![]() 三、20、
三、20、![]() 干燥
干燥![]() 过量Fe粉 21、⑴
-1 2 -1 表示原子核中有1个反质子;2表示最外层正电子数为2 ⑵不是化学变化,因为发生是原子核变化
过量Fe粉 21、⑴
-1 2 -1 表示原子核中有1个反质子;2表示最外层正电子数为2 ⑵不是化学变化,因为发生是原子核变化
四、22、答:不可行。 ①锌不溶于水; ②锌多了容易中毒; ③必须在医生控制下服用。 23、⑵原子核很小 ![]() 粒子没有碰到原子核就能顺利通过 ⑶原子核虽很小,但存在,少数
粒子没有碰到原子核就能顺利通过 ⑶原子核虽很小,但存在,少数![]() 粒子碰到原子核被撞了回来 24、⑴④ ② ⑵①钠(Na) 氟(F)
②AC ③7
粒子碰到原子核被撞了回来 24、⑴④ ② ⑵①钠(Na) 氟(F)
②AC ③7
五、25、⑴![]() ⑵76 ⑶24:4:48 ⑷63.2% 26、
⑵76 ⑶24:4:48 ⑷63.2% 26、![]() ,
,![]() 为混合物。
为混合物。