盐城市初级中学2005-2006学年度第一学期月考
初三年级化学试题(2005.12)
命题人:季进明 审核人:卞玉梅、季进明
相对原子质量H:1;C:12;O:16;F:19;Na:23;Mg:24; P:31; Cl:35.5; Ca:40
一、选择题:(每小题只有一个选项符合题意,1~13每题1分,14~26每题2分,计39分)
1、发现室内煤气泄漏使人中毒时,应采取的措施是( )
A.就地做人工呼吸 B。立即关闭煤气阀门,打开门窗
C.就在拨打急救电话120,等医生来 D。立即打开换气扇开关
2.下列说法中正确的是( )
A.钠原子失去一个电子就变成稀有气体元素氖原子
B.氯原子得到一个电子后与氢原子电子层结构相同
C.两种粒子次外层电子数相同,它们的化学性质一定相同
D.原子最外层数少于4个的元素,一定是金属元素
 3.下列化学方程式中,正确的是( )
3.下列化学方程式中,正确的是( )
A.Al+O3=AlO3 B.2H2O 2H2↑+O2↑
![]() C.2Fe+6Cl 2FeCl3+3H2↑ D.2H2+O2 2H2O↓
C.2Fe+6Cl 2FeCl3+3H2↑ D.2H2+O2 2H2O↓
4.下列有关金属的说法中,错误的是( )
A.生铁的含碳量比钢低 B。在空气中,铝的表面能形成氧化物薄膜
C.镀锌的白铁不易被腐蚀 D。钛具有耐蚀性,可用来制造轮船外壳
5.下列各组气体中,通常情况下,既无可燃性,也无助燃性的是
A.H2,O2 B。CO2,O2 C。CO2,O2 D。CO2,N2
6.下列各组物质中,碳元素化合价从高到低排列的是( )
A.Cu0、CO、CO2 B.CH4、CO、Na2CO3 C.CaCO3、CO、C D.NH4HCO3、CO、CO2
7.下列物质中能在空气中燃烧,且燃烧后气体的分子数肯定减少的是( )
A.木炭 B。硫磺 C。红磷 D。细铁丝
8.下列反应中,生成物为C,若C的化学式为AB3,则反应的化学方程式为( )
![]() A.3AB+B2 2C
B。2AB+B2 2C
A.3AB+B2 2C
B。2AB+B2 2C
C.2AB2+B2 2C D。2AB2+2B 2C
9.下列说法不正确的是( )
A.锌和稀硫酸完全反应后得到的液态残余物属于混合物
B.生成物是一种单质和一种化合物的反应不一定是置换反应
C.特殊条件下,将石墨转化为金刚石的变化是化学变化
D.一般说来,氢气和二氧化碳的收集方法完全相同
10.拉瓦锡研究空气的成分时曾得出了如下两点结论:①空气是由氧气和氮气组成的;②空气中氧气的体积分数为20%。现在你认为拉瓦锡的这两点结论( )
A.只有①正确 B。只有②正确 C。①②都不正确 D。①②都正确
11.下列叙述完全符合质量守恒定律的是( )
A.水结成冰前后,质量保持不变
B.50mL水和50mL乙醇混合后总体积小于100mL
C.在90g水中含有10g氢气和80g氧气
D.3g碳与适量氧气反应可生成11g二氧化碳
12.下面一些化学常识与我们息息相关,其中错误的是( )
A.通常的食醋中约含3%-5%的醋酸
B.医用消毒剂含酒精质量分数越大,杀菌消毒效果越好
C.空气中分数为0.03%r CO2不可少,但达到 10%就能使人窒息而死
D.工业酒精中含少量的甲醇,不能饮用,也不能配酒出售
13.明年1月起,苏北地区全面推广使用乙醇汽油,所谓乙醇汽油就是在汽油中加入适量的乙醇混合而成的一种燃料。下列叙述错误的是( )
A.乙醇汽油是一种新型的化合物 B。汽车使用乙醇汽油后能减小有害气体的排放
C.用石油为原料可制得汽油 D。乙醇可由玉米和高粱等发酵制得
14.自2003年6月1日开始,三峡蓄水工程正式启动,三峡工程的年发电量相当于每年燃烧3000万吨原煤产生的电能,三峡工程将有助于控制( )
①温室效应 ②白色污染 ③SO2排放 ④烟尘排放
A.①②④ B。①②③ C。①③④ D。②③④
15.欲除去一氧化碳中混有的少量的二氧化碳,采取的最恰当的措施是将气体( )
A.通过灼热的氧化铜 B。点燃
C.通过足量石灰水 D。通入石蕊试液
16.下列物质中,只含C、H、O三种元素,且属于有机化合物的是( )
![]() A.白酒 B。甲烷 C。碳酸 D。醋酸
A.白酒 B。甲烷 C。碳酸 D。醋酸
17.将燃着的镁条伸入盛有二氧化碳的集气瓶中,镁条继续燃烧,反应式表示为2Mg+CO2 2MgO+C,则下列叙述中错误的是
A.该反应中镁发生了氧化反应 B。该反应属于置换反应
C.镁着火后不能用CO2灭火 D。该反应中MgO作氧化剂
18.下列关于生铁和钢的叙述,正确的是
A.由铁矿石炼成铁是化学变化,由生铁炼成钢是物理变化
B.用铁制容器盛放硫酸铜溶液,容器易被腐蚀
C.生铁和钢都是铁、碳合金,它们在性能和用途上差别不大
D.它们都能完全溶解在盐酸中
19.下列各组名称所代表的物质均属于同一物质的是
A.石灰浆、碳酸钙 B。干冰、二氧化碳
C.一氧化碳、水煤气 D。碳酸钙、生石灰
20.组成溶液的溶质
A.只能是固体 B。只能是液体
C.只能是气体 D。可能是气体、液体或固体
21.下列实验叙述中,正确的是
A.酒精灯中的酒精不能超过其容积的1/3 B。量筒一般用于测量液体的体积
C.可用酒精灯引燃另一只酒精灯 D。过滤时,滤纸要高于漏斗的上边缘
22.下列物质与适量的水混合振荡后,可以形成溶液的是
A.面粉 B。汽油 C。蔗糖 D。植物油
23.20℃时,NaCl的溶解度是36g。在20℃时将20gNaCl放入50g水中充分搅拌,静置后得到溶液质量为
A.86g B。70g C。68g D。136g
24.最近科学家经过确认,存在一种化学式为N5的分子,这一发现可能开辟世界能源的新领域,它可能成为一种好的火箭燃料,下列关于N5的说法正确的是
A.N5是一种化合物 B。N5的相对分子质量为140kg
C.N5中氮元素显零价 D。N5这种物质是由氮原子直接构成的
25.下列各组气体,在同温同压下按密度由大到小的顺序排列的是
A.CO2、CH4、H2 B。CO、CO2、H2
C.H2、CH4、CO2 D。O2、CH4、CO
26.下列措施中不可改变固体溶解度的是
A.增加溶剂水的量 B。改变溶液的温度
C.改变溶剂的种类 D。改变溶质的种类
二、填空题(共32分)
27.(2分)干涸的深井、深洞和久开启的菜窖的底部 浓度较大,在进入这些地方前,须做 试验。
28.(6分)(1)指出下列溶液中的溶质:①硫酸铜溶液 ②稀硫酸 ③铁和盐酸恰好完全反应后的溶液 ;
(2)现有一瓶20℃时接近饱和的硝酸溶液,欲将它转化为饱和溶液,可采取的措施是 、 、 。
29.(3分)把一团光亮的铁丝放入大试管内,将试管倒插入水中后再固定好(试管中水面与烧杯中水相平,设温度不变,装置见右图),放置足够的时间后,观察到铁丝表面的变化是 ,试管内的水面将 ,此时试管内气体的压强将 。
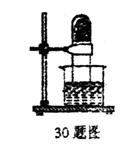 30.(6分)以Fe2O3、H2O为原料,制取Fe3O4,请用化学方程式表示其中的反应:
30.(6分)以Fe2O3、H2O为原料,制取Fe3O4,请用化学方程式表示其中的反应:
(1)分解反应: ;
(2)置换反应; ;
(3)化合反应: 。
 31.(4分)已知氨气(NH3)具有还原性,把氨气通过灼热的氧化铜(如图所示),结果黑色粉末变成亮红色,同时生成水和一种气态单质,试写出氨气和氧化铜反应的化学方程式
;该实验中试管口部略向下倾斜是为了
;反应完成后停止加热,继续通氨气至试管冷却是为了防止
。
31.(4分)已知氨气(NH3)具有还原性,把氨气通过灼热的氧化铜(如图所示),结果黑色粉末变成亮红色,同时生成水和一种气态单质,试写出氨气和氧化铜反应的化学方程式
;该实验中试管口部略向下倾斜是为了
;反应完成后停止加热,继续通氨气至试管冷却是为了防止
。
32.(3分)某种无色气体可能含有氢气、一氧化碳、二氧化碳和氖气中的一种或几种气体。当混合气体依次通过紫色石蕊试液时,试液没有变色;通过灼热的氧化铜时固体变成红色,再通过澄清石灰水时,石灰水变成浑浊。该混合气体中一定含有 ,一定不含有 ,可能含有 。
33.(5分)第五章所见的A、B、C、D、E五种物质,其中B、D通常状况下为液体,A、E为气体,A、B、C三种物质都是汽水饮料中含有的物质。它们之间有如下转化关系,A、B两种物质在不同条件下可分别发生①和②两个反应,反应①和光合作用。试回答下列问题:
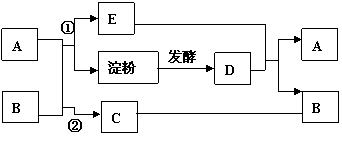
(1)写出化学式:A ,B ,C
(2)写出D与E反应的化学方程式: 。
34.(3分)我市拥有几百公里长的海岸线和较为发达的农牧业,请你回答下列问题:
(1)下列情况下,不会造成海洋污染的是 。
A.垃圾填海 B。油轮上原油泄漏
C.利用潮汐发电 D。利用海风推动发电机发电
(2)关于沿海的海洋资源的利用中,你认为能实现的是 。
A.海水养殖 B。远洋运输 C。海洋捕捞 D。海水淡化
(3)每到麦子和水稻收获的季节,田野里有许多秸秆。你认为处理秸秆的方法是 。
A.就地焚烧作肥料 B。制沼气
C.粉碎后做饲料 D。堆在田里让其在田里腐烂
三、实验题:(共18分)
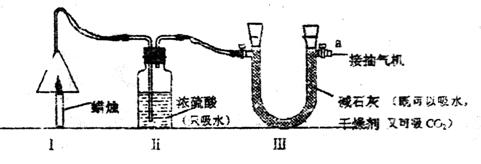 35.(7分)为了测定石蜡中碳,氢两种元素的质量比,某化学兴趣小组设计了如图所示的实验,实验步骤如下:先分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量。按图示连接仪器装置,点燃蜡烛,同时从a导管口抽气,一段时间后熄灭蜡烛,再分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量,设每步吸收是完全的。实验数据如下表。
35.(7分)为了测定石蜡中碳,氢两种元素的质量比,某化学兴趣小组设计了如图所示的实验,实验步骤如下:先分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量。按图示连接仪器装置,点燃蜡烛,同时从a导管口抽气,一段时间后熄灭蜡烛,再分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量,设每步吸收是完全的。实验数据如下表。
|
| 蜡烛 | 装置Ⅱ | 装置Ⅲ |
| 反应前的质量/g | 25.9 | 280.6 | 115.5 |
| 反应后的质量/g | 24.5 | 281.8 | 119.9 |
(1)该实验中测得水的质量为 g,二氧化碳的质量为 g.
(2)由该实验数据计算,蜡烛中碳、氢元素的质量比为 。
(3)装置Ⅱ、装置Ⅲ的顺序能否颠倒? ( 选填“能”或“不能”)
(4)理论上,装置Ⅱ、装置Ⅲ增加的质量之和大于蜡烛减轻的质量,其原因是
。
(5)该实验能否准确测出蜡烛燃烧生成的二氧化碳和水的质量? (选填“能”或“不能”),理由是 。
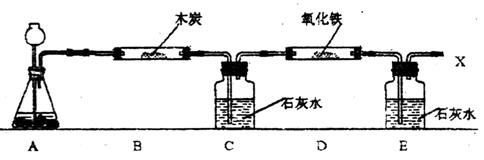 36.(11分)下面是用二氧化碳制备某种还原性气体并用于还原氧化铁的装置(已略去了加热的仪器)。请据图回答:
36.(11分)下面是用二氧化碳制备某种还原性气体并用于还原氧化铁的装置(已略去了加热的仪器)。请据图回答:
(1)装置A中的药品是 ,反应时A处的现象是 ;
装置A中发生反应的化学方程是 。
(2)装置D中反应的化学方程式是 。
(3)C、E两处都可看到的现象是 。
反应的化学方程式是 。
(4)从X导管导出的气体中肯定含有对人体有害的 ,你准备如何处理它 。
四、计算题(共11分)
 37.(5分)右图是一种牙膏包装盒上的部分说明。其主要成分单氟磷酸钠(Na2PO3F)是牙膏中常用的添加剂之一,试验表明牙膏中单氟磷酸钠的质量分数达到0.76%~0.80%时,防蛀牙的效果较好。请计算:
37.(5分)右图是一种牙膏包装盒上的部分说明。其主要成分单氟磷酸钠(Na2PO3F)是牙膏中常用的添加剂之一,试验表明牙膏中单氟磷酸钠的质量分数达到0.76%~0.80%时,防蛀牙的效果较好。请计算:
(1) 单氟磷酸钠的相对分子质量。
(2) 单氟磷酸钠中氟元素的质量分数。
(3)通过计算判断,该牙膏是否有较好的防蛀牙效果。
38.(6分)有一石灰石样品,其中含有的杂质是不溶于水,也不与盐酸反应耐高温的固体。某学生想测定该样品的纯度,他取用10g这种石灰石样品,把100g稀盐酸分4次加入,充分反应后剩余固体的质量如下表:
| 稀盐酸的用量 | 剩余固体的量 |
| 第1次加入25g | 6.5g |
| 第2次加入25g | 3.0g |
| 第3次加入25g | 1.5g |
| 第4次加入25g | 1.5g |
问:(1)10g石灰石样品中,含杂质的质量是多少克?
(2)石灰石样品中碳酸钙的质量分数是多少?
(3)1000kg这种石灰石充分燃烧,可得到固体多少千克?