初三化学模拟试卷
一、选择题:
1、下列变化中,肯定是化学变化的是( )
A.爆炸 B.干冰升华 C.燃烧 D.空气液化
2、下列说法不正确的是( )
A.水银不是银 B.铅笔不含铅
C.生铁不含铁 D.纯碱不是碱
3、下列化学肥料属于复合肥料的是( )
A.尿素 B.硫酸钾 C.过磷酸钙 D.硝酸钾
4、下列物质中存在自由移动的氯离子的是( )
A.液态氯化氢 B.氯酸钾溶液 C.食盐晶体 D.氯化亚铁溶液
5、下列物质在空气中因发生化学变化质量会增加的是( )
A.浓盐酸 B.粗盐 C.生石灰 D.硝酸钾
6、当今世界上的三大环境问题是:酸雨、温室效应和臭氧层衰竭,其中形成酸雨的主要原因是燃烧化石燃料向空气中排放了大量的气体是( )
A.SO2 B.CH4 C.CO2 D.CO
7、园林工人在树身上涂上一层石灰浆,石灰浆的作用是( )
A.美观作用 B.标记作用
C.杀菌作用 D.以上三种说法都不对
8、将空气依次通过足量的烧碱溶液、浓硫酸、灼热的铜网,最后得到的气体是( )
A.氮气 B.氧气
C.二氧化碳和水水蒸气 D.氮气和稀有气体
9、下列各组中的离子,在PH〈7 的溶液中可能大量共存的是( )
A. Ba2+、Mg2+、NO3-、SO42- B.Fe3+、Al3+、Cl-、SO42-
C. NH4+、Na+、Cl-、OH- D.K+、NH4+、CO32-、NO3-
10、下列物质的变化,必须是通过加入盐的溶液才能一步实现的是( )
A.CaO→CaCl2 B.K2CO3→KCl
C.CaCl2→CaCO3 D.Mg(OH)2→MgCl2
11、有A、B、C三种物质各15g,在一定条件下充分反应后只生成30gD,若增加10gC,A与C恰好完全反应,则参加反应的A、B的质量比为( )
A.2:3 B.3:2 C.5:2 D.5:3
12、下列混合物加入到足量的水中充分搅拌,沉淀物肯定只有1种的是( )
A.Fe、CuSO4、NaCl B.Fe、CuSO4、Ag
C.Na2CO3、CaCl2、CaCO3 D.Ba(OH)2、CuCl2、CuSO4
13、下列各组稀溶液中,利用组内物质的相互反应,就能将各种物质鉴别出来的是( )
A.Na2CO3、H2SO4、HCl、KNO3
B.CuSO4、KOH、NaC l、NaOH
C.Na2SO4、Na2CO3、BaCl 2、HNO3
D.NaNO3、MgCl2、KCl、Ba(OH)2
14、食盐、食醋和纯碱均为家庭厨房中常用的物质,利用这些物质你能完成的实验是⑴检验自来水中是否含有氯离子;⑵鉴别食盐和纯碱;⑶检验鸡蛋壳中是否含有碳酸钙;⑷除去热水瓶中的水垢
A.⑴⑵ B.⑴⑶ C.⑴⑷ D.⑵⑶⑷
15、向Zn(NO3)2和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,洗涤,向滤渣中加入盐酸,有气泡产生,则滤液中存在的阳离子有( )
A.NO3- B.Zn2+ C.Cu2+ D.Fe3+
16、可以鉴别稀盐酸、石灰水、食盐水的试剂是( )
A.氧化铜 B.氯化钡溶液
C.碳酸钠溶液 D.氢氧化钡溶液
17、某气体在氧气中的燃烧后的产物依次通过浓硫酸和氢氧化钠溶液,经完全吸收后,测得两溶液增重的质量比为9:11,则该气体可能是( )
A.C2H5OH B.CH4和CO的混合气体
C.C2H2 D.CO和H2的混合气体
18、为完全中和一强碱溶液,需用一定量的盐酸,如果改用相同质量的硝酸,反应后溶液的PH为( )
A.大于7 B.小于7 C.等于7 D.等于0
19、1923年丹麦化学家布郎斯台提出一理论叫酸碱质子理论。该理论认为凡是能释放质子(H+)的任何物质(包括分子或离子)都是酸,任何能接受质子的分子或离子都是碱。根据这一理论,下列各项中既属于酸又属于碱的是( )
A.H2SO4 B.OH- C.HNO3 D.HCO3-
20、日常生活中许多问题涉及到化学知识,下列认识不正确的是( )
A.“西气东输”工程中的“西气”主要指CH4
B.“绿色食品”是指颜色一定是绿色的食品
C.通常所说“煤气中毒”是指CO气体中毒
D.“白色污染”是指“塑料垃圾”对环境的污染
二、填空题:
1、用化学符号表示:
⑴2个硫离子 ⑵2个氧原子
⑶3个镁离子 ⑷硝酸
⑸硝酸汞中汞显+2价 ⑹5个氯化氢分子
2、在石灰石、熟石灰、胆矾、食盐、锌、铝、烧碱、纯碱、乙醇、甲醇等物质中,按下列要求,选用适当物质,用它们的化学式填空:
⑴日常生活里用作调味品的是 ;
⑵各种饮用酒里含有的有机物是 ;
⑶可用作制波尔多液的碱是 ;
⑷假酒中的有害物质 ;
⑸常用于制干电池的金属是 ;
⑹“侯氏制碱法”制得的碱是 ;
3、按要求写出制取硫酸锌的化学方程式(原料自选,但必须一步完成)
⑴金属氧化物与酸反应
⑵中和反应
⑶盐和酸反应
4、向少量氧化铜和铁粉的混合物中,加入一定量的稀硫酸,反应停止后,过滤去不溶物,向滤液中加铁片,未看到铁片有任何变化,则滤出的不溶物中的一定含有 ,可能含有 ;滤液中一定含有 ;不可能含有 。
5、在实验室进行物质的鉴别或提纯时,需选择合适的试剂,如鉴别石灰水和苛性钠溶液,可选择 (填一种即可),欲除去硝酸钠溶液中的少量硫酸铁,若只允许使用一种试剂,则应选择 ,该试剂在溶液中的电离方程式为 ;若可以使用两种试剂,则应选择 和 。
6、生石灰、无水硫酸铜、浓硫酸分别接触空气,均能吸收 ,检验水蒸气常用 ,除去水蒸气常用
7、(1)往盛有少量稀硫酸的试管里放入生锈铁钉,待铁锈消失后即取出铁钉,再往试管里滴入氢氧化钠溶液,会有沉淀出现。写出有关的化学方程式。 、
(2)我国古代,劳动人民就会利用燃烧天然气(主要成分是甲烷)熬制井盐。甲烷在空气中完全燃烧:
(3)、我国劳动人民早已在生产实践中积累出“百炼成钢”的经验。不断地将烧红的生铁放在铁砧上反复锤炼(敲打),使生铁变成性能较好的钢。试写出其中主要反应的化学方程式: 。
(4)某固体粉末由氯化钡、氯化钠、氯化钙、碳酸钠四种中的一种或若干种组成。取少量该粉末置于水中,搅拌,得无色溶液。向溶液滴入硝酸银溶液,有白色沉淀出现,再加稀硝酸,仍有部分白色沉淀不能溶解。该粉末由(写化学式) 组成。
8、(1)最新科技报道,夏威夷联合天文中心的科学家在宇宙中发现了氢元素的一种新粒子,它的组成可用H3+表示。1个H3+粒子中含有 个质子,
个电子。
(2)已知明矾是一种良好的净水剂,可用于家庭饮水的净化,它的化学式是:KAl(SO4)2・12H2O,明矾溶于水后,电离方程式:KAl(SO4)2=K++A13++2SO42-,请回答下列问题:
①明矾是由 种元素组成。
②往明矾水溶液中滴加几滴氯化镁溶液,是否有明显现象出现 (填:“是”“否”)
③已知K2SO4溶液、KCl溶液的PH=7,A1C13溶液、A12(SO4)3溶液的PH<7。请猜想用明矾净化后的水,其PH 7。(填“>”、“<”或“=”)
三、实验题:
1、为了证明长期暴露在空气中的氢氧化钠溶液已变质,可选择三种不同物质类别(酸、碱、盐)的试剂分别进行实验。试用化学方程式表达出来。
⑴
⑵
⑶
2、水蒸气通过灼热的煤所产生的混合气,其主要成分是CO、H2,还含有CO2和水蒸气。请用下图的装置设计一个实验,以确认上述混合气中含有CO和H2。
⑴连接上述装置的正确顺序是(填各接口的代号字母);
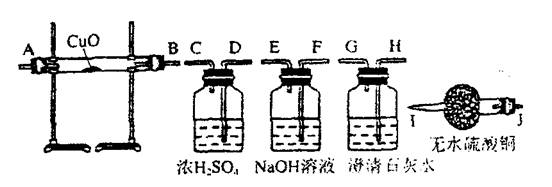 混合气→(
)( )接(
)( )接(
)( )接(
)( )接(
)
混合气→(
)( )接(
)( )接(
)( )接(
)( )接(
)
⑵确认混合气中含有H2的实验现象。其理由是 。
⑶确认混合气中含有CO的实验现象。其理由是 。
⑷使剩余的CO气体不能排入大气污染环境的措施是 。
四、计算题:
1、钙是青少年生长发育所不可缺少的重要元素。一体重为50kg的缺钙学生,根据医生建议,每天除了从食物中补充钙以外,还需要从药物中补充0.4g钙。问如用碳酸钙来补充钙质,每天需服用碳酸钙多少克?
2、取碳酸钠和氯化钠的固体混合物13.6g与一定质量的稀盐酸恰好完全反应,得到10%的氯化钠溶液147g,计算:
⑴固体混合物中碳酸钠的质量分数;
⑵生成二氧化碳的质量;
⑶该盐酸中溶质的质量分数。
初三中考模拟试卷
一、选择题
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | C | C | D | D | C | A | C | D | B | C | B | C | C | D | B | C | D | A | D | B |
二.题空题
1(1)2S2- (2)2O (3)3Mg2+ (4)HNO3 (5)Hg(NO3) 2 (6)5HCl
2.(1)NaCl (2)C2H5OH (3)Ca(OH)2 (4)CH3OH (5)Zn (6)Na2CO3
3.(1) ZnO+H2SO4=ZnSO4+H2O
(2) Zn(OH)2+H2SO4=ZnSO4+2H2O
(3) ZnCO3+H2SO4=ZnSO4+H2O+CO2↑
4 Cu ;Fe ;FeSO4; H2SO4,CuSO4
5. Na2CO3溶液 ; Ba(OH)2溶液 ; Ba(OH)2=Ba2++2OH-
NaOH溶液;Ba(NO3)2溶液
6H2O;CuSO4;浓H2SO4
7.(1)3H2SO4+Fe2O3=Fe2(SO4)3+3H2O
Fe2(SO4)3+6NaOH=3Na2SO4+2Fe(OH)3 ↓
![]()
![]() (2)CH4+2O2======CO2+2H2O
(2)CH4+2O2======CO2+2H2O
(3)C+O2=====CO2
(4)NaCl.Na2CO3
8.(1)3 2 (2)5 否 (3) 〈
三、实验题:
1(1)Na2CO3+2HCl==2NaCl+H2O+CO2↑
(2)Na2CO3+CaCl2==CaCO3↓+2NaCl
(3)Na2CO3+Ba(OH)2==BaCO3↓+2NaOH
2(1)FEDCABJ或FEDCBAJ
(2)黑色的氧化铜变红,无水硫酸铜变蓝
(3)黑色的氧化铜变红,澄清石灰水变浑浊
(4)在G出口处点燃(或用气球.塑料袋收集)
四、计算题 1.1克 2.(1)78.0 % (2)4.4 (3)5.3%