第八章 食品中的有机物 B卷
一、选择题
1、 下列物质中,不属于有机物的是()
A、纤维素 B、蛋白质 C、淀粉 D、二氧化碳
2、 下列物质属于有机高分子化合物的是()
A、甲烷 B、二氧化碳 C、淀粉 D、金刚石
3、人们把把食品分为“绿色”食品、“蓝色”食品、“白色”食品等。“绿色”食品是绿色植物通过光合作用转化的食品;“蓝色”食品是海洋提供的食品;“白色”食品是通过微生物发酵的食品。下列食品中属于白色食品的是()
A、莱油 B、面粉 C、海带 D、食醋
4、相同质量的下列物质在人体内氧化,放出热量最多的是()
A、油脂 B、葡萄糖 C、蛋白质 D、纤维素
5、下列有关实验现象的描述错误的是()
A、高锰酸钾溶于水,溶液呈紫红色
B、硫在空气中燃烧发出明亮的蓝紫色火焰
C、淀粉遇到碘水变蓝色
D、蛋白质遇到浓硝酸变黄色
6、食用下列食品,通常下会对人体健康造成危害的是()
A、用甲醛溶液浸泡的海鲜品
B、用工业食盐腌制的泡菜
C、霉变的大米、花生
D、牛奶经工业发酵后得到的酸奶
7、植物为人类提供了大量的营养物质,某些儿童由于偏食(不吃蔬菜、水果),结果生长发育出现障碍,患营养缺乏症,这些病症曾成为医学难题。这是由于摄入物质不足而引起的()
A、维生素 B、蛋白质 C、油脂 D、糖类
8、导致老年人骨质疏松的主要原因是人体骨骼中缺乏下列元素中的()
A、Ca B、Na C、Fe D、K
9、目前许多城市的公交车上印有(CNG)(“压缩天然气”的英文缩写)的标志。CNG的使用,可以大大降低汽车尾气的排放,减少空气污染,提高城市生活质量。“CNG”的主要成分的化学式为()
A、C2H6O B、C2H4O2 C、CH4 D、CH4O
10、已知几种食品的pH如下表
| 食品 | ①苹果 | ②香蕉 | ③鸡蛋 | ④玉米粥 | ⑤西瓜 | ⑥茶叶 |
| pH | 3.1 | 4.6 | 7.8 | 7.6 | 6.3 | 5.0 |
以上能用来缓解胃酸过多的一组物质是()
A、①③ B、②④ C、⑤⑥ D、③④
11、苯甲酸(C6H5COOH)及其盐可用作食品防腐剂,已知苯甲酸的酸性比醋酸的强。下列对苯甲酸性质的推测不合理的是()
A、苯甲酸溶液能跟活泼金属反应
B、苯甲酸溶液的pH小于7
C、苯甲酸溶液能使紫色石蕊试液变红
D、苯甲酸溶液能跟所有的盐反应
12、过氧乙酸的分子结构如图所示(注:![]() --表示碳原子;
--表示碳原子;![]() --表示氧原子;
--表示氧原子;![]() --表示氢原子)。有关过氧乙酸的下列叙述不正确的是()
--表示氢原子)。有关过氧乙酸的下列叙述不正确的是()
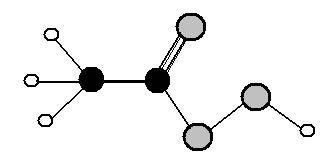
A、 过氧乙酸分子的化学式为C2H4O3
B、 其相对分子质量为76
C、 C、H、O三种元素的质量比为2∶4∶3
D、 完全燃烧生成CO2和H2O
13、液化石油气作为燃料,已普遍进入城市家庭,它是含有下列物质的混合物,在常压下这些物质的沸点如下表所述:
| 物质名称 | 乙烷 | 丙烷 | 丁烷 | 戊烷 | 己烷 |
| 沸点/℃ | -88。6 | -44。2 | -0。5 | 36.1 | 69.2 |
在常温下使用至无气体放出时,钢瓶中常剩余一些液态物质,这些物质是最有可能是是( )
A、 乙烷、丙烷和丁烷
B、 乙烷和丙烷
C、 只有乙烷
D、 戊烷和己烷
二、填空题
14、现有大豆、玉米、花生、鲜鸡蛋、精面粉、白砂糖、奶油、食盐、味精、柠檬汁等,其中富含蛋白质的有 ,富含糖类的有
,富含油脂的有 富含
维生素是有 。
15、在人的胃液中,HCL的质量分数大约是0。45﹪~0.6﹪。胃液中的盐酸是有胃肠的壁细胞分泌的,它具有以下生理功能:①促进胃蛋白酶的催化作用,使蛋白质易水解而被人体吸收;②使糖类物质进一步水解;③杀菌。请结合上述内容回答下列问题:
(1)如用 MgCO3和Al(OH)3的混合粉剂治疗胃酸过多,则发生的化学反应方程式为
; 。
(2)从元素的组成来看,食用适量是NaCL有利于 。
A.促进消化分泌物的产生
B.骨骼中钙质的增加
C.治疗胃酸过多
D.治疗缺碘性甲状腺肿大
16.维生素C(C6H8O6)主要存在于蔬菜、水果中,它能增强人体对疾病的抵抗能力。
(1)取3片维生素C压碎后溶液于10mL水中过滤,取少量滤液向其中滴加几滴紫色石蕊试液,试液变红,证明维生素C的水溶液显 性。
(2)维生素C在酸性环境中比较稳定,在高温时易被破坏。请你想一想,如何食用黄瓜,才能充分利用黄瓜中丰富的维生素C?
17、科学家预言:“未来最理想的燃料是绿色植物。”绿色植物的秸杆[主要成分是纤维素,化学方程式为(C6H10O5)n],在适当催化剂的作用下与水作用生成葡萄糖。葡萄糖在有适当的催化剂的条件下可转化成乙醇(C2H5OH)和二氧化碳。写出由纤维素制乙醇的化学方程式:
、 。
18、20世纪科学技术的发展,为人们提供了可以观察和操纵单个原子和分子的可能性,从而实现了直接用原子来制造分子。葡萄糖是人体需要的重要是营养物质之 其化学式为(C6H12O6)
若采用上述方法制造葡萄糖,请你指出所需要的原子名称: 。
19、下表列出两种食品部分营养成分,请仔细阅读后,回答下列问题。
| 营养成分 | 单位 | 每百克平均含量 | |
| 食品甲 | 食品乙 | ||
| KJ | 2100 | 1700 | |
| 糖类 | g | 78 | 50 |
| 脂肪 | g | 28 | 6 |
| 蛋白质 | g | 24 | 6 |
| 钙 | mg | 930 | 200 |
| 磷 | mg | 720 | 150 |
(1)没100克食品中所含营养成分质量最大的是 ,表中所列营养成分中属于有机物是有 。
(2)某同学准备到野外探险,在上述食品中进行选择,你建议他携带食品
(填“甲”或“乙”),你建议的依据是
21、现有一种人工制成的膜,为探究淀粉和碘能否透过该膜,用铁架台、烧杯、用这种膜制成的袋、细棉线、1%的淀粉溶液、稀碘溶液等用品,设计如图8-2所示的实验装置:
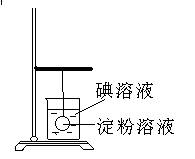
(1)碘能使淀粉变蓝,这是碘的 性质。(填“物理”或“化学”)
(2)如果实验结果是袋内外液体均不变蓝,则表明淀粉和碘均不能透过该膜;如果袋内液体变蓝,袋外液体不变蓝,则表明 。
22葡萄糖在人体组织中慢慢氧化放出的热量,是人类生命活动所需能量的重要能量的重要来源之一。葡萄糖的化学式为C6H12O6,从葡萄糖的分子式你能总结出哪些信息(请写出两条)?
;
。
24、某同学用如图所示装置进行“绿色植物光合作用”实验的探究实验。先将甲、乙两个装置同时放在黑暗处一昼夜,然后一起放在阳光下。几小时后检验发现:甲装置中植物是叶片中淀粉生成,乙装置中植物的叶片没有淀粉生成。
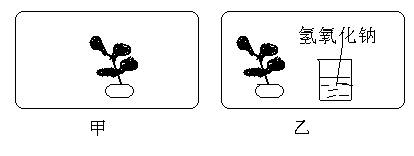
(1)乙装置中绿色植物在阳光下 (填“能”或“不能”)进行光合作用。
(2)乙装制中盛放氢氧化钠溶液的目的是 ,
写出相应的方程式 。
(3)由以上实验可知,绿色植物光合作用的原料是 。
26、乙醇(C2H5OH)俗称洒精,具有可燃性。甲、乙两小组同学为了确定乙醇在氧气中燃烧的产物,他们分别先将乙醇在氧气中点燃,再用燃烧后的混合气体进行如下实验。(实验中所用的新鲜鸭血是指先加入抗凝剂,再用水稀释后的鸭血。它遇氧气呈鲜红色,遇二氧化碳呈暗红色,遇一氧化碳呈胭脂红)甲、乙两小组实验顺序及观察到现象如图所示。
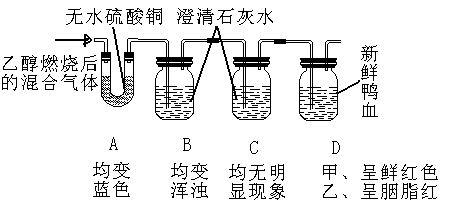
根据以上实验,回答下列问题:
(1)、甲小组确定乙醇燃烧的产物可能是 ;
乙小组确定乙醇燃烧的产物可能是
(2)、分析甲、乙两个小组确定的产物为什么不同?
(3)、把A、B两个装置顺序对调,行吗?为什么?
(4)请你谈谈合理使用燃烧的一种方法:
(5)写出乙醇完全燃烧的化学方程式 。
23、植物进行光合作用时,可表示为: 水+二氧化碳→淀粉+氧气。由此可推断淀粉的组成中一定含有 元素,可能含有 元素。
| 葡萄糖注射液5% Glucose Injcction [规格]500ml内含葡萄糖25g [适应症状]补充能量和体液及全静脉内营养等 [生产日期]04年6月1日 [有效期]07年6月 [产品批号] |
24、医生给病人输液时,常用葡萄糖注射液。如图为葡萄糖注射液的部分标签图,根据下图回答下列问题:
(1)葡萄糖是化学式为C6H12O6,它是由 种
元素组成,其相对分子质量是 。
(2)每克葡萄糖完全氧化约放出17。2KJ的能量,一瓶这样的葡萄糖注射液可放出
KJ的能量。
(3)现要配置10Kg这种葡萄糖注射液,需用葡萄糖 Kg
20、人体中的钙元素主要用于骨骼和牙齿中,以羟基磷酸钙晶体[Ca10(PO4)6(OH)2]的形式存在,其相对分子质量为1004。牛奶含钙丰富又易吸收,且牛奶中钙和磷的比例合适,是骨骼的理想食物。如图是某乳业公司包装标签的部分文字。请仔细阅读后回答下列问题:
| 纯牛奶 配料:鲜牛奶 保持期:8个月 净含量:250ml/盒 营养成分:(没100ml) 钙≥0.11g 脂肪≥3.3g 蛋白质≥2.9g |
(1)包装标签上脂肪≥3.3g,是指100ml牛奶中,含脂肪的质量至少为3.3g。那么一盒牛奶含钙至少 g(保留到0.01)
(2) 求羟基磷酸钙中钙元素的质量分数(保留到0.1%)
(3)若人体每天至少需要0.6g 钙,且这些钙有90%来自牛奶,则一个人每天至少要喝多少盒牛奶?
25、人体缺乏维生素C可能的坏血病,维生素C的化学式C6H8O6,在新鲜水果、蔬菜中含量都较高,探究小组测定了某品牌橙汁的维生素C的含量。过程如下:取20。00g橙汁用碘1.00%的碘溶液与其反应,恰巧反应时消耗碘溶液25.40g(反应方程式:C6H8O6+I2= C6H6O6+2HI)。求:
(1)维生素C分子中氧元素的质量分数?
(2)橙汁中维生素C的质量分数?