2005学年初三级下学期第一次月考·化学试卷
说明:请把选择题的正确答案用2B铅笔涂在答题卡上
请用黑色钢笔或签字笔把非选择题的正确答案写在答题卡对应题号的答题框内
可能用到的相对原子质量:
H-1 C-12 O-16 S-32 Cl-35.5 Ca-40 Cu-64
一、选择题 本题共20小题,共40分
1.下列物质属于纯净物的是
A.石灰水 B.稀盐酸 C.水银 D.雪碧
2.人体由于缺乏而造成骨质疏松的是
A.铁 B.铁元素 C.碳酸钙 D.钙元素
3.下列有关铁的描述中,属于铁的化学性质的是
A.软 B.在潮湿的空气中容易生锈
C.能导电 D.熔点高达1535℃
4.下列变化中属于化学变化的是
A.把海水晒成食盐 B.用铁铸造成模具
C.我国出土的商朝铜器表面出有铜绿 D.把铜拉成很长的铜丝
|
|
|
C.Fe2O3 + 3CO === 2Fe + 3CO2 D.2Fe(OH)3 === Fe2O3 + 3H2O
6.下列关于溶液的说法中,正确的是
A.只有水才可以作溶剂
B.一瓶溶液里各部分的性质不相同
C.饱和溶液一定是浓溶液
D.饱和溶液一定是该温度下这种溶质最浓的溶液
7.已知20℃时,氯化钠的溶解度为36g,对这理解正确的是
A.最多能溶解氯化钠36g B.100 g水溶解了氯化钠36g
C.100 g水最多只能溶解氯化钠36g D.20℃时,100 g水最多只能溶解氯化钠36g
8.在下列因素中,影响固体溶解度的是
A.溶质的质量 B.溶剂的质量 C.溶液的质量 D.温度的高低
9.把10g某固体完全溶解在90g的水中,恰如达到饱和,再加入10g该固体,则所得溶液的溶质质量分数为
A.10% B.11.1% C.18.1% D.20 %
10.有X、Y、Z三种金属。将X和Y浸入稀硫酸中,Y溶解,X不溶解;将X侵入Z的化合物的溶液中,在X表面有Z析出。则X、Y、Z的金属活动性由强到弱的顺序是
A.Z、Y、X B.Z、X、Y C.Y、Z、X D.Y、X、Z
11.在过滤的操作中,下列玻璃仪器无需用到的是
A.玻璃棒 B.烧杯 C.量筒 D.漏斗
12.铁在下列各种环境中,保存的时间最久的是
A.潮湿的土壤中 B.干燥板结的土壤中 C.酸性的土壤中 D.含铜矿的土壤中
13.从1000g溶质的质量分数为98%的浓硫酸中取出10g,则这10g溶液的溶质质量分数为
A.10% B.9.8% C.98% D.1%
14.在氯化亚铁溶液中混有少量的氯化铜,可以用下列哪种物质除去?
A.铜粉 B.盐酸 C.锌粉 D.铁粉
15.最近科学家们发现了一种新型的净水剂铁酸钠(Na2FeO4),该物质铁元素的化合价是
A.+2 B.+3 C.+4 D.+5
16.欲将100g溶质质量分数为20%的氯化钠溶液加变成溶质质量分数为10%的溶液,下列做法可行的是
A.蒸发40g水 B.蒸发50g水 C.加入20g氯化钠 D.加入100g水
17.某学生在做有关溶液的实验时,作了如下的记录,其中你认为恰当的是
A.用托盘天平称取10.01g食盐 B.用100mL的量筒量取50mL水
C.把食盐加入到量筒的水中 D.用玻璃棒搅拌
18.下列物质加入到水中,温度会明显改变的是
A.CuCl2 B.NaCl C.NaOH D.Cu(OH)2
19.下列混合物放置在空气中一段较长时间(不考虑水的蒸发及压强的变化)不会发生明显变化的是
A.食盐水 B.牛奶 C.刚冲好的麦片冲剂 D.澄清石灰水
20.20℃时,氯化钠的溶解度为36g,现把50g氯化钠加入到100g水中,所得到的溶液的溶质质量分数为
A.50% B.36% C.33.3% D.26.5%
二、计算题 本题共2小题,共10分
21.(4分)辉铜矿的主要成分是Cu2S,试计算:
(1)Cu2S中Cu元素的质量分数。
(2)现有含Cu2S 35%的辉铜石,最多能够冶炼出金属铜多少t?
22.(6分)现有150g稀盐酸,向其中加入大理石,直至无气体放出,共收集到8.8g气体。试计算:
(1)参加反应的HCl的质量。
(2)稀盐酸的溶质的质量分数。
三、填空题 本题共7小题,共27分
23.(5分)请用化学用语填空:
(1)2个氮原子___________, (2)2个水分子____________,
(3)3个铁离子___________, (4)4个硝酸根离子_____________,
|
|
|
|
24.(3分)请用C、O、Fe、H四种元素组成下列所要求的物质,用化学式表示:
(1)一种气体_______________, (2)一种金属氧化物_______________
(3)一种酸_______________。
25.(3分)澄清的石灰水___________溶液(填空“属于”或“不属于”,下同),向其中通入足量的二氧化碳气体之后所得的混合物___________溶液,这个过程中所发生的有关反应的化学方程式为:________________________________________________。
26.(2分)在4支试管中分别盛有相同的稀盐酸,将A、B、C和锌四种固体金属分别同时放入其中。小明将观察到的现象画了一幅卡通画,每个卡通人物表示一种金属,周围的小黑点表示反应中生所的气体(如下图所示)。问:
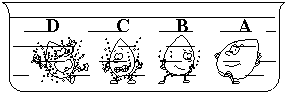
(1)A、B、C三种金属的活动性由强到弱的顺序可能是_______________________。
(2)A可能的表示的金属为____________(填元素符号)。
27.(6分)甲、乙、丙是三种单质,其中甲、丙是固体,乙是气体;A、B、C、D、E都是化合物,其中E是B的水溶液,常存在于大量燃烧煤所导致的酸雨中,而很多建筑物因含有D,易受酸雨的侵蚀。上述物质的相互转化关系如下图所示(部分产物已略去):
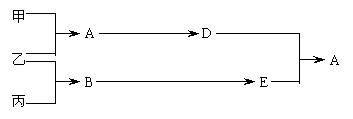 |
(1)写出下列物质的化学式:A ________________,D _________________;
(2)写出反应乙 + 丙 → B的化学方程式:___________________________________。
28.(3分)现有某一硝酸钾溶液,为了确定其是否达到饱和,甲、乙、丙三位同学分别设计了以下的实验,请你判定他们的做法是否可行(填空“可行”或“不可行”):
| 同学 | 方 案 | 现 象 | 结论 | 判定 |
| 甲 | 把溶液放入冰箱中,使其温度降低 | 不久即观察到有固体析出 | 原溶液饱和 | |
| 乙 | 对溶液进行加热蒸发 | 过了一会儿才有固体析出 | 原溶液不饱和 | |
| 丙 | 向原溶液中加入5g硝酸钾,充分搅拌后过滤 | 发现固体没有减少 | 原溶液饱和 |
29.(5分)请列举出能把不饱和的硝酸钾溶液转化为饱和溶液的可行的方法:
(1)__________________________________ (2)__________________________________
(3)__________________________________
请列举出把饱和溶液转化为不饱和溶液的可行的方法:
(1)__________________________________ (2)__________________________________
四、实验题 本题共3小题,共17分
30.(7分)现有以下仪器:
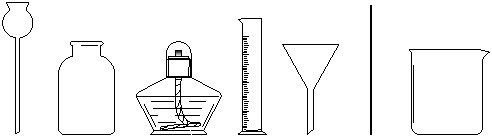
A B C D E F G
(1)可用于热源的仪器是__________________(填写仪器名称,下同);
(2)用于量取液体体积的仪器是__________________;
(3)在溶解、过滤、蒸发、称量时均需要用到一种玻璃仪器,它是_______________,它在各操作中的作用分别为:
| 操 作 | 用 途 |
| 溶 解 | |
| 过 滤 | |
| 蒸 发 | |
| 称 量 |
31.(7分)实验室现有下列药品:盐酸(5%),硫酸(5%);大小相同的镁片、铝片、铁片;铁粉,铝粉。某同学为了比较金属与酸的反应,按下图所示的实验方案进行实验。

① ② ③
从实验开始到反应5分钟,所观察到的现象记录如下:
| 编号 | ① | ② | ③ |
| 现象 | 金属表面立即有大量无色气泡冒出,反应不到5分钟金属已消失 | 金属表面慢慢有少量无色气泡冒出,反应到5分钟时,铝片还在冒气泡 | 铁粉中不断有无色气泡冒出,气泡的量比②中多,溶液逐渐显线绿色,反应到5分钟时,铁粉还在冒气泡 |
该同学根据上述实验现象得出结论:金属与酸反应的剧烈程度按镁、铁、铝的顺序减弱。
你认为该同学的结论是否合理(填“合理”或“不合理”)________________________,如果有不合理的地方,请你在上述设计的基础上完善该实验,在下图中填写所需的化学药品;如果合理,可以不填。
|
|
|
|
|
|

① ② ③
32.(3分)稀食盐水与蒸馏水均为无色且密度相当的液体, 除了用品尝的方法将其区分开来以外,还可以用什么样的方法?
(1)_________________________________________________
(2)_________________________________________________
(3)_________________________________________________
(4)_________________________________________________
五、简答题 本题共6分
33.(6分)请用所学知识简要解释下面的现象:
(1)(4分)当打开未经冷冻过的啤酒瓶的瓶盖时,通常会有大量气泡冒出;而把啤酒放入冰箱中冷冻之后再打开,则冒出的气泡较少。
(2)(2分)食盐固体能溶解在水中形成均一、稳定的溶液,这说明了分子、原子的什么性质?
