初三化学上学期月考试题
一、选择题:(共8小题,每小题2分,共16分)
1、化学“家庭小实验”是利用家庭日常生活用品进行化学学习和探究的活动,下列实验中用家庭日常生活用品能够进行的是( )。
①检验纯碱中含有CO32- ②除去热水瓶内壁上的水垢
③检验鸡蛋壳能溶于醋酸 ④检验自来水中含有Cl-
A.①②④ B.①③④ C.①②③ D.①②③④
2、“NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl”是著名的“侯氏制碱法”的重要反应。下面是4位同学对该反应涉及的有关知识发表的部分见解。其中不正确的是
 | |||
 | |||





![]()
A B C D
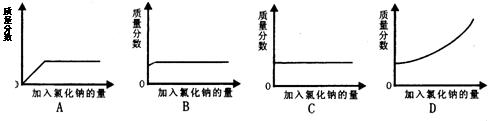 3、向接近饱和的氯化钠溶液中,逐渐加入氯化钠固体,边加边搅拌。下列图形中变化关系正确的是
3、向接近饱和的氯化钠溶液中,逐渐加入氯化钠固体,边加边搅拌。下列图形中变化关系正确的是
4、A图表示硝酸钾和氢氧化钙的溶解度随温度变化的情况。B图中甲、乙试管分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体。向烧杯中加入一种物质后,甲试管中固体减少,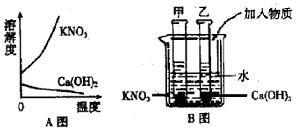 乙试管中的固体增加,则加入的物质不可能是
乙试管中的固体增加,则加入的物质不可能是
( )
A.浓硫酸 B.氢氧化钠
C.氧化钙 D.氯化钠
5、金(Au)、银(Ag)、铜(Cu)曾长期作为货币金属进行流通,我国有着悠久的金属货币历史和丰富的货币文化。下列关于金、银、铜三种金属的说法中,错误的是 ( )
A.金、银、铜都属于不活泼金属
B.单质铜可以将银从硝酸银溶液中置换出来
C. 三种金属原子失去电子能力的大小顺序为:金原子的>银原子的>铜原子的
D. 黄铜(为铜、锌合金)貌似黄金,有人以此冒充黄金行骗,其真伪可用稀盐酸鉴别
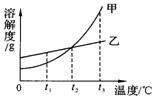 6、根据右图的溶解度曲线,判断下列说法中不正确的是
6、根据右图的溶解度曲线,判断下列说法中不正确的是
A.t1℃ 时,甲物质的溶解度小于乙物质的溶解度。
B.t2℃ 时,甲、乙两物质的饱和溶液中含甲、乙两物
质的质量相等
C.将t3℃ 的甲、乙两物质的饱和溶液降温至t2℃ 时,
都会析出晶体
D.当甲物质中混有少量乙物质时,可采用冷却热饱和液(降温)的方法提纯甲
7、下列叙述正确的是
A.将pH试纸浸入溶液中测溶液的pH
B.用100mL量筒量取5.55mL的稀硫酸
C.将氢氧化钠固体直接放在托盘天平的托盘上称量
D.粗盐提纯主要步骤是:溶解、过滤、蒸发。
8、为测定a、b、c三种金属的活动性强弱,某同学将金属a、b、c分别放入稀硫酸中,b溶解并产生气泡,a、c不反应;另将a放入c的硝酸盐溶液中,a表面析出c。据此分析,三种金属的活动性由强到弱的顺序为
A.b、a、c B.c、b、a C.b、c、a D. a、b、c
选择题答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 |
二、填空与简答题:(每空2分,共26分)
9、我市正在实施一项宏伟的工程----兴建“海上荣成”,旨在充分开发我市濒临的渤海资源 ,造福潍纺人民。小明同学住在渤海边上,他对建设“海上潍纺”的宏伟规划很感兴趣。
 小明模拟化工厂的生产流程,以海水和贝壳(主要成分是碳酸钙)为原料制取生产镁的原料----无水MgCl2 。
小明模拟化工厂的生产流程,以海水和贝壳(主要成分是碳酸钙)为原料制取生产镁的原料----无水MgCl2 。
|
①试剂a是一种溶液,加入该试剂时发生反应的化学方程式 。
②加入试剂后,要将Mg(OH)2沉淀分离出来,应该应用的方法是 ,如果在学校实验室中完成该实验,需要的玻璃仪器除烧杯、玻璃棒外还有 。
③流程中的X是“一定条件下,结晶”,在这里应该采用 结晶的方法。
④金属镁是一种较活泼金属,在二氧化碳气体中也能燃烧。燃烧的化学方程式为
2Mg+C02![]() C+2MgO,此反应类型属于 ( )
C+2MgO,此反应类型属于 ( )
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
10、有A、B、C、D四种物质的溶液,他们分别是硫酸钠、盐酸、氢氧化钡、碳酸钠中的一种,它们之间能发生如下的反应:①A+C→E↓+F ②B+C→G↓+F ③B+D→H+J+K↑
根据以上关系推断:(填化学式)
A.为__________ B.为__________ C.为__________ D.为__________
11、 为了除去粗盐中的Ca2+、Mg2+、SO42-及泥砂,可将粗盐溶于水,然后进行下列五项操作①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液。下列操作顺序中最合适的是_______________________________(填序号)
12、某同学想探究酸碱中和反应是放热反应。进行下列实验操作:取溶质质量分数为20%的稀硫酸30mL,用温度计测出其温度为13℃。然后向其中加入5.6gNaOH固体,恰好完全反应。再用温度计测出温度为22℃。由此,该同学得出NaOH与稀硫酸发生的中和反应是放热反应的结论。请回答下列问题:
(1) 该同学所得的结论的依据是否科学?_____________(选填“科学”或“不科学”)
理由是 。
(2)根据本实验的目的,请你改进他的实验操作 。
三、实验探究题:(每空2分,共30分)
13、小涛在做某次实验时,发现一瓶瓶口敞开不知多久的氢氧化钠溶液(下称试液)。联想到药品保存注意事项,小涛利用提供的试剂(CaCl2溶液、盐酸、CaCO3固体、酚酞)对试液是否变质展开探究。
他首先猜想:试液没有变质,溶液的溶质还是NaOH。
小涛通过查资料知Na2CO3溶液呈碱性。他根据首先的猜想进行的实验是:取少量试液加入试管,滴入酚酞,观察到试液变红。由此得出的结论是原试液没有变质,还是NaOH。
(1)小涛反思实验验证,觉得不够完善,理由是__________________________________。
(2)完善实验方案后,他从提供的试剂中选取一种试剂进行实验发现原试液确已变质。请你写出他这次实验的操作、现象______________________________________________________________
小涛是个爱思考的学生,他又有一个新的疑问:试液中真的没有NaOH了吗?他又作了探究:
(3)猜想:试液中还有NaOH。
(4)实验验证:(要求写出操作、现象)_____________________________________________
___________________________________________________________,试液中还有NaOH。
14、科学探究是奇妙的过程,请你一起参与实验探究。有一包从海水中获得的粗盐,已经经过初步提纯(已除去不溶性杂质)。现在需要进一步提纯和测定粗盐中含NaCl质量分数。
实验一:探究这包粗盐可能含有可溶性的杂质。
(1)查资料获得:粗盐常含有可溶性杂质主要是氯化钙和氯化镁。现用实验验证这包粗盐中的杂质:
(2)取样并溶解,加入数滴NaOH溶液,发现没有明显现象,说明没有___________杂质(填化学式);接着再加入数滴a试剂,有白色沉淀生成,实验证明,这包粗盐可能含有的杂质是_____________(填化学式)。
实验二:提纯并测定这包粗盐中NaCl的质量分数。按下面步骤继续进行实验:
①称取10克粗盐样品,溶于水制成溶液;
②向溶液中加入过量的a试剂,过滤;
③沉淀洗涤后烘干,得到纯净固体A;
④滤液中滴加适量的盐酸后,移入蒸发皿蒸发,得到固体B;
⑤称量实验中得到的某种固体。
(3)在①②④步骤的实验操作中,都需使用到实验仪器是_________________;该仪器在步骤①④操作方法相同,但操作目的不同,在步骤④的操作目的是_________________________。
(4)步骤②中加入过量的a试剂是__________
写出该步涉及到的化学方程式________________________________________________
验证a试剂过量的方法是________________________________________________________。
(5)步骤⑤中,你认为需要称量的固体是A还是B(填A或B)________
选择的理由____________________________________________________________
15、 下图为某同学探究铁、铜、银三种金属活动性顺序的一组实验
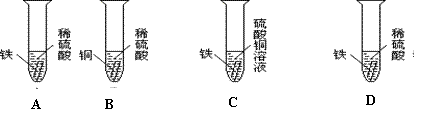 |
(1)上述实验中,有气泡产生的试管中发生反应的化学方程式 。
(2)我国古代“湿法冶铜”就是利用了C中的反应原理,请写出该反应的化学方程式
(3)通过上述实验,还不能证明铁、铜、银三种金属的金属活动性顺序,请你在此基础上补充一个实验帮助这位同学达到实验目的。(写出实验步骤、实验现象和和结论)
四、计算题:(8分)
可能用到的相对原子质量:H:1 Na:23 Cu:64 S:32 O:16
16、将24.9克NaOH溶液跟140克CuSO4溶液混合,两者恰好完全反应,经过滤,得滤液160克,求NaOH溶液的溶质质量分数。
参考答案
一、选择题:(共8小题,每小题2分,共16分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 | C | C | B | D | C | B | D | A |
二、填空与简答题:(每空2分,共26分)
9、①MgCl2 +2NaOH = 2NaCl +Mg(OH)2↓
②过滤 漏斗 ③蒸发 ④ C
10、 A、Na2SO4 B、Na2CO3 C、Ba(OH)2 D、HCl
11、⑤②④①③ 其他合理答案也正确
12、(1)不科学 氢氧化钠固体溶于水时,放出大量的热。将5.6g氢氧化钠固体直接加入稀硫酸中,会使溶液的温度升高。
(2)将氢氧化钠溶于水,冷却至室温后加入到稀硫酸中,测量温度。
三、实验探究题:(每空2分,共30分)
13、(1)Na2 CO3溶液呈碱性,也能使无色酚酞试液变红
(2)取少量试液于试管中。滴入稀盐酸(或CaCl2溶液),观察到有气泡(或白色沉淀)产生
(4)取少量试液于试管中,加入足量的CaCl2溶液,过滤,往滤液中滴加酚酞试液,振荡,溶液变红。
14、(1)MgCl2 (2)CaCl2 (3) 玻璃棒 防止液滴飞溅.
(4)碳酸钠(或Na2CO3) Na2CO3 + CaCl2 = Ca CO3 ↓ +2 NaCl
加入碳酸钠溶液,无白色沉淀生成,证明已过量
(5)A B中固体还含有过量的碳酸钠与盐酸反应生成的氯化钠.
15、(1)Fe+H2SO4==FeSO4+H2 ↑(2)Fe+CuSO4==FeSO4+Cu (2分)
(3)将金属铜置于硝酸银溶液中,铜的表面有白色固体生成,铜的金属活动性比银强。
四、计算题:(8分)
16、16.1%