九年级化学期中考试试卷
(1――4单元)
相对原子质量:H~1 N~14 O~16 S~32 Cl~35.5 K~39 I~127
我能选(每小题只有一个正确答案,请将答案填在答案栏中。共32分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| 答案 |
1、地壳中含量最多的元素是
A、氮 B、氧 C、硅 D、铁
2、室内空气污染危害健康,应引起人们的高度重视。以下不属于室内空气污染物的是
A、厨房烹饪时产生的油烟 B、室内摆放的水果散发出的香味
C、石材释放出的有害放射性气体氡
D、劣质粘合剂释放出的甲醛等有毒物质
3、下列仪器中,不能用酒精灯加热的是
A、试管 B、烧杯 C、集气瓶 D、燃烧匙
4、生活中的下列物质属于纯净物的是 ( )
A、蓝墨水 B、蒸馏水 C、煤 D、啤酒
5、某校907班沈妮同学收集的××药品说明书上这样写到:本品每片主要成分及含量为:Ca 40mg、P 31mg、K 7.5mg、Mg 100mg、Cl 7.5mg、Fe 27mg……。这里的成分及含量是指
A、原子 B、离子 C、分子 D、元素
6、下列所示的实验操作与方法正确的是
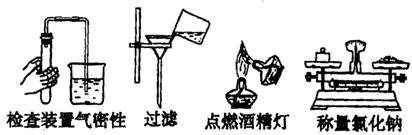
7、下列是日常生活中常发生的一些变化,其中都属于化学变化的一组是
A、水受热沸腾、酒精燃烧 B、汽油挥发、动物的呼吸
C、剩饭变馊、铁锅生锈 D、玻璃破碎、桔子榨成汁
8、1991年,我国著名化学家张青莲教授与另一位科学家合作,测定了铟(In)元素的相对原子质量新值。铟元素的核电荷数为49,相对原子质量为115。铟原子的核外电子数为
A、115 B、49 C、66 D、164
9、阅读下文:在通常情况下,硫化氢是一种没有颜色、具臭鸡蛋气味的有毒气体,经空气重,能溶于水。在空气中点燃硫化氢气体有二氧化硫和水生成。硫化氢的实验室制法是用块状硫化亚铁和液体状稀硫酸反应,则属硫化氢的化学性质的是( )
A、无色 B、有臭鸡蛋气味 C、比空气重 D、能燃烧
10、氯气与水反应生成的次氯酸(HClO)具有杀菌作用,常用于对自来水的消毒。在HClO中,氯元素的化合价为
A、-1 B、+1 C、+3 D、+5
11、一杯混有泥沙且硬度较高的水,使它净化并变成软水的操作有:
①过滤 ②加明矾吸附沉淀 ③蒸馏,正确的顺序应为:
A、①②③ B、②①③ C、②③① D、①③②
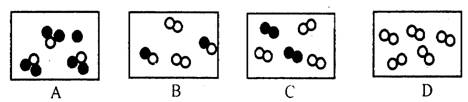
12、下列是表示物质分子的示意图。图中“●”和“○”分别表示两种有不同
质子数的原子,则图中表示单质的是
13、某集气瓶里盛有N2和O2的混合气体(体积比为4:1)。小贝同学要用燃
烧法除去O2而得到较纯净的N2时,你认为她采用的试剂最好是
A、铁丝 B、红磷 C、木炭 D、硫磺
14、下列所述情况①城市生活污水的任意排放;②农业生产中农药、化肥使用
不当;③海上油轮石油泄漏;④工业生产中“三废”的任意排放,可能引起水污染的是
A、只有①③ B、只有①④ C、只有②④ D、①②③④
15、以保护环境和垃圾资源化为目的,将城市生活垃圾进行分类,下列垃圾属于同类物质的是( )
A、废电池、易拉罐 B、废铜烂铁、塑料袋
C、废旧报纸、硬纸板 D、一次性塑料饭盒、空啤酒瓶
16、下列说法完全正确的是( )
A、 氖气的化学式――Ne2
硅的元素符号――Si
2个氮气分子――2N2
B、 决定元素和原子种类――质子数
决定元素的化学性质――最外层电子数
决定元素周期表元素排列顺序――质子数
C、 铁――由分子构成
二氧化碳――由原子构成
氯化钠――由离子构成
D、分子――化学变化中的最小粒子
原子――保持物质化学性质的最小粒子
离子――带电的原子
二、我能填(共34分)
17、用化学符号表示:
(1)空气中含量最多的气体的元素 ;(2)3个氮原子 ;
(3)1个亚铁离子 ; (4)2个二氧化硫分子 。
18、俗语说,酒香不怕巷子深。这句话体现了分子的哪一点性质?
。
19、写出下列化学反应的文字表达式,并注明各物质的化学式。
(1)用过氧化氢溶液制取氧气
(2)铁在氧气中燃烧
20、有些化学实验必须严格遵循操作的顺序,请你举出两个这样的实验,并仿照示例填写下表
| 必须遵循操作顺序的实验 | 先做什么 | 再做什么 |
| 示例:点然氢气 | 先检验氢气的纯度 | 后点燃氢气 |
21、正确认识相关事物的相同点与不同点,是学好化学的关键之一。我们可用
下图来表示事物的异同点。将两种事物的相同点写在两个圆重叠的区域内,每种事物的不同点则写在相应圆中重叠区域以外的部分。请参照下图左侧示例,另外确定一组化学事物,填写在图下面的相应的空格内:
A ;
B ;
a ;b ;c 。
22、根在实验室里制取氧气的研究中,有下列仪器可选用(铁架台、导管、橡皮塞等已省略)
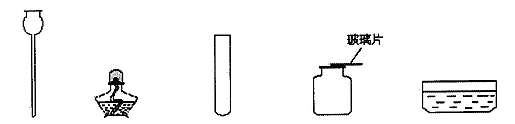
(1)写出编号仪器的名称:① ;② ;③ 。
(2)在实验室里制取氧气,你选用的药品是 。
(3)根据选用的药品,设计一套制取氧气的发生装置。你选用的仪器是(填编号) 。
(4)检查你所设计的装置气密性的方法是
。
(5)收集一瓶较纯净的氧气,比较好的方法是用 。
(6)若要较好地控制产生氧气量的速率,节约反应药品,你对你所设计的装置的评价是:
三、我能分析(共14分)
23、元素周期表是学习和研究化学的重要工具,它的内容十分丰富。下表是依据元素周期表画出的1~18号元素的原子结构示意图。我对它进行研究:

(1)原子序数为16的元素名称是 ,在化学反应中,该元素的原子容易 电子,变成 (填符号);原子序数为11的元素属于 元素,上述两种元素所形成的化合物的化学式为 。
(2)我发现如下规律:①原子最外层电子数一般不超过8个;
②金属元素的原子最外层电子数一般少于4个,非金属元素的原子原子最外层电子数一般多于4个;
③ ;
④ ;
⑤ 。
24某气体由SO2、H2、CO2 中的一种或几种组成。现测知该气体中氧元素的质量分数为50%,则该气体可能有的各种组成为 。
四、我能答:(共10分)
25、现有下列三组物质:①氧气和氢气、②自来水和汽水。请你任选其中一组,用两种方法来区别它们。
(1)你选择一组物质是 。
(2)你区别它们的两种方法是(写出实验步骤、现象和结论):
26、小明同学打算自己探究一下MnO2在分解过氧化氢时所起的作用,但手边没有现成的MnO2药品,只有高锰酸钾,30%过氧化氢溶液、木条、水、火柴,其它仪器可任选。
(1)若要先得到MnO2粉末,反应原理是(用化学式表示化学反应) ,装置为 (用图示)
(2)已知实验(1)中试管中剩下两种物质,其中二氧化锰难溶于水,而另一种易溶于水,小明用了一种方法将它们分离开来,步骤为:① ,② 。
(3)小明认为若要探究MnO2在较低的温度下对分解H2O2有无催化作用,需作对比实验,他设计了三组实验:①在试管中加入5ml 30%的过氧化氢溶液,把带火星的木条伸入试管,看木条是否复燃。②...;③在第3支试管中加入5ml 30%过氧化氢溶液,并加入少量二氧化锰,把带火星的木条伸入试管,观察木条是否复燃。
你认为小明设计的第2组实验过程应为: 。
(4)小明得到的是③中有O2放出,但他认为③中有O2放出是因为MnO2与H2O2发生了反应,你如何帮他设计实验来说明MnO2没有和H2O2起反应,而只是起了催化作用?
五、我能算(共10分)
27、为了消除碘缺乏病,我国政府规定居民的食用盐必须加碘,简称碘盐。
(1)碘酸钾的化学式为KIO3,则碘酸钾的相对分子质量为 ,碘酸钾
中钾、碘、氧元素的质量比为 。
(2)若1kg碘盐中含30mg碘。已知成年人每天约需要0.15mg碘,假设这些碘主要从碘盐中摄取的,则成人每天需要食用碘盐 g?
(3)多少克碘酸钾中含碘元素20mg?
28、某校902班小东同学从网上收集的某硝酸铵化肥外包装袋标签如图所示,请计算该袋化肥的纯度(即化肥中硝酸铵的质量分数)。
期中考试 参考答案
一、1、B 2、B 3、C 4、B 5、D 6、A 7、C 8、B 9、D 10、B 11、B 12、D 13、B 14、D 15、C 16、B
二、17、(1)0 (2)3N (3)Fe2+ (4)2SO2 18、分子不断运动
19、(1)过氧化氢 水+氧气 (2)铁+氧气 四氧化三铁
H2O2 H2O O2 Fe O2 Fe3O4
20、提示:先读题,观察题中示例,再去回忆后填写。
21、提示:先读题,弄懂“单质化合物”的含义相同点和不同点,再访例回忆找出一对概念来,把这俩的相同点与不同点等写出来。
22、(1)①长颈漏斗②酒精灯③试管;(2)过氧化氢或高锰酸钾;(3)③⑤④或③⑤④②
(4)热膨胀法(塞上带导试管的橡皮塞,将导管放入水槽中,手握试管,观察有无气泡冒民);(5)排水集气瓶;(6)提示:从放入氧气的速率,节约药品,安全方便操作等方面来反思。
三、23、(1)硫,得到,S2-,金属,Na2S;
(2)提示:采用比较观察的方法,从纵向、横向等几方面,化合价,电子个数,2层数等因素去比较,把自己得到的结果写出来即可。
24、SO2或H2与CO2或SO2、H2与CO2;
四、25、答案有多种,因选择的对象和采用的方法而不同:(1)若选择氧气和氢气,其两种方法可以用A试燃法,用带有大量木条去试验,能复燃的那种气体是氧气。B、比较质量法,同体积的氢气比氧气轻许多。
(2)若选择自来水和汽水,其两种方法可以是A检验其是否残存消毒产业的氯教的方法。有则是自来水。B、比较有气泡,接动则有数量气泡的为汽水。
26、(1)KMnO4 K2MnO4+MnO2+O2;试管、铁架、酒精灯。
(2)溶解;过滤;
(3)任第二支试管加入少量二氧化锰,把带火星的木条伸入试管,观察木条是否复燃。
(4)提示:比较反应后的M2O2是否仍具有这样的性质。如果反应的结果必然有M2O2不复存在,反应的残留物不再具有相同的性质。如果仍具有这个性质,则可以说明M2O2在反应中起了催化作用,自己没有变化。
五、27、(1)214;39:127:48;(2)5;(3)667.7g
28、98%,提示:先计算纯净的硝酸铵的含氧量,再将34.3%与它比较,可求得。