2006年中考仿真模拟 (二)
总分:100分 时量:90分钟
可能用到的相对原子质量:Fe-56 H-1 Cu-64 O-16 C-12
Ca-40 Cl-35.5 Na-23
一、选择题:(每小题只有一个正确答案。2′×25共50′)
1.下列过程中没有发生化学变化的是( )
A.海水晒盐 B.铁锅久置出现锈斑 C.铁矿石炼铁 D.食物腐败
2.下列各组物质中,前者属于化合物,后者属于混合物的是( )
A.食盐 干冰 B.冰水共存物 碘酒
C.红磷 纯碱 D.净化后的空气 石灰石
3.实验室制取H2、O2、CO2气体的化学反应中,不包含的反应类型是( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
4.下列符号所表示的粒子中,能保持氯气化学性质的最小粒子是( )
A.Cl2 B.Cl C.Cl- D.ClO3-
5.参加化学反应的物质在反应前后一定变化的是( )
A.原子的种类 B.原子的数目 C.分子的种类 D.分子的数目
6.NO是大气污染物,但少量NO在人体内具有扩张血管,增强记忆功能。NO难溶于水,通常条件下极易与O2反应。则实验室收集NO的方法为( )
A.向下排空气法 B.向上排空气法 C.排水集气法 D.以上方法都可以
7.根据化学常识,判断下列说法正确的是( )
A.用完后的干电池应该回收集中处理 B.加碘食盐中的“碘”通常是指碘单质
C.农药波尔多液可盛放在铁制容器中
D.某雪饼包装中有一小袋干燥剂,其主要成分是CaCO3
8.下列化学方程式正确的是( )
A.2H2 + O2 === 2H2O B.2Fe + 6HCl = 2FeCl3 + 3H2↑
C.KClO3 = KCl + O2↑ D.H2SO4 + 2KOH = K2SO4 + 2H2O
 9.测定生活中一些物质的pH,结果如下图,参照该图判断,下列说法正确的是( )
9.测定生活中一些物质的pH,结果如下图,参照该图判断,下列说法正确的是( )
A.牙膏是中性物质 B.草木灰可改良碱性土壤
C.胃酸过多的人不宜多吃橘子 D.食醋能使无色酚酞变红
10.往5.6g混有少量铜粉的铁粉中加入足量稀硫酸,产生氢气的质量( )
A.大于0.2g B.等于0.2g C.小于0.2g D.无法确定
11.下列说法正确的是( )
A.物质的溶解度都随温度的升高而增大
B.浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液
C.任何物质的饱和溶液都比它的不饱和溶液
D.某温度下,在硝酸钾的饱和溶液中加入氯化钠,若温度不变,氯化钠不溶解
12.检验一瓶长期露置在空气中的氢氧化钠溶液是否变质,下列不能作为检验用的试剂是( )
A.澄清石灰水 B.氢氧化钡溶液 C.氯化钙溶液 D.酚酞试液
13.下列事实能证明在化学反应中分子可分的是( )
A.冷却硝酸钾的热饱和溶液有硝酸钾晶体析出 B.水蒸气冷凝成水
C.水通电可以得到氢气和氧气 D.碘升华
14.2003年3月,美英联军在伊拉克遭遇沙尘暴。沙尘暴已成为世界环境问题中的一个重点问题,下列措施可以防止沙尘暴的是( )
A.植树造林,加强绿化 B.合理使用化肥和农药
C.工业“三废”经处理后再排放 D.矿物产品的综合开发和利用
15.生活中处处充满化学,下列生活中的化学知识叙述正确的是( )
A.铁制品在干燥的空气中易生锈 B.用纯碱溶液除水壶中的水垢
C.硫酸铜可用于游泳池水消毒,亦可用于自来水消毒
D.通常用含单质碳的墨水书写档案,以便于保存
16.用氢气还原8g氧化铜,将反应后的气体全部通入足量的浓硫酸中,浓硫酸的质量增加了0.9g,则剩余的固体是( )
A.CuO和Cu B.CuO C.Cu D.无法确定
17.关于下列物质的转化过程:H2→H2O,CO→CO2,C→CO2,说法不正确的是( )
A.都能通过化合反应实现 B.都能通过置换反应实现
C.都能通过和单质反应实现 D.变化前后都有元素化合价改变
18.对下列物质在氧气中燃烧的实验现象描述正确的是( )
A.石蜡在氧气中燃烧时,有水和二氧化碳生成
B.硫粉在氧气中燃烧时,火焰呈蓝紫色,生成无气味的气体
C.氢气在氧气中燃烧时,火焰呈黄色,放出大量的热
D.铁丝在氧气中燃烧时,火星四射,有黑色固体生成
19.以下说法违背科学事实的是( )
A.医疗上常用体积分数为70﹪~75﹪的酒精溶液作消毒剂
B.煤、石油、天然气是当今世界上最主要的三大化石燃料,它们都是化合物
C.晒盐时,日晒、风吹都有利于氯化钠晶体的析出
D.点燃不纯的氢气可能会发生爆炸
20.在盛有AgNO3和Mg(NO3)2混合溶液的试管中,加入一定量的锌粉充分反应,试管底部有少量固体存在。过滤,向滤液中加稀盐酸,产生白色沉淀。滤渣是( )
A.Mg B.Ag C.Zn 和Ag D.Zn 和Mg
21.火柴划着后,如果将火柴直立,使火焰在上,火柴就不易继续燃烧,其原因是( )
A.氧气不足 B.温度没达到着火点
C.火柴的着火点升高 D.空气不足
 22.右图是a、b两种固体物质的溶解度曲线,下列说法中错误的是( )
22.右图是a、b两种固体物质的溶解度曲线,下列说法中错误的是( )
A.a的溶解度大于b的溶解度
B.在t℃时,a、b的溶解度相同
C.当a中含有少量b时,可以用结晶法提纯a
D.a、b都属易溶物质
23.要除去CaCl2溶液中混有的少量HCl,加入过量下列物质,其中最合理的是( )
A.CaCO3 B.Ca(OH)2 C.CaO D.AgNO3
24.下列说法错误的是( )
A.一定温度下,NaCl的饱和溶液比它的不饱和溶液要浓
B.铜和氯化银反应生成银和氯化铜
C.酸跟碱作用而生成盐和水的反应叫中和反应
D.浓硫酸不慎沾在皮肤上,先用抹布擦拭,再用大量水冲洗
25.下列各组内物质在溶液中能大量共存的是( )
A.NaCl、AgNO3、K2SO4 B.KOH、NaNO3、H2SO4
C.Ba(OH)2、NH4Cl、CuSO4 D.KNO3、MgCl2、ZnSO4
二、填空题:(书写化学方程式每个2分,其余每空1分,共20分)
26.写出下列化学符号或符号的意义:
(1)两个铁原子 ;(2)甲烷分子 ;(3)5H2O 。
27.用化学式填空:在稀硫酸、食盐、熟石灰、干冰四种物质中,生活中常用作调味剂的是__________;可用于人工降雨的是_________;可用于清洗钢铁表面铁锈的是_________;能用来改良酸性土壤的是___________。
28.“非典”肆虐时期,过氧乙酸(CH3COOOH)是被人们广泛使用的消毒剂,它无色且有辛辣味,具有强氧化性,温度稍高即分解放出氧气并生成乙酸。过氧乙酸中碳、氢、氧三种元素的质量比为_________;写出过氧乙酸分解的化学方程式____________________。
29.水是人类宝贵的自然资源。电解水属于________(填“物理”或“化学”)变化;如水中混有泥沙,可采用__________(填“过滤”或“结晶”)的方法除去泥沙。
30.将物质进行科学地分类给我们学习化学带来了很大的方便。利用你具备的知识将下列物质用两种方法进行简单分类,写出所分物质的类别及对应的物质:
H2O CuO CH4 HNO3 Ca(OH)2 ZnSO4 CH3COOH
方法一:___________________________________________________________________
方法二:___________________________________________________________________
31.已知6g A物质和若干克B物质恰好完全反应生成13g C物质和9g D物质,则参加反应的B物质是_________g,若12g A物质参加反应,则生成D物质________g。
32.家庭饮用的纯净水,经测定其pH略小于7,说明略显________性。这是因为其中溶有______________的缘故。
33.用Zn、Zn(OH)2、ZnCO3、CuCl2溶液、盐酸五种物质两两反应制备,发生的反应共有___________个,其中有___________个属于置换反应。
 三、简答题:(4′×3共12分)
三、简答题:(4′×3共12分)
34.四支试管中分别盛有相同质量分数的稀盐酸,将甲、乙、丙、丁四种金属分别同时放入其中。小明将观察到的现象形象地画了一幅卡通画,每个卡通人物表示一种金属,周围的小黑点表示反应中生成的气体。
(1)上述四种金属可以分为两类,其中哪几种金属可以归为一类?
(2)若乙是金属Zn,则丙可能是什么金属?请你说出理由。
35.根据酸的通性和碱的通性,请你总结盐的通性(大多数盐具有的性质)。
36.已知:A、B、C、D、E、F六种物质之间存在如下关系:
①A + B → C + H2O ②C + KOH → D↓(蓝色)+ E
③B + D → C + H2O ④E + BaCl2 → F↓(白色,不溶于稀硝酸)+ KCl
⑴试确定A、B、E的化学式:A:___________ B:___________ E:___________
⑵写出②的化学方程式:_________________________________________________
四、实验题:(每空1分,共12分)
37.现有下图所示仪器和装置(集气瓶口方向不变)试回答下列问题:(南京市中考试题)
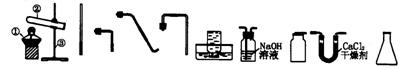
A B C D E F G H I J
(1)写出A中两种仪器的名称:①__________ ②__________ ③__________
(2)用氯酸钾与二氧化锰混合加热制取氧气的化学方程式为____________________
(3)用石灰石与稀盐酸制备并收集二氧化碳,应选用的仪器和装置的编号为__________
(4)实验室用无水醋酸钠和碱石灰的固体混合物加热制取甲烷。甲烷的密度比空气小,难溶于水。制备并收集甲烷所需仪器和装置的编号为____________________
 (5)用锌与盐酸反应制取纯将干燥的氢气并还原氧化铜,按气体产生、流经仪器和装置的先后顺序,填写仪器和装置的编号____________________
(5)用锌与盐酸反应制取纯将干燥的氢气并还原氧化铜,按气体产生、流经仪器和装置的先后顺序,填写仪器和装置的编号____________________
38.根据右图装置回答:(福州市中考试题)
(1)实验室可用该装置制取干燥的 _____气体,所用的药品是___________________。若在上述实验中气体无法收集满,请说出可能的一种原因:____________________________________。
(2)若只改变收集方法,还可以制取干燥的__________气体。固体和液体 浓硫酸(干燥剂)
(3)把发生装置改装后,可用来制取干燥的氧气,但必须添加的一种仪器是 。
五、计算题:(6分)
39.称取氯化钠和氯化钙的固体混合物14g,放入烧杯中,加入96g碳酸钠溶液恰好完全反应(反应的方程式为:Na2CO3
+CaCl2![]() CaCO3↓+2NaCl)。待反应完全后过滤,称得滤液的总质量为100g。
CaCO3↓+2NaCl)。待反应完全后过滤,称得滤液的总质量为100g。
(1)根据质量守恒定律,可知生成的沉淀质量为____________________。
(2)固体混合物中氯化钙的质量是多少?
(3)所得虑液中溶质的质量分数是多少?
![]() 综合与创新 中考仿真模拟(二)
综合与创新 中考仿真模拟(二)
一、选择题:(每小题只有一个正确答案。2′×25共50′)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 答案 | A | B | A | A | C | C | A | D | C | C | B | D | C |
| 题号 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| 答案 | A | D | A | B | D | B | B | B | A | A | B | D |
二、填空题:(书写化学方程式每个2分,其余每空1分,共20分)
26.(1)2Fe(2)CH4(3)5个水分子
27.NaCl;CO2;H2SO4;Ca(OH)2
28.6︰1︰12 2CH3COOOH = 2CH3COOH + O2↑
29.化学 过滤
30.方法一:有机化合物:CH4 CH3COOH 无机化合物:H2O CuO HNO3 Ca(OH)2 ZnSO4
方法二:含氧化合物:CH3COOH H2O CuO HNO3 Ca(OH)2 ZnSO4 无氧化合物:CH4
31.16g;18g
32.酸 二氧化碳
33.4 ;2
三、简答题:(4′×3共12分)
34.(1)甲、乙、丙可以归为一类。(2)丙可能是Fe(或Sn、Pb)。其理由是丙能和盐酸反应,但反应的剧烈程度比乙(Zn)小,在金属活动顺序表中位于Zn和H之间。
35.盐溶液与金属的置换反应、盐与盐溶液的反应、盐与酸的反应、盐与碱溶液的反应
36.A.CuO B.H2SO4 C.K2SO4 ②CuSO4 + 2KOH = Cu(OH)2 ↓ + K2SO4
 四、实验题:(每空1分,共12分)
四、实验题:(每空1分,共12分)
37.(1)①酒精灯 ②试管 ③铁架台 (2)2KClO3 ===== 2KCl+3O2↑ (3)JEH (4)ADF (5)JCGIBA(顺序错误不给分)
38.(1)二氧化碳(或CO2) 石灰石(或大理石)、稀盐酸 反应物的量不足
(2)氢气(或H2) (3)酒精灯
五、计算题:(6分)
39.解:(1)10g
(2)设固体混合物含氯化钙的质量为x,反应后生成氯化钠的质量为y
Na2CO3+CaCl2![]() CaCO3↓+2NaCl
CaCO3↓+2NaCl
111 100 117
x 10g y
x=![]() =11.1g
=11.1g
y=![]() =11.7g
=11.7g
原混合物中含氯化钠的质量=14g-11.1g=2.9g
(3)所得滤液的溶质的质量分数=![]() ×100%=14.6%
×100%=14.6%
答:略