化学模拟试题(四)
班级____座号____姓名________成绩____
有关的原子量:O:16 Fe:56 C:12 Zn:65 Mg:24 Al:27 Cu:64 S:32
H:1 N:14 Ca:40 Cl:35.5
一、填空题:
1、用数字和化学符号表示:
(1)二个氧化铁分子___;(2)三个硫酸根离子___;(3)四个硝酸铝分子___;(4)二个钙离子___;(5)五个氮原子___。
2、海洛因是我国政府明令严禁的毒品,其化学式为C21H33NO5,计算其碳元素、氢元素、氮元素、氧元素的质量之比_______,氧元素的质量分数为______。
3、现有A、B、C、D、E五个集气瓶,分别盛有氢气、氧气、一氧化碳、二氧化碳和甲烷。试根据所叙述的性质,判断五个集气瓶中各盛有哪种气体,并填写下列各空格。
(1)气体A燃烧后只生成一种能使石灰水变浑浊的气体,A的化学式为____,燃烧的化学方程式为____________。A在高温下能还原铁矿石里的氧化铁,此反应化学方程式为___。
(2)气体B燃烧后生成水和二氧化碳,该气体是____,它是一种最简单的____物,根据B能燃烧的性质,它可以用作____。
(3)气体C是相同条件下最轻的气体,C的化学式为___,点燃C前,一定要______。气体C在空气中燃烧,火焰呈____色,气体C与氧化铜反应的化学方程式为__________,反应中C是____剂。
(4)气体D是人和动物片刻不能离开的气体,D的化学式为____。细铁丝在D中燃烧时除放出热量,生成黑色固体外,还能看到的现象是_______。在实验室里可用氯酸钾和二氧化锰混合加热制取D,反应的化学方程式为__________。
(5)气体E的水溶液能使紫色石蕊试液变红,E的化学式为____它与水反应的化学方程式为________。实验室制取E所用的药品是_____和____。
(6)上述五种气体中,有剧毒的气体是____,通常情况下能灭火的气体是_____。
4、在ax3y4+8z=bz2y3+cx中,a、b、c的值分别是___ ___ ___。
5、在化学反应:2A+3B=2C+D中,5克A和7克B恰好完全反应,
若生成C的质量是D的3倍,则生成D的质量为____克。
6、取8克某有机物在氧气中完全燃烧,生成11克二氧化碳和9克水,该
化合物中一定含____元素,各元素质量比为________。
7、氯酸钾和二氧化锰的混合物3.4克,加热完全分解后,冷却,称得残
留固体为2.6克,根据质量守恒定律可知产生氧气的质量为____
克,若从固体残留物中提纯可得二氧化锰,应经过____和___
等主要操作。
8、t℃时,将202克硝酸钾溶液蒸发掉20克水,冷却至t℃时,析出2
克硝酸钾,再蒸发掉20克水,冷却至t℃时,又析出4克硝酸钾,则
原硝酸钾溶液中含硝酸钾____克。
9、发射通讯卫星的火箭用联氨(化学式为N2H4)作燃料,用N2O4作氧
化剂,燃烧后生成氮气和水。写出联氨和N2O4反应的化学方程式:
_______________。
10、在①水 ②硫酸铜溶液 ③铁 ④高锰酸钾 ⑤稀硫酸 ⑥硫 ⑦氧气
其中属于混合物的是____,属于化合物的是____,属于单质的有____,属于氧化物的有____(以上均用题号表示)。
从以上各物质中选择适当物质写出符合下列要求的化学方程式:
(1)通电时产生两种气体_____________;
(2)实验室制取氧气_______________;
(3)现代湿法冶炼金属______________;
(4)燃烧时有刺激性气体的是___________。
二、实验题:
1、为了制取CO2进行有关实验,采用下列实验装置,请回答以下问题:
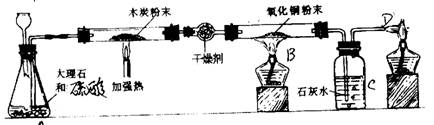
(1)作为CO2的发生器的装置A中有___处错误,经改正后该装置
中发生的反应的化学方程式为_______________。
(2)使用改正后的A装置来制取气体应具备的条件①_______
②________。
(3)装置B中发生的化学方程式为__________。
(4)通过装置C的作用,可以除去尾气中的_____。
(5)D处反应的化学方程式为__________。
(6)装置A还可以用于实验室制取____气体。
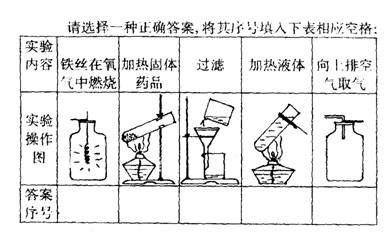
2、下列实验操作图中各有一处错误需要改正,改正时可供选择的答案如
下:
A、试管口略向下倾斜;B、导管口应接近集气瓶口;C、集气瓶底部
应放有少量水或一层细砂;D、液体体积不超过试管容积的1/2;E、
导管口应接近集气瓶底部;F、液体应沿着玻璃棒流入过滤器;G、
液体体积应不超过试管容积的1/3。
三、计算题:
1、在一定温度时,50克的硝酸钾饱和溶液蒸干,可得到12克硝酸钾,
计算:(1)这一温度下硝酸钾的溶解度。
(2)该温度下,硝酸钾饱和溶液中溶质的质量分数。
(3)配制该温度下饱和硝酸钾溶液1000克,需硝酸钾和水各多
少克?
2、80克含碳酸钙杂质的氯化钙样品,与124.4克盐酸恰好完全反应,反
应结束后所得溶液的质量为200克。求(计算时精确到0.01,氯化钙
与盐酸不反应)。
(1)生成二氧化碳的质量为____克,它在标准状况下所占的体积约
为____升。(标准状况下CO2的密度为1.977克/升)
(2)该样品中杂质碳酸钙的质量分数为多少?反应后所得溶液中溶质
的质量分数为多少?
四、选择题:
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 答案 | |||||||||||||
| 题号 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| 答案 |
四、选择题:(每题只有一个正确答案,请将答案填在表格上)
1、下列变化:①铜在潮湿的空气里生成铜绿,②石蜡熔化,③“干冰”
气化,④木材变成木炭,其中属于化学变化的是( )
A、①④ B、②③ C、③④ D、④
2、下列各组物质中,前一种是化合物,后一种是混合物的是( )
A、干冰和白磷 B、盐水和含铁质量分数为70%的氧化铁
C、澄清的石灰水和石灰石 D、氧化钙和天然气
3、从改善人类的生存环境来看,最理想的新型燃料是( )
A、一氧化碳 B、氢气 C、焦炭 D、液化石油气
4、下列操作中,正确的是( )
A、用燃着的酒精灯引燃另一酒精灯
B、用量筒量取液体时,视线要跟量筒内液面的最高处保持水平
C、试管、燃烧匙、蒸发皿都可以直接在酒精灯的火焰上加热
D、称量物放在托盘天平的右盘
5、下列说法错误的是( )
A、空气是多种分子构成的混合物 B、空气是多种元素的混合物
C、原子量不是原子的质量
D、分子是保持物质的化学性质的一种微粒
6、下列物质的用途中,与该物质的化学性质无关的( )
A、用氧气炼钢 B、墨鱼骨粉(主要成分是CaCO3)用于治胃酸过多
C、氢气作填充探空气球的原料 D、用氧炔焰切割金属
7、由碳和氧两种元素组成的气体,碳与氧两种元素的质量比为2∶3,该
气体的组成( )
A、属于混合物 B、属于纯净物 C、属于单质 D、无法确定
8、限用碳、一氧化碳、氧化铜、碳酸钙、盐酸五种物质,进行单一或两
两反应,可以写出生成物中有二氧化碳的化学方程式共有( )
A、2个 B、3个 C、4个 D、5个
9、下列说法错误的是( )
A、镁条在空气中燃烧后,生成物的质量比原来的质量增大了
B、3克碳和10克氧气反应,可生成13克二氧化碳
C、氯酸钾受热分解后,剩余固体的质量比原来反应物的质量轻
D、化学反应前后各物质的质量总和必须相等
10、根据四种微粒结构示意图判断,下列说法错误的是( )
+11 2 8 +9 2 8 +8 2 8 +13 2 8
A、它们都是带电微粒 B、它们都已达到稳定结构
C、它们都是稀有气体元素的原子结构
D、它们的电子层结构都相同
11、在下列各反应中,反应前后各元素的化合价都不发生变化的是( )
A、2H2O![]() 2H2↑+O2↑
B、C+O2
2H2↑+O2↑
B、C+O2![]() CO2
CO2
C、Zn+2HCl=ZnCl2+H2↑ D、Cu(OH)2+H2SO4=CuSO4+2H2O
12、市场上发现的假酒使人眼睛变瞎主要因为其中含有( )
A、水 B、甲醇 C、酒精 D、乙酸
13、在托盘天平两边各放一只等质量的烧杯,往烧杯中各注入足量的稀硫
酸,并使天平处于平衡状态,在左边的烧杯中加入2.4克锌,在右边
的烧杯中加入2.4克镁,待两边的金属都完全反应后天平指针的位置
( )
A、向左偏转 B、向右偏转 C、没有偏转 D、无法判断
14、元素X的最外层有3个电子,元素Y的最外层上有7个电子,这两
种元素形成的化合物的化学式可能是( )
A、xy B、x3y C、xy3 D、x2y
15、在20℃时,把质量分数为20%的某物质的水溶液,蒸发掉溶剂10
克,再冷却到20℃,有2克晶体析出。此时,溶液中溶质的质量分数
为25%,则该物质20℃时的溶解度为( )
A、20克 B、25克 C、33.3克 D、50克
16、要使A克a%的食盐溶液中溶质的质量分数增大一倍,可采用的方法
是( )
A、加入一倍的食盐 B、把溶剂蒸发掉一半
C、把溶剂蒸发掉A/2克 D、把溶液去掉A/2克
17、进行粗盐提纯的实验中,一定要用到的一组仪器的是( )
①试管 ②烧杯 ③漏斗 ④蒸发皿 ⑤玻璃棒 ⑥烧杯 ⑦酒精灯
⑧长颈漏斗
A、②③④⑤⑦ B、①③④⑥⑦ C、②④⑤⑦⑧ D、①③④⑤⑦
18、在20℃时,食盐的溶解度为36克,在该温度下,不可能得到的溶液
中溶质的质量分数的是( )
A、15% B、20% C、25% D、30%
19、有关溶液的说法,不正确的是( )
A、溶液都是无色的 B、一瓶溶液的各部分性质都相同
C、饱和溶液不一定是浓溶液 D、溶液是均一,稳定的混合物
20、20℃时,将18.6克硝酸钠放入50克水中,充分搅拌全部溶解,
20℃时硝酸钠的溶解度为( )
A、37.2克 B、18.6克 C、9.3克 D、无法计算
21、将铁片分别放入下列溶液中充分反应,反应后溶液的质量(不包括固
体)比反应前溶液的质量减轻的是( )
A、硫酸铜 B、硫酸 C、硫酸亚铁 D、稀盐酸
22、取56克不纯的铁粉与足量的稀硫酸反应,生成2克氢气,下列情况
可能是( )
A、铁中含有碳和锌 B、铁中含有碳
C、铁中含有碳和铝 D、铁表面有铁锈
23、配制溶质的质量分数一定的溶液,正确的操作步骤是( )
A、称量(或量取)、计算、溶解 B、计算、称量(或量取)、溶解
C、溶解、称量(或量取)、计算 D、称量(或量取)、溶解、计算
24、下列关于铁的说法中正确的是( )
A、铁是地壳中含量最多的金属元素 B、铁在氧气中燃烧生成氧化铁
C、生铁属于金属单质 D、生铁的含碳量比钢的含碳量高
25、在反应X+3O2![]() 2CO2+2H2O中,根据质量守恒定律,可判断X的
2CO2+2H2O中,根据质量守恒定律,可判断X的
化学式为( )
A、CH3OH B、CH3COOH C、C2H2 D、C2H4
