中考化学模拟试卷(1)
一、择题(本大题包括15小题,其中第1—10小题每小题1分,第11—15小题每小题2分,共20分。每小题只有一个选项符合题意,请将正确选项的序号填入下表相应空格内。)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| 答案 |
1. 在互联网上搜索“中央电视台每周质量报告”时,可搜索到被曝光的事件中一定涉及到化学变化的是
A、 用淀粉、蔗糖、奶香精等掺和成“假奶粉” B、用工业石蜡等给瓜子“美容”
B、 用硫磺燃烧法熏蒸粉丝 D、用毛发水、酱色、水、盐等兑制成“假酱油”
2.“绿色化学”是当今社会提出的一个新概念。在“绿色化学工艺”中,理想状态是反应中原子全部转化为欲制得的产物,即原子的利用率为100%。在用C3H4(丙炔)合成C5H802(2-甲基丙烯酸甲酯)的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要的其它反应物是
A. CH3OH和H2 B.C02和H2O C.CO和C2H5OH D.CO和CH3OH
3.2004年5月央视《每周质量日报》报道,市场上发现假冒的2B铅笔。下列说法错误的是
A.铅笔芯中含有石墨 B.铅笔芯是用铅做的
C.2B铅笔芯可以导电 D.铅笔芯在氧气中灼烧能生成C02
4.毒品严重危害人类社会。冰毒的化学式为C10H15N,有关冰毒的叙述正确的是
A.不完全燃烧时会生成CO B.完全燃烧时的生成物只有两种
C.C、H、N三种元素中质量分数最高的是H元素 D.C、H、N元素的质量比为10:15:1
5.下列生活中的常见材料,属于有机合成高分子材料的是
A.钢筋混凝土 B.陶瓷 C.塑料 D.钢铁
6.下图所示的实验操作正确的是

7.下列生活经验和知识原理的叙述中,不正确的是
A.铝合金比铁制品耐腐蚀的原理是:铁的化学性质比铝活泼
B.用汽油洗涤衣服上的油渍的原理是:油渍易溶于汽油
C.用含Al(OH)3的药物治疗胃酸过多的原理是:胃酸会和Al(OH)3发生中和反应
D.食醋除水垢的原理:食醋中的醋酸和水垢中的物质发生化学反应,生成可溶于水的物质
8. 鱼胆弄破后,会使鱼肉粘上一种难溶于水的胆汁(一种酸),使鱼肉变苦,要消除这种苦味,可用下列何种溶液冲洗最适宜
A、食盐水 B、醋酸 C、纯碱不溶液 D、NaOH溶液
9.分别用以下三组物质比较锌和铜的金属活动性:(1)Zn、Cu、稀硫酸;(2)Zn、Cu、MgSO4溶液;(3)Zn、Cu、AgNO3溶液。仅用组内物质就能够直接达到目的的是
A. 仅有(1) B. (2)(3) C. (1)(3) D.(1)(2)(3)
10.下列四个图像反映的变化趋势,分别对应四种操作过程,其中正确的是
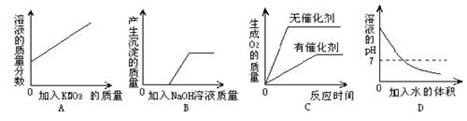
A.某温度下,向一定量接近饱和的硝酸钾溶液中不断加入硝酸钾晶体
B. 向氯化铁和盐酸的混合溶液中加入过量的氢氧化钠溶液
C.用相等质量的双氧水来制取氧气
D.氢氧化钠溶液中加足量的水稀释
11.以下叙述正确的是
A.由不同种元素组成的物质一定是化合物 B.含有氧元素的化合物是氧化物
C.物质可以由分子、原子或离子构成
D.由于反应前后原子种类相同,所以化学反应遵循质量守恒定律
12. 化学知识中有很多的“相等”,下列说法中不正确的是
A、 参加化学反应的物质的总质量等于反应后生成的物质
B、 化合物中元素化合价的正价总数与负价总数的数值相等
C、 溶液稀释前后深质的质量相等
D、在原子中原子核内的质子数等于中子数
13.对容器口进行磨砂处理可提高容器的密封性。下列仪器中容器口没有进行磨砂处理是
14. 下列各组混合物中,用一种试剂不能将括号内的杂质除去的是
A.CuSO4 (Na2SO4) B.C (CuO) C.CO2 (CO) D.NaCl (MgCl2)
15. 对下列实验过程的评价,正确的是
A.某溶液滴加BaCl2溶液,生成不溶于稀硝酸的白色沉淀,该溶液中不一定含有SO42-
B.某无色溶液中滴入酚酞试液变红色,该溶液不一定是碱溶液
C.检验氢气纯度时,将一收集气体的试管移近火焰,没有响声,表明氢气纯净
D.验证烧碱溶液中是否含有Cl-,先加稀盐酸除去OH- ,再加AgNO3溶液有白色沉淀出现,证明含Cl-
二、填空题(本大题包括5小题,每空1分,共19分)
16. (4分)自来水消毒过程中通常会发生化学反应,其反应的微观过程可用下图表示:
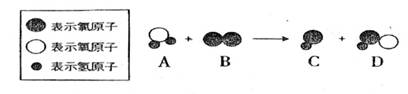
(1)请写出该反应的化学方程式 。
(2)A物质属于 (填物质分类)。
(3)D物质中氯元素的化合价为 。
(4)分析以上微观过程模拟图,你能总结出的一条结结论是 。
17. (4分)明矾[化学式为KAl(SO4)2·12H2O]是农村常用的一种净水剂,它在水中离解出K+、Al3+和SO42- ,甲同学炎了探究明矾中每粒子是否有净水作用,进行了如下实验,请填写表中空白:
| 实验操作 | 实验现象 | 结论 |
| 在一杯浑浊的水中加入少量KCl,静置 | 烧杯中的水仍然浑浊 | |
| 在一杯浑浊的水中加入少量Al2(SO4)3,静置 | 烧杯中的水变澄清 |
乙同学看到甲方的方案后,认为该方案不完善,他对甲同学的方案进行补充完善,请你把乙同不这的补充方案中要达到的目的和所使用的试剂填入下表。
| 实验目的 | 使用的试剂 |
 18. (3分)海洋是巨大的资宝库,从海洋中可
18. (3分)海洋是巨大的资宝库,从海洋中可
提取许多重要物质。请你参与下列问题的讨论:
(1)我市某盐场测得:①海水中含NaCl约为3.5%;②在海边打深井,井水中NaCl约为8%。晒盐最好选择 (填序号)作原料,晒盐的原理是 。
(2)晒盐后得到的母液(又称卤水)中含有氯化镁(MgCl2)、硫酸镁(MgSO4)和氯化钾(KCL)等物质。参照右图各物质的溶解度曲线,将卤水加热到60℃以上蒸发水分就会逐渐析出 (填名称),理由是 。
19.(4分)已知有化合物甲、乙和单质丙、丁四种物质发生如下反应:甲+丙→乙+丁
(1)该反应所属反应类型是 反应。
(2)若乙的溶液为浅绿色,丁为无色气体,则丙是 (用化学式回答,下同)
(3)在常温下甲是固体,若乙为无色液体,则丙是 ;若乙为无色气体,则丙是
三、实验题(本大题包括3小题,每空1分,共16分)
20. (12分)化学是造福人类的科学,在人体保健、医疗卫生等方面作出了重大贡献。请你用所学的化学知识解答有关问题。
(1)食品安全与健康密切相关。下列做法不会危及人体健康的是( )
A. 用“苏丹红一号”作食品添加剂 B .蒸馒头时加入适量纯碱
C.加过量亚硝酸钠以保持肉质鲜美, D.把霉大米淘净后继续食用
(2)低血糖患者每天都应注意摄入一定量含淀粉的食物,以使血液中维持一定浓度的葡萄糖。请你列举两种富含淀粉的食物 、 。
(3)油炸食物不宜多吃,因长时间煎炸会产生有毒物质丙烯醛(C3H4O),丙烯醛在空气中完全燃烧时,生成二氧化碳和水。请写出丙烯醛完全燃烧的化学方程式 。
(4)食盐是人维持正常生理活动的重要物质。人体细胞中约含NaCl 0.9%,一般成年人每日需NaCl的量为4.5 g~9 g。
①某病人因食盐摄入量不足,需要补充溶质质量分数约为0.9%的生理盐水,现医生确定每天为他注射200 g生理盐水,则每天可为他补充约 g食盐。
②小明同学根据NaCl+AgNO3=AgCl↓(白)+NaNO3这一反应原理,对一瓶生理盐水进行分析时,不知道加入的硝酸银溶液与氯化钠溶液是否恰好完全反应,于是他设计了一个实验方案进行探究。请你帮他完善该实验方案。
| 探究步骤 | 可能观察到的现象 | 结论 |
| (1)取反应后的上层清液于试管中,滴加 溶液 | 若有白色沉淀生成 | 溶液过量 |
| 若无白色沉淀生成 | 还需进行下一步探究 | |
| (2) 另取反应后的上层清液于试管中,滴加 溶液 | ||
|
【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【猜想】①可能有一种气体和另一种物质生成 ②反应过程中可能有热量放出
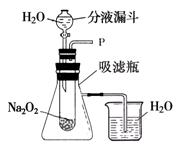 【实验装置】如右图所示
【实验装置】如右图所示
【实验探究】实验一:探究反应后生成的气体是什么?
(1)打开右图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃。说明生成的气体是 。
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:
实验二:继续探究反应后生成的另一种物质是什么?
(1)小张猜想另一种物质是Na2CO3,小蔡认为不可能。小蔡的依据是 。
(2)小蔡取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色。说明反应后所得的溶液呈 性。
【表达】由实验探究的结果,写出过氧化钠和水反应的化学方程式 。
七、计算题(本题共5分) 可能用到相对原子质量:Ca-40,Cl-35.5,C-12,O-16,H-1
22.(7分)小洁同学为测定测定钙片中碳酸钙的含量标注是否属实,她取出4片片剂,研碎后放入烧杯中,逐滴加入稀盐酸,至不再放出气体为止,共用去稀盐酸40.0 g,称量烧杯中剩余物质量为47.8 g(不含烧杯质量, 假定钙片其它成分不与盐酸反应。)求: (1) 生成二氧化碳的质量。(2) 稀盐酸中溶质的质量分数。(3) 通过计算判断钙片中碳酸钙的含量标注是否属实。
参考答案
一、选择题
1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15.
二、填空题
16、(1)H2O+Cl2=HCl+HClO
(2)氧化物(或化合物或纯净物)
(3)+1
(4)在化学反应前后,原子的种类、数目均不改变;或化学反应前后,元素的种不变;或在化学反应前后,分子的种类发生改变(其他合理答案均可)。
17、K+和Cl-都没有净水作用 Al3+或SO42-有净水作用
Al3+是否有净水作用 AlCl3
SO42-是否有净水作用 K2SO4
18、(1)② 井水中的水晒后被蒸发,NaCl结晶析出
(2)MgSO4 因为MgSO4在60℃以上随着温度的升高,溶解度降低
19.(1)置换 (2)Fe (3)H2 C
四、填空题
20. 1)B (2)面食,土豆(马铃薯)红薯等。(3)2C3H4O+7O2==6CO2+4H2O
(4)①1.8 ②(1)氯化钠溶液,硝酸银溶液 (2) 硝酸银溶液,有白色沉淀生成,氯化钠溶液过量
21. 实验一:
(1)氧气(或02 )
(2)过氧化钠与水反应放出热量,使吸滤瓶中的空气受热膨胀,因此伸入烧杯中的导管口看到有气泡产生。
实验二:
(1)根据质量守恒定律,反应物中没有碳元素,所以生成物中不可能有Na2CO3
(2)碱 2Na202 + 2H2O == 4NaOH + 02↑
三、计算题
22. 解:⑴ 根据质量守恒定律可知,生成C02的质量为:
40 g+4×2.5 g-47.8 g=2.2 g
⑵ 设参加反应的CaCO3和HCl的质量分别为x、y
CaCO3 + 2HCl === CaCl2 + H2O + C02↑
100 73 44
x y 2.2 g
73:44=y:2.2 g 解得:y = 3.65 g
则稀盐酸中溶质的质量分数为:(3.65 g/40 g)×100% =9.13%
⑶ 100:44=x:2.2 g 解得:x = 5 g
每片含CaCO3的质量为:5 g/4 =1.25 g>1.24 g,故钙片中碳酸钙的含量标注准确。
答:(略)
