山西省2005年初中毕业生学业考试
化学(非课程改革实验区)
总分80分
一、选择题(每小题只有一个选项符合题意,请将其字母标号填在括号内。每小题1分,共20分)
1. 以下做法不会对环境造成影响的是( )
A. 大量使用含磷洗衣粉洗衣
B. 大量使用农药、化肥
C. 随意丢弃塑料食品袋
D. 集中回收废旧电池
2. 下列变化中,前者是物理变化,后者是化学变化的是( )
A. 牛奶变酸,蜡烛燃烧
B. 瓷器破碎,水分蒸发
C. 干冰致冷,银器变黑
D. 矿石冶炼,空气液化
3. 图中○和●分别表示氢原子和氧原子,其中的粒子可用4H表示的是( )
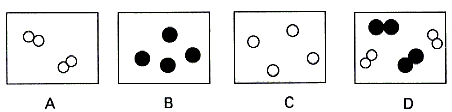
4. 关于氧气和铁的构成,下列说法正确的是( )
A. 由氧元素、铁元素构成 B. 由氧分子、铁原子构成
C. 由氧原子、铁原子构成 D. 由氧分子、铁分子构成
5. 下列属于氧化物的是( )
A. ![]() B.
B.
![]() C.
NaOH D.
C.
NaOH D.
![]()
6. 以下混合物中所含各组分,全部是化合物的是( )
A. 空气 B. 碘酒 C. 工业酒精 D. 爆鸣气
7. 某溶液可使酚酞试液变红色,则该溶液会使石蕊试液( )
A. 变红 B. 变紫 C. 变蓝 D. 不变色
8. 某护发素的pH值小于7,其水溶液显( )
A. 酸性 B. 碱性 C. 中性 D. 无法确定
9. 既利用了物质的化学性质,又利用了物质的物理性质的是( )
A. 用氢气充气球 B. 用二氧化碳灭火
C. 用食醋除去水垢 D. 用金刚石切割大理石
10. 关于一氧化碳、二氧化碳的说法正确的是( )
A. 都能与水反应 B. 都是大气污染物
C. 只有一氧化碳具有还原性 D. 都易分解为碳和氧气
11. 配制一定质量分数的溶液,肯定用到的仪器是( )
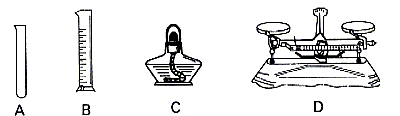
12. 下列实验的操作过程,符合操作规范的是( )
A. 将水沿着玻璃棒缓缓注入浓硫酸中
B. 转动或上下移动试管刷刷洗试管
C. 将滴管下端插入烧碱溶液后再捏瘪橡胶乳头
D. 将块状固体药品直接放入垂直放置的试管内
13. 安全生活离不开化学,下列做法正确的是( )
A. 厨房煤气泄露,迅速开启排风扇
B. 室内起火,立即敞开门窗
C. 煤矿井下停电,赶快引燃火把照明
D. 进入久未开启的菜窑,先要做灯火试验
14. 某金属R与硝酸银溶液反应的化学方程式为![]() ,R与硝酸铜溶液不反应,关于R的推断正确的是( )
,R与硝酸铜溶液不反应,关于R的推断正确的是( )
A. R能置换出酸中的氢
B. R的活动性介于铜、银之间
C. R的活动性比铜强,比银弱
D. R的活动性比铜、银都弱
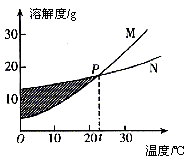
15. 下图表示M、N两种固体物质的溶解度曲线,有关图示信息的描述正确的是( )
A. 20℃时,M的溶解度大于N的溶解度
B. M、N都不是易溶性物质
C. P点表示M、N的溶解度相等
D. 阴影处M、N均为饱和溶液
16. 下列化学反应的表示式符合事实的是( )
A. 铁和稀硫酸反应:![]()
B. 水的分解反应:![]()
C. 氧化铁放入水中:![]()
D. 将二氧化硫气体通入氢氧化钠溶液:![]()
17. 用一种试剂区别硫酸铜、氯化铁、氯化镁、氯化钠四种物质,这种试剂是( )
A. 硝酸银 B. 氢氧化钠 C. 氯化钡 D. 盐酸
18. 关于物质之间反应的分析正确的是( )
A. 生成两种化合物的反应,一定不是化合反应或置换反应
B. 碱能与所有的非金属氧化物反应
C. 生成盐和水的反应,一定是中和反应
D. 酸与活泼金属反应,一定生成盐和氢气
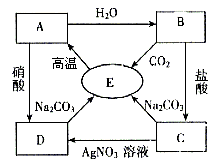
19. A、B、C、D、E中都含有同一种元素,它们之间的相互转化关系如下图所示,其中所含的相同元素是( )
A. 铜 B. 碳 C. 铁 D. 钙
20. 分子个数相等的三种物质:①一氧化氮 ②二氧化氮 ③三氧化二氮,它们之间含氧的质量分数关系是( )
A. ①+②=③ B. ①+③=②
C. ②+②=③ D. ②+③=①
二、填空题(每空1分,共25分)
21. 现有镁、碳、氢、氧四种元素,由其中一种或多种元素依次组成以下物质或粒子,写出相应符号:酸_________,碱_________,盐_________,阳离子_________,阴离子_________。
22. 请写出以下各组物质在化学性质方面存在的相似点:
(1)氢气和一氧化碳____________________________________;
(2)盐酸和氯化钠溶液____________________________________;
(3)二氧化碳和氧化钙____________________________________。
23. 写出实验室用氯酸钾制取氧气的化学方程式___________________________,反应类型属于__________________;该反应前后化合价没有发生变化的元素是_______________。
24. 我省农村正积极推广沼气项目,沼气的主要成分是(写化学式)_________;被蜂蜇虫咬后,患处由甲酸引起奇痒,若在该患处涂抹少量氨水,可以止痒,原因是____________________________________;消防队员戴的防毒面具中除活性炭外,还有少量氧化银,这是由于氧化银能与一氧化碳反应生成银和二氧化碳,化学方程式是____________________________________。
25. 废铜屑与浓硫酸反应,能制得硫酸铜,其反应原理是:
![]() ,则X是_________(写化学式)。若用废铜屑、稀硫酸和空气作原料制取硫酸铜,依次写出制备过程中发生反应的化学方程式__________________,___________________________。
,则X是_________(写化学式)。若用废铜屑、稀硫酸和空气作原料制取硫酸铜,依次写出制备过程中发生反应的化学方程式__________________,___________________________。
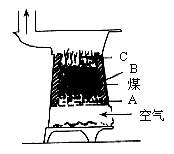
26. 煤炉里,煤燃烧时由下至上会发生一系列化学反应。下图中A、B、C处分别发生不同的化学反应,请依次写出它们的化学反应方程式:
A处___________________________;
B处___________________________;
C处___________________________。
27. A、B、C、D四个试剂瓶中分别盛碳酸钠、硝酸银、烧碱、稀硫酸四种稀溶液中的一种,取四种溶液各少量,依次滴入物质X的溶液和稀硝酸,发生的现象如下表所示:
| A | B | C | D | |
| X | 白色沉淀 | 白色沉淀 | 白色沉淀 | 无现象 |
| 稀硝酸 | 沉淀不消失 | 沉淀消失 有气体产生 | 沉淀不消失 | 无现象 |
回答:
(1)物质X的化学式是_________。
(2)物质B是_______________,加入X后反应的化学方程式是__________________,加稀硝酸后,沉淀消失的反应化学方程式是___________________________。
(3)为进一步区别A和C,可根据置换反应的原理进行实验,写出其中一个反应的化学方程式___________________________。
三、简答题(本大题共11分)
28. (3分)化学给我们的生活带来了巨大变化。在化学家眼里,空气、水、煤、石油、粮食、植物秸秆、大理石、食盐、石英砂等等,都是基本化工原料。仿照示例,从上述物质中分别选取一种作为原料,说明其在衣、住、行方面给我们带来的变化。
示例:石英砂——制取半导体材料,推动了信息技术及信息产业的发展
关于“衣” _____________________________________________(1分)
关于“住” _____________________________________________(1分)
关于“行” _____________________________________________(1分)
29. (4分)某同学把足量的铁粉放入100g稀硫酸中,并想通过硫酸的多少来计算出生成氢气的质量,但发现缺少一个数据。这个数据是什么?若想通过一定的方法测出生成氢气的质量,请设计一个实验方案(简述实验操作)。
30. (4分)小军在一次实验中,将带有铁锈的铁片放入一定量的稀硫酸中,细心观察,发现下列现象:①铁锈逐渐消失,溶液变为橙黄色;②铁片表面有气泡产生,溶液由橙黄色逐渐变为浅绿色。回答:
(1)写出现象①的反应化学方程式_________________________________;(1分)
(2)写出现象②中产生气泡的反应化学方程式_________________________________;(1分)
(3)为弄清溶液由橙黄色变为浅绿色的原因,请你帮助小军设计出探究方案(简略写出实验内容)
四、实验题(本大题共16分)
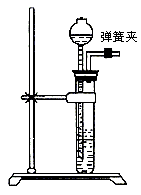
31. (6分)化学实验小组在实验室制备氢气时,发现没有锌粒或铁屑,仅有一些碎铝片。根据有关资料提示,他们将铝片放入烧碱溶液中,除去表面的氧化膜(![]() ),洗净后用于制取氢气。
),洗净后用于制取氢气。
回答下列问题:
(1)已知氧化铝与烧碱溶液反应时,会生成偏铝酸钠(![]() )和水,写出该反应的化学方程式___________________________。(1分)
)和水,写出该反应的化学方程式___________________________。(1分)
(2)图中是实验小组组装的制取氢气的发生装置,检验该装置气密性的方法是_______
____________________________________________________________________________________________________________________________________________________。(1分)
(3)用金属铝和稀盐酸反应制取氢气的化学方程式是____________________________。(1分)
(4)收集氢气的常用方法是______________________。(1分)
(5)在相同温度下,若用锌片和铝片分别与相同浓度的盐酸反应制取氢气,反应速率:锌_________铝(填“>”“=”“<”),理由是___________________________。(各1分)
32. (10分)某粗盐样品中含有杂质氯化镁、氯化钙。小林设计了以下提纯方案:
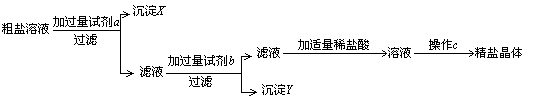
(1)若方案中先除去的是氯化镁,接着除去氯化钙,回答:
①试剂a的化学式是_________,b的化学式是__________________。(2分)
②指出操作c的名称_________。(1分)
③操作过程中加适量稀盐酸时,可能发生的反应化学方程式是__________________,____________________________________。(2分)
(以上两个反应,顺序不分先后)
(2)用图中所示装置进行过滤时,向过滤器内倾注液体的正确的方法是_________(1分)
A. 倾注时,玻璃棒插入过滤器中心
B. 倾注时,玻璃棒下端靠住过滤器内任意位置
C. 倾注时,玻璃棒下端靠住过滤器内三层滤纸一边
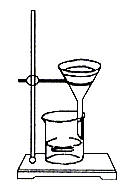
(3)若一次过滤后发现滤液仍浑浊,且滤纸未破损,需接着进行的操作是_________。(1分)
(4)若所取粗盐样品中实际含氯化钠的质量为mg,除杂后所得精盐的质量为ng,则m与n的关系是m_________n(1分)(填“>”“=”“<”),原因是__________________。(2分)
五、计算题(本大题共8分)
33. (3分)某地一不法商贩销售的“尿素”中,经检验含氮的质量分数为28%。求:
(1)已知尿素的化学式为![]() ,则尿素中氮元素的质量分数是多少?(精确到0.1%)
,则尿素中氮元素的质量分数是多少?(精确到0.1%)
(2)该商贩所售每袋“尿素”(50kg)中,实际含尿素多少千克?
34. (5分)市售双氧水溶液中含![]() 的质量分数为30%,密度
的质量分数为30%,密度![]() 。分别计算(写出计算过程,结果精确到0.1):
。分别计算(写出计算过程,结果精确到0.1):
(1)每1000mL上述双氧水溶液中,含![]() 多少克?
多少克?
(2)已知![]() 在
在![]() 催化下,可发生下列反应:
催化下,可发生下列反应:
![]()
欲用该溶液制取96g氧气,至少需取用30%的![]() 溶液多少毫升?
溶液多少毫升?
化学参考答案
一、选择题
1. D 2. C 3. C 4. B 5. A 6. C 7. C
8. A 9. B 10. C 11. B 12. B 13. D 14. B
15. C 16. D 17. B 18. A 19. D 20. A
二、填空题
21. ![]()
![]()
![]() [或
[或![]() ]
] ![]() (或
(或![]() )
)
![]() (或
(或![]() 或
或![]() 或
或![]() )
)
22. (1)可燃性(或还原性)
(2)都与![]() 溶液反应
溶液反应
(3)都能与水反应
23. ![]() 分解反应 K(或钾)
分解反应 K(或钾)
24. ![]() 氨水和甲酸发生中和反应(或氨水显碱性,或氨水显碱性甲酸显酸性)
氨水和甲酸发生中和反应(或氨水显碱性,或氨水显碱性甲酸显酸性)
![]()
25. ![]()
26. ![]()
27. (1)![]()
(2)碳酸钠(或![]() 或纯碱)
或纯碱)
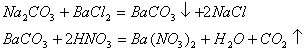
(3)![]() (或
(或![]() )
)
三、简答题
28. 石油——合成纤维,改变了服装的品质(或煤——提取染料,使服装具备丰富的色彩)
大理石——制造水泥,促进建筑材料业的发展(或煤——炼钢,促进建筑材料业的发展)
石油——合成橡胶,促进交通工业的发展(或植物秸秆——制酒精,改变燃料的结构,促进交通业的发展)
评分说明:其他合理答案,可酌情给分。
29. 稀硫酸中溶质的质量分数
在反应前称取铁的质量,反应后称取剩余铁的质量,通过参加反应的铁的质量,计算出生成氢气的质量。
评分说明:其他合理方法,可酌情给分。
30. (1)![]()
(2)![]()
(3)配制![]() (或
(或![]() )溶液,并取该溶液少许分别注入两支试管中,其一加入过量铁粉,振荡,观察橙黄色溶液是否变浅绿色;另一试管中通足量氢气,观察橙黄色溶液是否变浅绿色。
)溶液,并取该溶液少许分别注入两支试管中,其一加入过量铁粉,振荡,观察橙黄色溶液是否变浅绿色;另一试管中通足量氢气,观察橙黄色溶液是否变浅绿色。
四、实验题:
31. (1)![]()
(2)关闭弹簧夹,从长颈漏斗中慢慢注水至淹没长颈漏斗下端管口,继续注入少量水,至漏斗颈部形成水柱,静置,观察水柱是否下降(或关闭弹簧夹,从长颈漏斗中缓缓注水至淹没长颈漏斗下端管口,用热水加热试管,观察长颈漏斗颈部是否有液柱上升)
(3)![]()
(4)向下排空气法(或排水法)
(5)< 铝比锌金属活动性强
32. (1)①![]()
②蒸发
③![]()
![]()
(2)C
(3)再过滤,至滤液变澄清
(4)< 除杂过程中有新生成的![]()
五、计算题
33. 解:(1)尿素中氮元素的质量分数
![]()
(2)![]()
答:实际含尿素30kg。
34. (1)解:![]()
![]()
(2)设:至少需![]() 的质量为x
的质量为x
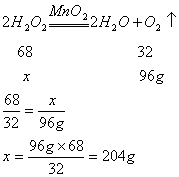
![]()
答:每1000mL双氧水溶液中含![]() ,至少需取用30%的
,至少需取用30%的![]() 溶液611.4mL。
溶液611.4mL。
