太原市2005年初中阶段学业(中等学校招生)统一考试
化学部分
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32
第I卷 (选择题 共28分)
—、选择题(本大题含14个小题,每小题2分,共28分)
在每小题给出的四个选项中,只有一项符合题目要求,请选出并在答题卡上将该项涂黑。
1.太原市被评为“节水城市”,每位市民都应树立节水意识。下列用水习惯能够节水的是
A.用淘米水浇花 B.用流动的自来水为西瓜降温
C.用大量水冲洗自行车 D.加了过量洗衣粉洗衣服,然后反复冲洗
2.“自洁净玻璃”是在玻璃表面镀上一层纳米TiO2,使玻璃具有自洁能力。TiO2属于
A.单质 B.氧化物 C. 酸 D.盐
3.农作物生长需施用氮肥、磷肥、钾肥。其中氮、磷、钾是指
A.元素 B.原子 C.分子 D.离子
4.汽车尾气中,氮的各种氧化物都可以通过灼热的铁粉转化为氮气消除其污染,其中一种的化学反应可表示为2X+3Fe △ Fe3O4+N2,则X的化学式为
A.N2O B.NO C,NO2 D.N2O4
5.下列实验操作错误的是
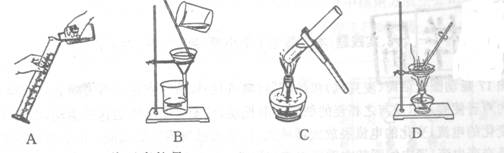
6.下列化合物中,含有+4价元素的是
A.SO2 B.KMnO4 C.FeCl3 D.H2SO4
7.在装有澄清石灰水的两支试管中,各加入一种溶液,两支试管里分别出现白色沉淀、红褐色沉淀。则加入的溶液依次是
A.碳酸钠溶液、氯化铜溶液 B.氯化钠溶液、硝酸铁溶液
C.硝酸铁溶液、碳酸钠溶液、 D.碳酸钠溶液、硝酸铁溶液
![]()
8.某原子结构示意图为 有关该原子的叙述错误的是
A.质子数为11 B.核电荷数为10 C.电子层数为3 D.核外电子数为11
9.鲜肉是日常主要食品之一,新鲜度可以通过测试pH来判断。据资料,pH与肉的新鲜度的关系为:新鲜肉pH 5.8~6.2;次鲜肉pH 6.3~6.6;变质肉pH 6.7以上。新鲜肉在变质过程中酸性强弱的变化为
A.变弱 B.变强 C.不变 D.无法确定
10.有一瓶无色溶液,要确定它是硫酸钠溶液还是氯化钾溶液,应选择的试剂是
A.硝酸银溶液 B.氯化钡溶液 C.碳酸钠溶液 D.氢氧化钾溶液
11.下列关于灭火方法的解释正确的是
A.用扇子扇灭烛火,是将可燃物与空气隔绝
B.用二氧化碳灭火,是将可燃物与空气隔绝
C.用沙土灭火,是将可燃物的温度降到着火点以下
D.用灯帽盖灭酒精灯,是将可燃物的温度降到着火点以下 。
12.有甲、乙、丙三种无色气体,分别是甲烷、氢气、一氧化碳中的一种。点燃三种无色气体。用干而冷的烧杯罩在火焰上方,乙、丙火焰上方的烧杯壁上有水滴出现,而甲火焰上方的烧杯壁上没有水滴。请你确定甲气体的名称及进一步鉴别乙、丙气体所用试剂的名称
A.甲烷、澄清石灰水 B.一氧化碳、碳酸钠溶液
C.氢气、澄清石灰水 D.一氧化碳、澄清石灰水
13.把过量的稀硫酸加入盛有少量Zn和Cu混和物的试管里,充分反应后过滤,滤液中含有的阳离子是
A.Zn2+ B.H+、Cu2+ C.H+、Zn2+ D.Zn2+、Cu2+
14.若100g过氧化氢(化学式为H2O2)溶液中氢元素的质量分数为l0%,则此溶液中过氧化氢的质量分数是
A.10% B.11.25% C.17.75% D.21.25%
第Ⅱ卷 (非选择题 共42分)
| 题 号 | 二 | 三 | 四 | 总 分 | 核 分 人 |
| 得 分 |
| 得分 | |
| 评卷人 |
二、填空题(本大题含4个小题,共18分)
15.(4分)用相应物质的化学式填空。
古代山西有许多领先的化学工艺。如1989年永济出土四尊唐
代铁牛,每尊重达30吨,震惊中外。现代炼铁用 气体还原
铁矿石,而唐代炼得如此多的铁,所用还原剂是用木材制得的一种
黑色固体 ,十分不易。这样炼得的铁易生锈变为
(填主要成分),因此铁牛留存至今,极为珍贵。又如,两千多年前太
原酿造的醋就已远近闻名,醋中除含显酸性的 外,还含
有多种营养成分,成为当时的皇家贡品。
16.大蒜有增味、杀菌等作用,被誉为“天然广谱抗菌素。”大蒜中的两种有效成分大蒜辣素和蒜氨酸的相关资料如下表所示:
| 成 分 | 化学式 | 性 质 |
| 大蒜辣素 | C6HloS20 | 无色油状液体,有臭味,难溶于水 |
| 蒜氮酸 | C6HloNOaS | 无色针状晶体,元气味,易溶于水 |
(1)大蒜辣素的相对分子质量为 ,蒜氨酸中碳、氢元素的质量比为 。
(2)表格中提供的是大蒜辣素和蒜氨酸的 性质(填“物理”或“化学”),从宏观和微观角度分析它们属于不同物质的原因 。
17.(3分)根据右图a物质的溶解度曲线,回答下列问题。
 (1)在30℃时,将30g的a物质放入100g的水中,得到的溶
(1)在30℃时,将30g的a物质放入100g的水中,得到的溶
液是 溶液,若降温到20℃时,是 溶液。
(填“饱和”或“不饱和”)
(2)将a物质的饱和溶液变为不饱和溶液的一种方法是 。
18.(7分)下图已标出四种含铜物质之间的部分转化关系。
(1)请根据你对四种物质性质的理解,用“→”标出物质间其它的转化关系。要求“→”指向生成物,并且在“→”上标出参与反应物质的化学式。
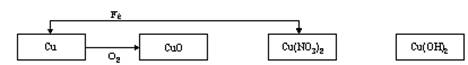
(2)写出上述转化关系中属于不同基本反应类型的两个化学方程式。
① ②
| 得分 | |
| 评卷人 |
三、实验探究题(本大题含2个小题,共17分)
15.回答实验室制取气体的有关问题。
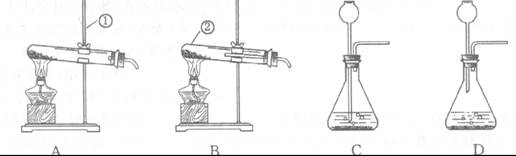
(1)图中标有序号的仪器名称是① ② 。
(2)用氯酸钾固体和二氧化锰粉末制取氧气的化学方程式为
若用此反应制氧气,可选用 装置(填字母代号)。
(3)常温下过氧化氢溶液在二氧化锰粉末的催化作用下可以生成水和氧气。若用此反应制
氧气,可选用 装置(填字母代号)。
(4)根据(2)、(3)两个实验装置的选用,归纳出实验室制取气体时,选择发生装置的依据是 和 。
20.(9分)在实验室,请你和豆豆同学共同完成有关碱的性质的探究活动。
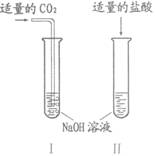 (1)根据碱与多数非金属氧化物、碱与酸反应都生成盐和水
(1)根据碱与多数非金属氧化物、碱与酸反应都生成盐和水
的规律,请写出右图所示两个反应的化学方程式:
I
Ⅱ
(2)豆豆在做这两个实验时,均没有观察到明显现象,于是
他怀疑在I、Ⅱ两只试管中并未发生化学反应。现在,请
你设计方案证明两支试管中已经发生了化学反应。
I试管中应加入 ,看到的现象是 。
Ⅱ试管中应加入 ,看到的现象是 。
(3)完成以上探究后,你向豆豆解释道: 。
| 得分 | |
| 评卷人 |
四、计算题(本大题含1个小题,共7分)
21.(7分)某工厂化验室用10%的的NaOH溶液洗涤石油产品中的残留硫酸。
(1)配制200 mL l0%的NaOH溶液(密度为1.l g/cm3),需氢氧化钠 g,
水 g。
(2)配制所需的NaOH溶液要经过以下步骤。下图中空缺的实验步骤依次是 、
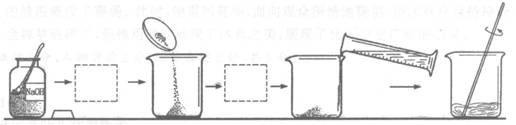 。
。
(3)用80g配制好的10%的NaOH溶液分几次洗涤一定量石油产品中的残余硫酸,洗涤至溶液恰好呈中性,此时还剩余NaOH溶液30g,求这一定量的石油产品里所含H2SO4的质量。(计算结果精确到0.1)