溶质的质量分数专题练习
1.溶液中溶质的质量分数就是 和 的 比。根据溶液中溶质质量分数的计算公式可得:溶液中溶质的质量= × 。
2.20℃时硝酸钾的饱和溶液的质量分数为24%,它表示 。
3.在 下,某(固体)物质在 克溶剂里达到 状态时所溶解的质量为该物质在这种溶剂里的溶解度。溶解度数值越大,表明该温度下,物质的溶解能力 。20℃时硝酸钾的溶解度是31.6克,这表示 。
4.20℃时,将9克食盐溶于25克水中,刚好制得饱和溶液34克,则20℃时食盐的溶解度为 ( )
A.36 B.36克 C.26.5 D.26.5克
5.20℃时,A物质的溶解度为S克,现将b克A物质放到c克水中充分溶解。
(1)如果b克A物质全部溶解,则所得溶液中A物质的质量分数为
(2)如果b克A物质不能全部溶解,则所得溶液中A物质的质量分数为 。
6.根据溶质质量、溶剂质量的变化情况,以及变化所得的结果,在表中填上相应的文字。
| 溶液中各部分变化情况 | 溶质质量 | 不变 | 不变 | 增加 | 减少 |
| 溶剂质量 | 减少 | 增加 | 不变 | 不变 | |
| 变化结果 | 溶液质量 | ||||
| 溶液浓度 |
7.图1—38是配制50克质量分数为5%的氯化钠溶液的操作过程示意图:
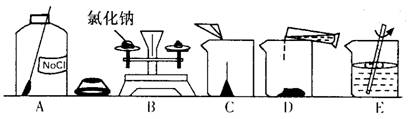
(1)B操作中应称量氯化钠的质量是 克;
(2)放好砝码和调好游码后,向托盘天平的左盘上加氯化钠时,若指针偏向分度盘的左边,应进行的操作是 ;
(3)D操作应选用 毫升的量筒(从10毫升、100毫升中选择)。量水时量筒必须放
平稳,视线要跟量筒内液面的 保持水平;
(4)E操作的作用是 。
有关溶液稀释和浓缩的计算:
[例1] 工业生产上,有时要用溶质的质量分数为10%的稀硫酸来清洗钢材。把50千克溶质的质量分数为98%的浓硫酸稀释成溶质的质量分数为10%的稀硫酸,需要水多少千克?
[例2] 配制1 000毫升溶质的质量分数为10%的稀硫酸,需要溶质的质量分数为98%的浓硫酸多少毫升?需要水多少毫升?(硫酸溶液的密度请查阅p.36表)
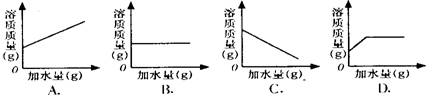
1.把m克质量分数为a%的NaCl溶液加水稀释,下列图像中正确描述溶液中溶质质量与加水质量关系的是 ( )
2.密度为1.18克/厘米’的浓盐酸(质量分数36%),用100毫升水稀释100毫升浓盐酸,所得稀盐酸的质量分数 ( )
A.等于18% B.大于18% C.小于18% D.无法确定
3.浓度为10%的食盐溶液100克,将其浓度增加到20%,可采用的方法是 ( )
A.加入10克食盐固体 B.把溶液中的水蒸发掉一半
C.加入100克10%的食盐溶液 D.把水蒸发掉50克
4.100克A溶液中水的质量分数为98%,现在要使溶液中水的质量分数变为99%,则应加入水的质量为 ( )
A.1克 B.10克 C 50克 D.100克
5.用浓度为60%的酒精溶液A与25%的酒精溶液B配制成45%的酒精溶液,则A、B溶液的质量比为 ( )
A.1:2 B.2:3 C.4:3 D.3:1
6.把溶质的质量分数为l0%的硫酸溶液50克浓缩到40克,此时溶液中硫酸的质量分数为
。
7.用溶质的质量分数为98%的浓H2SO4 25毫升(密度为1.84克/厘米3),配制溶质的质量分数为70%的硫酸溶液(密度为1.60克/厘米3),需加水多少毫升?
8.用溶质的质量分数为40%的浓氢氧化钠溶液(密度为1.43克/厘米3)配制,143克溶质的质量分数为10%的氢氧化钠溶液,需量取40%的氢氧化钠溶液 毫升与 毫升水混合而成。
