八年级科学(下)竞赛试卷
班级 姓名 学号
相对原子质量 H 1 C12 N14 O16 Na23 Mg24 S32 Cl35.5 K39 Mn55 Fe56
一.选择题20*2=40
1.某人排出的尿中含2%的尿素[ CO(NH2)2 ],如不考虑其他成分,则人尿中氮的质量分数约为 A.2% B.9.3% C.0.93% D.0.8% ( )
2.碳和氢两种元素组成的化合物,所含碳元素与氢元素的质量比为3∶1,则碳原子与氢原子的个数比为 ( )
A.12∶1 B.4∶1 C.1∶2 D.1∶4
3.在1~18号元素中X元素的原子最外层只有1个电子,Y元素的原子的第三层有6个电子,Z元素的第二层也有6个电子,在化合物中只有Z元素的化合价为负。由这三种元素组成的化合物的化学式可能是 ( )
A.X3YZ4 B.X3YZ3 C.X2YZ4 D.XYZ3
4.X原子的最外电子层上有1个电子,Y元素的化合价为-2价,由X和Y两种元素形成的化合物的化学式可能是 ( )
A.XY2 B.XY C.X2Y D.X6Y
5.等电子体具有原子数目相同,电子数目相同的特征.下列各组中的物质属于等电子体的是
A.NO和O2 B.CO和N2 C.NO2和CO2 D.SO2和ClO2 ( )
6.在FeO、Fe2O3、Fe3O4三种化合物中,与等质量铁元素相结合的氧元素的质量比为 ( )
A.6∶9∶8 B.12∶8∶9 C.2∶3∶6 D.1∶3∶4
7.在19世纪,化学家对氧化锆的化学式有争议。经测定,锆的相对原子质量为91,其氯化物的相对分子质量是233。若氧化锆中锆的化合价与氯化物中的相同,试判断氧化锆的化学式为
A.ZrO2 B.Zr2O C.Zr2O3 D.ZrO ( )
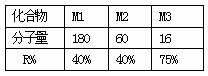 8.有M1、M2、M3 三种含R元素的化合物,已知下列数据(R%表示R元素在化合物中所占质量分数),则R的相对原子质量为
( )
8.有M1、M2、M3 三种含R元素的化合物,已知下列数据(R%表示R元素在化合物中所占质量分数),则R的相对原子质量为
( )
A.72 B.36 C.24 D.12
9.X、Y两元素的相对原子质量之比为2:1,由两元素形成的化合物中X、Y元素的质量比为2:3,其中X元素的化合物价为+a则化合物中Y元素的化合价为 ( )
A.- B.- C.- D.-
10.要使Fe3O4和FeO的含铁量相等,则它们的质量比应为 ( )
A.232:72 B.72:232 C.29:27 D.160:72
11.某种锰的氧化物中,锰、氧元素的质量比为55:56,则该氧化物中锰的化合价是( )
A.+2价 B.+4价 C.+6价 D.+7价
12.对Na2SO4、Na2S、H2S、S四种物质的叙述,正确的是 ( )
A.都含有硫元素 B.都含有硫单质 C.都含有一个硫原子 D.都是化合物
13.在化合物X2Y和YZ2中,Y的质量分数分别为40%和50%,则在化合物X2YZ3中,Y的质量分数为 ( )
A.20% B.25% C.30% D.35%
14.某些化学试剂可用于净水,水处理过程中常用到的一种无机高分子混凝剂,它的化学式为[A12(OH)nClm・yH2O]x,式中m等于 ( )
A.3-n B.6-n C.6+n D.3+n
15.已知NaHS、MgSO4、NaHSO3组成的混合物中,硫元素的质量分数为a%,则混合物中氧元素的质量分数为 ( )
A.a% B.2a% C.(100-1.75a)% D.(1-0.75a)%
16.甲、乙两种化合物都只含X、Y两种元素,甲、乙中X元素的质量分数分别是30.4%和25.9%,若已知甲的化学式是XY2,则乙的化学式只可能是 ( )
A.XY B.X2Y C.X2Y3 D.X2Y5
17.A元素与氧元素组成的氧化物分子中共有7个原子核,A元素与氧元素的质量比为31∶40,该氧化物的相对分子质量为142,则A元素的相对原子质量为 ( )
A.12 B.56 C.31 D.7
18.某粒子M2+所含的质子数为a,据此还不能确定粒子的 ( )
A.元素种类 B.在化合物中的化合价 C.中子数 D.电子数
19.X、Y均是在1~18号内的元素。它们可组成化合物X2Y3,若已知Y的核电荷数为m,则X的核电荷数不可能是 ( )
A.m+5 B.m-1 C.m-3 D.m+6
20.甲基橙(指示剂)是一种含C、H、N、S、O、Na 等元素的化合物,定量分析得到下列元素的质量分数:C为51.4%;H为4.3%;N为12.8%;S为9.8%;O为6.5%。则甲基橙的相对分子质量至少不低于 ( )
A.98 B.109 C.327 D.82
二.填空题 11*3=33
21.已知铁的氧化物中通常只有+2、+3两种化合价,氧元素在化合物中通常显-2价,测得铁的某种氧化物晶体的化学式为Fe23O25,则其中Fe2+、Fe3+的粒子个数比为 。
22.录像用的高性能磁粉,主要材料之一是由三种元素组成的化学式为CoxFe3-xO3+x的化合物。已知氧为-2价,钴(Co)和铁可能显+2或+3价,且上述化合物中,每种元素只有一种化合价,则x值为 ,铁的化合价为
23.一瓶NO和NO2的混合气体,测知其中氮元素与氧元素的质量比为1∶2,则NO和NO2的质量比为 。
24.在K2R2O7中(R代表某元素)含钾元素26.5%,氧元素38.1%,推算出R的相对原子质量是 。
25.若某质量的SO2与某质量的SO3中,含有等质量的氧元素,则SO2 与SO3的质量比是
。相等质量的SO2和SO3中所含氧元素的质量比是 。
26.蛋腐败时会产生一种无色、有臭鸡蛋味的硫化氢(H2S)气体,它是一种大气污染物,在空气中点燃完全燃烧时,生成SO2和水,把H2S通入浓硫酸中,发生的反应为:H2S+H2SO4(浓)=SO2+X +2H2O
(1)上述内容中,属于H2S物理性质的是
(2)写出H2S在空气中完全燃烧的化学方程式
(3)H2S与H2SO4(浓)反应时,生成物中X的化学式是
(4)若尾气中含有H2S,用浓H2SO4来吸收行吗?为什么? 。
八年级科学(下)竞赛试卷06.5
班级 姓名 学号 成绩
一.选择题40分
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | ||||||||||
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 |
二.填空题33分
21.
22. 。
23
24.
25 。
26
三.计算题27分
27. 过氧乙酸(CH3COOOH或C2H4O3)是一种常用的消毒剂。
(1)它由_____种元素组成,一个过氧乙酸分子由 个原子构成。
(2)若用0.2%的溶液对全校教室进行消毒,一次需50千克。问该溶液含过氧乙酸溶质多少千克?配制50千克0.2%的该溶液时需20%的过氧乙酸溶液多少千克?
28. 将氯酸钾和二氧化锰的混合物25克加热到一定时候时,得到20.2克固体混合物:
求:(1)生成多少克氧气?
(2)有多少克氯酸钾分解?
(3)如果氯酸钾分解了50%。则20.2克物质中含有哪些物质各多少克?
29. 现有一种晶体(Na2CO3・nH 2O在不同温度下,可失去部分或全部结晶水。),为了测定其组成,在不同温度下加热(温度依次升高),实验结果如下:
| 实验次序 | 温度 | 冷却后质量(坩埚和试样)(克) |
| 1 | T1 | 48.5 |
| 2 | T2 | 44.9 |
| 3 | T3 | 43.1 |
| 4 | T4 | 43.1 |
坩埚的质量为32.5克,坩埚和晶体的质量为55.7克
求1)第一次加热后坩埚里剩余试样的质量和失去的结晶水的质量
2)第二次加热后坩埚里试样的结晶水的质量分数
3)原样品的化学式
八年级科学(下)竞赛辅导试卷⑴ 06年5月
班级 姓名 学号
一.选择题20*2=40
1.某人排出的尿中含2%的尿素[ CO(NH2)2 ],如不考虑其他成分,则人尿中氮的质量分数约为 ( C )
A.2% B.9.3% C.0.93% D.0.8%
2.碳和氢两种元素组成的化合物,所含碳元素与氢元素的质量比为3∶1,则碳原子与氢原子的个数比为 ( D )
A.12∶1 B.4∶1 C.1∶2 D.1∶4
3.在1~18号元素中X元素的原子最外层只有1个电子,Y元素的原子的第三层有6个电子,Z元素的第二层也有6个电子,在化合物中只有Z元素的化合价为负。由这三种元素组成的化合物的化学式可能是 ( C )
A.X3YZ4 B.X3YZ3 C.X2YZ4 D.XYZ3
4.X原子的最外电子层上有1个电子,Y元素的化合价为-2价,由X和Y两种元素形成的化合物的化学式可能是 ( C )
A.XY2 B.XY C.X2Y D.X6Y
5.等电子体具有原子数目相同,电子数目相同的特征。下列各组中的物质属于等电子体的是
A.NO和O2 B.CO和N2 C.NO2和CO2 D.SO2和ClO2 ( B )
6.在FeO、Fe2O3、Fe3O4三种化合物中,与等质量铁元素相结合的氧元素的质量比为 ( A )
A.6∶9∶8 B.12∶8∶9 C.2∶3∶6 D.1∶3∶4
7.在19世纪,化学家对氧化锆的化学式有争议。经测定,锆的相对原子质量为91,其氯化物的相对分子质量是233。若氧化锆中锆的化合价与氯化物中的相同,试判断氧化锆的化学式为
A.ZrO2 B.Zr2O C.Zr2O3 D.ZrO ( A )
 8.有M1、M2、M3 三种含R元素的化合物,已知下列数据(R%表示R元素在化合物中所占质量分数),则R的相对原子质量为
( D )
8.有M1、M2、M3 三种含R元素的化合物,已知下列数据(R%表示R元素在化合物中所占质量分数),则R的相对原子质量为
( D )
A.72 B.36 C.24 D.12
9.X、Y两元素的相对原子质量之比为2:1,由两元素形成的化合物中X、Y元素的质量比为2:3,其中X元素的化合物价为+a,则化合物中Y元素的化合价为 ( B )
A.- B.- C.- D.-
10.要使Fe3O4和FeO的含铁量相等,则它们的质量比应为 ( C )
A.232:72 B.72:232 C.29:27 D.160:72
11.某种锰的氧化物中,锰、氧元素的质量比为55:56,则该氧化物中锰的化合价是( D )
A.+2价 B.+4价 C.+6价 D.+7价
12.对Na2SO4、Na2S、H2S、S四种物质的叙述,正确的是 ( A )
A.都含有硫元素 B.都含有硫单质 C.都含有一个硫原子 D.都是化合物
13.在化合物X2Y和YZ2中,Y的质量分数分别为40%和50%,则在化合物X2YZ3中,Y的质量分数为 ( B )
A.20% B.25% C.30% D.35%
14.某些化学试剂可用于净水,水处理过程中常用到的一种无机高分子混凝剂,它的化学式为[A12(OH)nClm・yH2O]x,式中m等于 ( B )
A.3-n B.6-n C.6+n D.3+n
15.已知NaHS、MgSO4、NaHSO3组成的混合物中,硫元素的质量分数为a%,则混合物中氧元素的质量分数为 ( C )
A.a% B.2a% C.(100-1.75a)% D.(1-0.75a)%
16.甲、乙两种化合物都只含X、Y两种元素,甲、乙中X元素的质量分数分别是30.4%和25.9%,若已知甲的化学式是XY2,则乙的化学式只可能是 ( D )
A.XY B.X2Y C.X2Y3 D.X2Y5
17.A元素与氧元素组成的氧化物分子中共有7个原子核,A元素与氧元素的质量比为31∶40,该氧化物的相对分子质量为142,则A元素的相对原子质量为 ( C )
A.12 B.56 C.31 D.7
18.某粒子M2+所含的质子数为a,据此还不能确定粒子的 ( C )
A.元素种类 B.在化合物中的化合价 C.中子数 D.电子数
19.X、Y均是在1~18号内的元素。它们可组成化合物X2Y3,若已知Y的核电荷数为m,则X的核电荷数不可能是 ( D )
A.m+5 B.m-1 C.m-3 D.m+6
20.甲基橙(指示剂)是一种含C、H、N、S、O、Na 等元素的化合物,定量分析得到下列元素的质量分数:C为51.4%;H为4.3%;N为12.8%;S为9.8%;o为6.5%。则甲基橙的相对分子质量至少不低于 ( C )
A.98 B.109 C.327 D.82
二.填空题 11*3=33
21.已知铁的氧化物中通常只有+2、+3两种化合价,氧元素在化合物中通常显-2价,测得铁的某种氧化物晶体的化学式为Fe23O25,则其中Fe2+、Fe3+的粒子个数比为 19∶4 。
22.录像用的高性能磁粉,主要材料之一是由三种元素组成的化学式为CoxFe3-XO3+x的化合物。已知氧为-2价,钴(Co)和铁可能显+2或+3价,且上述化合物中,每种元素只有一种化合价,则x值为 1 ,铁的化合价为 +3 ,钴的化合价为 +2 。
23.一瓶NO和NO2的混合气体,测知其中氮元素与氧元素的质量比为1∶2,则NO和NO2的质量比为 5∶23 。
24.在K2R2O7中(R代表某元素)含钾元素26.5%,氧元素38.1%,推算出R的相对原子质量是 52 。
25.若某质量的SO2与某质量的SO3中,含有等质量的氧元素,则SO2 与SO3的质量比是
___6∶5___。相等质量的SO2和SO3中所含氧元素的质量比是___5∶6___。
26.蛋腐败时会产生一种无色、有臭鸡蛋味的硫化氢(H2S)气体,它是一种大气污染物,在空气中点燃完全燃烧时,生成SO2和水,把H2S通入浓硫酸中,发生的反应为:H2S+H2SO4(浓)=SO2+X +2H2O
(1)上述内容中,属于H2S物理性质的是 无色、有臭鸡蛋味的 气体
(2)写出H2S在空气中完全燃烧的化学方程式 2H2S+3O2===2SO2+ 2H2O
(3)H2S与H2SO4(浓)反应时,生成物中X的化学式是 S
(4)若尾气中含有H2S,用浓H2SO4来吸收行吗?为什么? 不行,会污染空气。 。
三.计算题8+10+9=27
27. 过氧乙酸(CH3COOOH或C2H4O3)是一种常用的消毒剂。
(1)它由___3__种元素组成,一个过氧乙酸分子由 9 个原子构成。
(2)若用0.2%的溶液对全校教室进行消毒,一次需50千克。问该溶液含过氧乙酸溶质多少千克?配制50千克0.2%的该溶液时需20%的过氧乙酸溶液多少千克?
答0.1 千克 0.5千克
28. 将氯酸钾和二氧化锰 的混合物25克加热到一定时候时,得到20.2克固体混合物:
求:(1)生成多少克氧气?
(2)有多少克氯酸钾分解?
(3)如果氯酸钾分解了50%。则20.2克物质中含有哪些物质各多少克?
答4.8克 12.25克 氯酸钾12.25克 氯化钾 7.45克 二氧化锰 0.5克
29. 现有一种晶体(Na2CO3・nH 2O在不同温度下,可失去部分或全部结晶水。),为了测定其组成,在不同温度下加热(温度依次升高),实验结果如下:
| 实验次序 | 温度 | 冷却后质量(坩埚和试样)(克) |
| 1 | T1 | 48.5 |
| 2 | T2 | 44.9 |
| 3 | T3 | 43.1 |
| 4 | T4 | 43.1 |
坩埚的质量为32.5克,坩埚和晶体的质量为55.7克
求1)第一次加热后坩埚里剩余试样的质量和失去的结晶水的质量 16克7.2克
2)第二次加热后坩埚里试样的结晶水的质量分数 14.5%
3)原样品的化学式 Na2CO3・7H 2O