第二章 空气与生命
第一节空气
基础:
1、对于空气,正确的叙述是:( )
A 新鲜空气是纯净物 B 空气是由几种元素组成的混合物
C 氧气质量占空气质量的21%
D 空气是由几种单质和几种化合物组成的混合物
2、空气中作为绿色植物进行光合作用的重要原料是( )
A 水蒸气 B 氧气 C 氮气 D 二氧化碳
3、在空气中,按体积百分比计算,含量最多的气体是( )
A 氧气 B 二氧化碳 C 氮气 D 水蒸气
4、在18世纪70年代首先通过实验得出“空气是由氮气和氧气组成的”结论的科学家是( )
A 拉瓦锡 B 汤姆森 C 道尔顿 D 门捷列夫
5、下列事实说明空气中含有哪些成分:①木炭在空气中燃烧 ;②酥脆的饼干在空气中逐渐变软 ;③空气中制氮肥的原料 ;④长期放在空气中的澄清石灰水表面有一层白色物质 。
提高:
6、下列因果关系不成立的是( )
A 因为氧气具有助燃性,所以可用于提高炼钢炉的温度
B 因为干冰蒸发时吸收大量热,并不留下液体,所以是优良的致冷剂
C 因为稀有气体有各种各样的颜色,所以可用于制造霓虹灯
D 因为氮气性质较不活泼,所以灯泡中充氮气可延长作用寿命
7、大气组成(体积分数)示意图。下列说法正确的是( )
A.地球和火星的大气中O2的体积分数相同
B. 地球和火星的大气中都含有N2
C. 地球和火星的大气中CO2的体积分数相同
 D. 地球和火星的大气组成完全相同。
D. 地球和火星的大气组成完全相同。
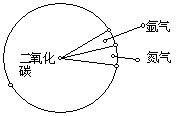
火星的大气组成 地球的大气组成
8、通常状况下,人体呼出的气体中部分气体的含量和空气中气体的含量如下表所示。
(含量指各组分的体积分数)
| 空气中的含量(%) | 呼出气体中的含量(%) | |
| 氧气 | 21 | 15.7 |
| 二氧化碳 | 0.03 | 3.6 |
| 水 | <0.03 | 6.2 |
请你利用所学知识,完成下列实验报告、并设计实验:验证剩余的一种气体成分在空气中和人体呼出气体中含量的不同,答案写在相应的空格中。(使用的仪器和药品可以任选,实验室备有刚收集好的呼出气体250mL两瓶)
| 取其中一瓶呼出气体和等体积的一瓶空气,将燃着的小木条分别插入集气瓶中,盖上玻璃片 | 人体呼出气体中氧气的含量少于空气中氧气的含量 | |
| 呼出气体瓶中澄清石灰水变浑浊,空气瓶中无明显现象 | ||
拓展:
9、某同学可用如图实验粗略测定空气中氧气的体积分数,图中烧杯上方玻璃管(预先固定好),中部有一可滑动的活塞,活塞左端管内有密封的空气,活塞右端的玻璃管口与空气连通,实验开始前活塞处在刻度为5cm处。
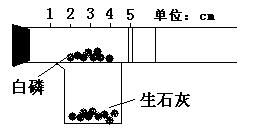 |
⑴向烧杯中加入适量的水,与生石灰反应的目的是 ;
⑵可观察到玻璃管内发生的现象是白磷(足量) ;活塞向 (填左或右)移动;实验结束后恢复到常温,活塞停在约 cm处,据此可得出结论
是 。
10、19世纪末,科学家瑞利通过如下两种实验方法制得氮气,并测定其密度,从而导致了科学上的某项重大发现。请你参与他的科学发现过程,填写如下空格:
实验一:
⑴ 将清新洁净的空气通过足量氢氧化钠溶液(可吸收二氧化碳),再通过浓硫酸(有吸水性)。通过氢氧化钠溶液的目的是为了除去空气中的 。通过浓硫酸的目的的为了除去空气中的 。
⑵ 将空气通过能与氧气反应的物质(瑞利教授提醒你:反应不能生成新的气体)请写出能用于除尽氧气的物质名称: 。
⑶ 收集气体,并测定该气体的密度。密度为:1.2572g/L。
实验二:用亚硝酸钠(NaNO2)和氯化铵(NH4Cl)反应制取氮气,同时还生成了氯化钠和一种最常见的溶剂。测得由此法得到的氮气密度为1,2508g/L。
分析两种方法测得氮气密度不完全一样的原因是: 。
答案:
1、 D
2、 D
3、 C
4、 A
5、 氧气、水蒸气、氮气、二氧化碳
6、 C
7、 B
8、
| 呼出气体瓶中木条熄灭,空气瓶中无明显变化 | ||
| 取其中一瓶呼出气体和等体积的一瓶空气,将澄清石灰水倒入瓶中,盖上玻璃片,振荡 | 人体呼出气体中二氧化碳的含量多于空气中二氧化碳的含量 | |
| 取二片干燥的玻璃片,向其中的一片上呼气,另一片放置在空气中 | 呼气的玻璃片上出现小水珠,空气中的玻璃片上无明显现象 | 人体呼出气体中水蒸气的含量多于空气中水蒸气的含量 |
9、(1)产生热量,使白磷燃烧
(2)剧烈燃烧,产生大量白烟;右;4;氧气体积约占空气体积的1/5
10、(1)二氧化碳;水蒸气
(2)磷
从空气中获得的氮气中含有稀有气体。