九年级科学常见的酸和碱复习练习
一、选择题
1.硫代硫酸钠晶体是一种恒温保温瓶的填充物,硫代硫酸钠(Na2S2O3)属于( D )
A.氧化物 B.酸 C.碱 D.盐
(类似中考题)(1)体操运动中在上器械之前常用“镁粉”搓手,“镁粉”的主要成分是MgCO3。试根据常见物质的类别判断出MgCO3属于( D )
A.氧化物 B.酸 C.碱 D.盐
(2)食品受潮后更易变质,因此许多食品包装中常放置干燥剂。其中生石灰(CaO)和硅胶(主要成分是二氧化硅)是常用的干燥剂,生石灰和二氧化硅都属于( D )
A.酸 B.碱 C.盐 D.氧化物
(3)光导纤维是将二氧化硅在高温下熔化、拉制成粗细均匀的光纤细丝,是信息高速公路的基础材料,在通讯、医疗、科技等领域都有广泛应用。二氧化硅(SiO2)属于( A )
A.氧化物 B.酸 C.碱 D.盐
2. 图2 所示实验操作不正确的是( A )
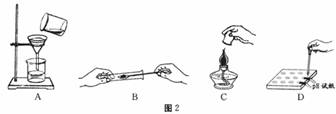
3.下列操作中,不正确的是( AD )
A.用胶头滴管向试管中滴加液体时,把滴管伸入试管内 B.把氢氧化钠固体放在天平左盘的玻璃器皿中称量
 C.在实验室里制取CO2气体时,应先检查装置气密性
C.在实验室里制取CO2气体时,应先检查装置气密性
D.浓硫酸沾到皮肤上,要立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液
4.某同学设计的下列各实验方案中,你认为不能达到实验目的的是( D )
A.用燃着的木条鉴别二氧化碳和氧气
B.加入适量的澄清的石灰水,以除去CaCl2溶液中的HCl
C.用浓硫酸除去氢气中混有的水蒸气
D.用石蕊试液鉴别澄清的石灰水和氢氧化钠溶液
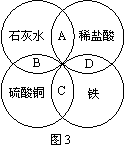
5. 铁、盐酸、石灰水、硫酸铜是初中科学中常见的物质,四种物质间的反应关系如图3所示,图中两圆相交部分(A、B、C、D)表示物质间反应的主要实验现象,其中描述正确的是( D )
A.有气泡产生 B.无明显现象 C.有红色固体析出 D.有蓝色沉淀生成
6.小王测得生活中一些物质的PH如下表,下列说法不正确的是( B )
| 物质 | 肥皂水 | 雨水 | 蔗糖水 | 食醋 | 纯碱水 | 柠檬汁 |
| PH | 10.2 | 5.8 | 7.0 | 3.3 | 8.1 | 2.0 |
A.蔗糖水是中性物质 B.肥皂水的碱性比纯碱水弱 C.柠檬汁的酸性比食醋强 D.雨水能使蓝色石蕊试纸变红
(类似中考题)(1)下列四种物质呈碱性的是 ( A )
| A | B | C | D | |
| pH | 7.4-7.9 | 6.3—6.6 | 3.5-4.55 | 2.9—3.3 |
(2)13.某同学不小心被黄蜂蛰了(黄蜂毒液呈碱性),为了减轻疼痛可以涂抹( B )
A.浓硫酸 B.食醋(pH=3) C.食盐水(pH=7) D.苏打或肥皂水(pH=9-10)
(3)某硫酸溶液的酸性太强,现要调节硫酸溶液的pH在一定范围内,但不能高于7,下列方法中能确保达到这一目标的最好方法是( D )
A.蒸发溶剂 B.加入硝酸钡 C.加入碳酸钠 D.用水稀释
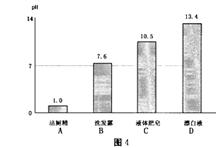 (4)家庭常用洗涤剂的pH 如图4 所示,其中最接近中性的是( B )
(4)家庭常用洗涤剂的pH 如图4 所示,其中最接近中性的是( B )
7. 以下说法正确的是( B )
A.中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应
B.氧化物中含有氧元素,而含氧元素的化合物不一定是氧化物
C.碱中都含有氢元素,所以含有氢元素的化合物一定是碱
D.置换反应一定有单质生成,所以有单质生成的反应一定是置换反应
8.下列物质的溶液长期放置在空气中,溶液质量因发生化学变化而减少的是(A )
A.烧碱 B.石灰水 C.浓盐酸 D.氯化钾
(类似中考题)(1)下列质量增加的变化有一种与其它三种存在本质的区别,这种变化是( B )
A.长期放置在空气中的氢氧化钠质量增加 B.长期敞口放置的浓硫酸质量增加
C.久置的生石灰质量增加 D.久置的铁钉生锈质量增加
(2)盛有饱和氢氧化钠溶液的烧杯在空气中放置一段较长时间,该溶液中的( A )
A.氧氧化钠的质量减小 B.氧氧化钠的质量保持不变
C.氧氧化钠的质量分数增大 D.氧氧化钠的质量分数保持不变
(3)为了检验长期暴露在空气中的氢氧化钠固体是否变质,下列方法正确的是 ( B )
A.放入水中,看是否全部溶解 B.滴加稀盐酸,看是否有气泡产生
C.滴加酚酞,看是否变色 D.用手接触,看是否有滑腻感
9.下列物质的用途,是利用其物理性质的是( A )
A.干冰用于人工降雨 B.盐酸用于除铁锈 C.氧气用于医疗急救 D.熟石灰用于改良土壤酸性
(类似中考题)(1)有关氢氧化钠的叙述不正确的是( D )
A.露置在空气中易变质 C.溶于水时放出热量 B.能使紫色石蕊试液变蓝色 D.能做治疗胃酸过多的药物
(2)将酚酞试液滴人碳酸钠溶液中,发现溶液变成了红色。由此可得到的信息是 ( BD )
A.碳酸钠是一种碱 B.碳酸钠溶液呈碱性 C.碳酸钠是一种白色固体 D.碳酸钠的pH大于7
(3)四位同学在一次小组讨论中,分别发表了各自的观点,其中正确的是( A )
A.能使紫色石蕊试液变红的溶液呈酸性 B.能使酚酞试液变红的物质就是碱
C.生成盐和水的反应一定是中和反应 D.能与BaCl2溶液反应产生沉淀的物质就是硫酸
(4)铜片在酒精灯上加热后表面变黑,有同学认为黑色物质是氧化铜(CuO),也有同学认为黑色物质是酒精不完全燃烧生成的炭黑(C)。下列试剂中,只要一步反应即可判断哪种观点正确的是( B )
A.蒸馏水 B.稀硫酸 C.氯化钡溶液 D.氢氧化钠溶液
(5)白蚁会腐蚀木头,它分泌的蚁酸是一种酸,还能腐蚀很多建筑材科。下列建筑材料.不容易被白蚁腐蚀的是( D )
A.大理石 B.铝合金 C.钢筋 D.铜制品
(6)把含有少量氧化铜的铁粉加入稀盐酸中,加热充分反应后,发现铁粉有剩余。将溶液过滤,滤液中可能含有的溶质是( D )
A.稀盐酸 B.氯化铜 C.氯化铁 D.氯化亚铁
10.下列除去杂质的方法中,错误的是( D )
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A. | 稀硫酸 | 铜 | 过滤 |
| B. | CaSO4溶液 | 稀硫酸 | 过量CaCO3、过滤 |
| C. | FeCl2溶液 | CuCl2 | 过量铁粉、过滤 |
| D. | 二氧化碳 | 一氧化碳 | 点燃 |
11.现有四组物质的溶液,仅用酚酞试液及同组物质之间相互反应就能鉴别出来的是 ( B )
A.NaOH Ba(OH)2 HCl B.NaOH HCl NaCl
C.NaOH HC1 HNO3 D.H2SO4 NaCl Na2SO4
(类似中考题)(1)下列实验能利用厨房中的食盐、食醋、纯碱三种物质做成功的是( B )
①检验自来水中是否含有氯离子;②检验鸡蛋壳能否溶于酸;③除去热水瓶中的水垢。
A.①②③ B.②③ C.①③ D.①②
(2)某同学设计的下列各实验方案中,你认为不能达到实验目的的是( D )
A.用燃着的木条鉴别二氧化碳和氧气 B.加入适量的澄清的石灰水,以除去CaCl2溶液中的HCl
C.用浓硫酸除去氢气中混有的水蒸气 D.用石蕊试液鉴别澄清的石灰水和氢氧化钠溶液
(3)下列试剂中,能把KOH溶液、稀硫酸、CaCl2溶液一次鉴别出来的是( B )
A.KCl溶液 B. K2CO3溶液 C. NaNO3溶液 D.稀盐酸
(4)小玲猜测一瓶久置于空气中的NaOH溶液中含有了Na2CO3,她设计的下列实验能对此猜测提供有力实证的是 ( B )
A.滴加CuSO4溶液 B.滴加稀盐酸 C.滴加酚酞试液 D.滴加石蕊试液
12.由Mg(OH)2和MgO组成的混合物,测得其中含镁元素的质量分数为48%。取该混合物10g,将其投入适量的稀硫酸中恰好完全反应,所得溶液中溶质的质量为( B )
A.12g B.24g C.36g D.48g
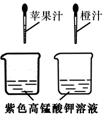 13.根据维生素C能够使紫色高锰酸钾溶液褪色的原理,用右图所示的实验可以测定出苹果汁和橙汁中维生素C含量的相对多少。要得出正确结论,实验过程中不需要进行控制的条件是( D )
13.根据维生素C能够使紫色高锰酸钾溶液褪色的原理,用右图所示的实验可以测定出苹果汁和橙汁中维生素C含量的相对多少。要得出正确结论,实验过程中不需要进行控制的条件是( D )
A.烧杯中溶液的体积 B.两个胶头滴管滴出的每滴果汁的体积
C.烧杯中紫色高锰酸钾溶液的浓度 D.胶头滴管滴出的果汁的滴数
14.下列推论正确的是( D )
(A)碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
(B)酸与碱反应生成盐和水,所以生成盐和水的反应一定是酸与碱的反应
(C)燃烧都伴随着发光、放热,所以有发光、放热现象的就是燃烧
(D)碱性溶液能使石蕊试液变蓝,所以能使石蕊试液变蓝的溶液呈碱性
15.有下列四种实验设计及操作,实验过程中其现象不足以说明C02与Na0H溶液发生了反应的是( B )
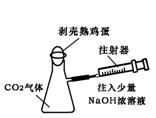
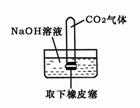
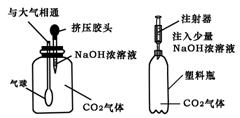
(A) (B) (C) (D)
二、填空
1.“果导片”是一种常用缓泻剂,主要成分是酚酞。某同学欲将其作为酚酞指示剂的替代品,他将“果导片”研成粉末放入酒精中,搅拌、静置,取上清液滴入白醋和食盐水,看到______不变色______________,滴入澄清石灰水发现__变红色____;确定“果导片”可作酸碱指示剂使用。当他用饮料吸管向滴有“果导片”清液的澄清石灰水吹气时,可观察到____澄清石灰水变浑浊_现象。
2.(1)写出下列物质的名称、俗名或化学式。
| 名称 | 汞 | 氧化钙 | 碳酸钠 |
| 俗名 | 水银 | 生石灰 | 纯碱 |
| 化学式 | Hg | CaO | Na2CO3 |
(2)写出下列化学方程式:
①电解水制取氢气: 2H2O 电解 2H2↑+O2 ↑ ;
②曾青(CuSO4)得铁化为铜: CuSO4+Fe==FeSO4+Cu 。
3. 小丽午餐时买了一份清炒菠菜和一份豆腐肉片汤,但同学告诉她菠菜不能与豆腐同食。
[发现问题]菠菜为什么不能与豆腐同食?
[查阅资料]a.制作豆腐需要加入石膏(主要成分:CaSO4);b.菠菜中含有草酸、草酸盐等成分;c.草酸钙是一种既不溶于水也不溶于醋酸的白色固体,是诱发人体结石的物质之一。
[提出猜想]菠菜与豆腐同食可能会产生人体不能吸收的沉淀物。
[设计实验]
| 实验步骤 | 实验现象 | 实验结论 |
| ①将菠菜在少量开水中煮沸2~3min,取l~2mL滤液于试管中,并滴加少量 溶液 | 产生白色沉淀 | 有草酸钙生成 |
| ②在步骤①的沉淀物中加入过量醋酸 | 沉淀部分溶解,且产生气泡 | 被溶解的沉淀一定 不是 草酸钙 |
[发现新问题]被溶解的沉淀是什么?产生的气体又是什么?于是她又设计如下实验进一步探究:
| 实验步骤 | 实验现象 | 实验结论 |
| ③将步骤②产生的气体 通入 澄清石灰水 中 | 澄清石灰水变浑浊 | 产生的气体是 二氧化碳 ;步骤②被溶解的沉淀是碳酸钙 |
[反思与应用]
(1)家庭中常常将菠菜放在开水中煮沸2~3min捞出后再烹饪,其目的是 除去菠菜中的草酸和草酸盐 ;
(2)联想到人体胃液中含有盐酸,请提出一个你想要探究的新问题: 盐酸能不能溶解草酸盐呢 。
4.合金A由四种单质组成,已知:①合金A中不含K、Ca、Na;②气体B可燃;③气体G为人体新陈代谢的主要产物之一,请据图回答以下问题:

(1)合金A由哪些单质组成(用化学式表示): Fe 、 Cu 、 C 、 Mg(或者Al) ;
(2)写出反应①的化学方程式: 3FeCl2+2Al==2AlCl3+3Fe ;
(3)写出反应②的化学方程式: CuO+H2SO4==CuSO4+H2O 。
5. 氢氧化钠是化学实验室中常用的试剂。
(1)氢氧化钠固体曝露在空气中,容易 潮解 ,还能 吸收二氧化碳反应 ,所以必须密封保存。
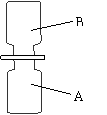 (2)实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,其原因是在常温下,氢氧化钠与玻璃中的二氧化硅缓慢地发生反应,产物使瓶口与瓶塞粘合在一起,反应的化学方程式为:SiO2 + 2NaOH == X
+ H2O,试推断X的化学式为
(2)实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,其原因是在常温下,氢氧化钠与玻璃中的二氧化硅缓慢地发生反应,产物使瓶口与瓶塞粘合在一起,反应的化学方程式为:SiO2 + 2NaOH == X
+ H2O,试推断X的化学式为
Na2SiO3 。
6. 化学课上老师表演了一个小魔术——“无中生有”:相同条件下,向A、B两个体积相同的集气瓶中分别充满无色的硫化氢(H2S)气体和二氧化硫气体。如图所示,抽开毛玻璃片,瓶口对紧,颠倒几次,使两种气体充分混合。一会儿,观察到两瓶内壁附着淡黄色固体颗粒。请回答下列问题:
![]()
![]()
![]() (1)若用“ ”表示氢原子,用“ ”表示氧原子,用“ ”表
(1)若用“ ”表示氢原子,用“ ”表示氧原子,用“ ”表
示硫原子,上述反应过程可用下图表示:

该反应的化学方程式为_____2H2S+SO2==3S+2H2O_____________;
硫化氢、二氧化硫中硫元素的化合价分别为____-2价 和+4价________________。
(2)如果这两个瓶子是质地较软的塑料瓶,我们将会观察到塑料瓶变瘪了,原因是___气体反应生成了固体物质,外界大气压大于瓶内压强__。
(3)已知:相同条件下,相等体积的气体所含的分子数目相等。反应完毕,瓶中剩余的气体为__二氧化硫___,处理该气体的方法是_____用氢氧化钠溶液来吸收______。
7. 某工厂实验室的废水中含有大量的硝酸银和硝酸铜,某校兴趣小组对其进行了如下研究。

(1)操作A是__过滤__(2)溶液M中含有的溶质可能有哪些情况_①硝酸亚铁②硝酸亚铁和硝酸铜③硝酸亚铁、硝酸铜、硝酸银__
