选择题训练(6)
一、选择题(每小题只有一个正确答案,每小题4分,共32分)
1.下列反应中,调节反应物的用量或浓度以后,不会改变反应产物的是
A.酒精在氧气中燃烧 B.在硫酸中加入铝粉
C.将二氧化碳气体通入烧碱中 D.向盐酸中加入铁钉
2.下列叙述中,不正确的是
A.原电池负极上发生的反应是氧化反应
B.失电子能力弱的物质获得电子的能力一定强
C.阳离子在氧化还原反应中,可能表现氧化性,也可能表现还原性
D.氯气分子在反应中,作氧化剂的同时也可能是还原剂
3.有氧化铜和二氧化二铁的混合物ag,加入2mol/L的HCl溶液50mL,恰好完全溶解,若将2ag该混合物在CO气流中加热并充分反应,冷却后,剩余固体的质量为
A.(2a-1.6)g B.(2a-3.2)g C.1.6ag D.0.8ag
4.将NH3气体通入到饱和食盐水中,没有沉淀生成,再通入适量CO2有晶体析出,该晶体是
A.Na2CO3 B.NaHCO3 C.NaCl D.NaOH
5.下列实验事实可以用同一化学反应原理解释的是
A.乙烯与SO2都能使溴水褪色
B.氢氧化钠和纤维素都能与醋酸反应
C.烧碱和乙酸钠的溶液都能使酚酞试液变红
D.向乙醛和葡萄糖溶液中加入新制氢氧化铜,加热,都有砖红色沉淀产生
6.以下方法中能够证明某无色透明液体是纯净水的是
A.测得该溶液中c(H+)=c(OH-)
B.向其中投入豆粒大小的金属钠,钠浮在液面上迅速游动,发出咝咝响声
C.在一个大气压下,4℃时测得其密度为1g/mL
D.测其导电能力很弱
7.在一支25 mL的酸式滴定管中盛入0.lmol・L-1 HCl溶液,其液面恰好在5 mL的刻度处,若把滴定管中的溶液全部放入烧杯中,然后以0.lmol・L-1 NaOH 溶液进行中和.则所需 NaOH 溶液的体积
A.大于20 mL B.小于20 mL C.等于20 mL D.等于5 mL
8.在100mL某混合溶液中,c(HNO3):0.4 molL-1,c(H2SO4)=0.1 molL-l,向其中加入1.92gCu粉,微热充分反应后溶液中的c(Cu2+)为
A.0.15m01.L-1 B.0.225mo1.L-1 C.0.3mo1.L-1 D.无法计算
二、选择题(每小题4分,10小题共40分,每小题有一个或两个正确选项。)
9.某同学想用实验证明高锰酸钾溶液的紫红色是MnO4-离子的颜色,而不是K+离子的颜色,他设计的下列实验步骤中没有意义的是
A. 将高锰酸钾晶体加热分解,所得固体质量减少
B. 观察氯化钾溶液没有颜色,表明溶液中K+无色
C. 在氯化钾溶液中加入适量锌粉振荡,静置后未见明显变化,表明锌与K+无反应
D. 在高锰酸钾溶液中加入适量锌粉振荡,静置后见紫红色褪去,表明MnO4-离子为紫红色
10.某密闭容器中放入一定量的NO2,发生反应2NO2(g)![]() N2O4(g)+Q,在达平衡后,若分别单独改变下列条件,重新达到平衡后,能使平衡混合气体平均相对分子质量减小的是
N2O4(g)+Q,在达平衡后,若分别单独改变下列条件,重新达到平衡后,能使平衡混合气体平均相对分子质量减小的是
A. 通入N2 B. 通入NO2 C. 通入N2O4 D. 降低温度
11.已知C-C键可以绕键轴自由旋转,结构简式为![]() 的烃,下列说法中正确的是
的烃,下列说法中正确的是
A.分子中至少有9个碳原子处于同一平面上
B.分子中至少有10个碳原子处于同一平面上
C.分子中至少有11个碳原子处于同一平面上
D.该烃属于苯的同系物
12.下列说法中,正确的是
A.室温下,CH3COOH分子不可能存在于pH>7的碱性溶液中
B.在c(H+)=c(OH-)的溶液中,AlO2-不可能大量存在
C.要NaAlO2溶液中,HCO3-离子不可能大量存在
D.在水溶液中石炭酸比碳酸容易电离
13.不久前,日本某一材料研究所的科学家发明了一种“碳纳米管温度计”,这种温度计被认定为世界上最小的温度计。研究人员在长约10-6m,直径为10-7m的碳纳米管中充人液态的金属镓。当温度升高时,管中的镓就会膨胀,通过电子显微镜就能读取温度值。这种温度计测量的范围可从18℃到490℃,精确度较高,所以它可用于检查电子线路是否异常,测定毛细血管的温度等许多方面。根据以上信息判断下列推测中不正确的是。
A.碳纳米管的体积在10℃至500℃之间随温度变化很小,可忽略不计
B.金属镓的熔点很低,沸点很高
C.金属镓的体积在10℃至500℃之间随温度变化比较均匀
D.金属镓的体积在10℃至500℃之间随温度变化很小,可忽略不计
14.1L某混合溶液中,溶质X、Y浓度都为0.1molL-l,向混合溶液中滴加某溶液Z(0.1molL-l氢氧化钠或硫酸溶液),所得沉淀的物质的量如图所示,则X、Y、Z分别是
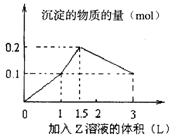
A.氯化铝、氯化铁、氢氧化钠 B.氯化铝、氯化镁、氢氧化钠
C.偏铝酸钠、氢氧化钡、硫酸 D.偏铝酸钠、氯化钡、硫酸
15.以铁为阳极,铜为阴极,对足量的NaOH溶液进行电解。一段时间后得到4mol Fe(OH)3沉淀,此间共消耗的水的物质的量为
A.8mol B.10mol C.11mol D.12mol
16.某溶液中含有HCO3-、SO32-、CO32-、CH3COO-等4种阴离子。若向其中加入足量的Na2O2后,溶液中离子浓度基本保持不变的是
A. CH3COO- B. SO32- C. CO32- D. HCO3-
17.关于氢键,下列说法正确的是
A.每一个水分子内含有两个氢键 B.冰和水中都存在氢键
C.分子间形成氢键使物质的熔点和沸点升高
D.水是一种非常稳定的化合物,这是由于氢键所致
18.取xg铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生8960mL的NO2气体和672mLN2O4的气体(都已折算到标准状态),在反应后的溶液中加足量的氢氧化钠溶液,生成沉淀质量为17.02g。则x等于
A.8.64g B.9.20g C.9.00g D.9.44g