08届高考理综化学第一次模拟考试
理科综合能力测试(化学部分)
相对原子质量:H-1 C-12 O-16 Na-23 S-16 Cu-64 Ag-108 Ba-137
一、选择题(每小题只有一个选项符合题意,每小题6分)
6.废旧的电池不可以随意丢弃,某同学希望将废旧的电池回收利用,他的以下想法不正确的是
A.把锌皮取下洗净用于实验室制取氢气
B.碳棒取下洗净用作电极
C.把铜帽取下洗净回收利用
D.废电池中的黑色糊状物含有氯化铵等物质,可作化肥
7.设NA为阿伏加德罗常数,下列说法正确的是
A.在含4molSi-O键的SiO2晶体中,氧原子的数目为4NA
B.标准状况下,等物质的量的NH3和SO3所含原子数都相等
C.12.5mL16mol/L浓硫酸与足量的铜反应,生成SO2的分子数约为6.02×1022
D.常温下含有NA个NO2、N2O4分子的混合气体,降温至标准状况下,其体积约为22.4L
8.下列离子方程式正确的是
A.将氯气通入水中:Cl2+H2O=Cl-+HClO+H+
B.常温下Al与浓硝酸反应:Al+6 H++3NO- 3=Al3++3NO2↑+3 H2O
C.氢氧化铁溶于氢碘酸中:Fe(OH)3+3H++I-=Fe2++I2+3 H2O
D.次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO
![]()
 9.我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂。某种兴奋剂的结构简式如右图所示,有关该物质的说法正确的是
9.我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂。某种兴奋剂的结构简式如右图所示,有关该物质的说法正确的是
A.该化合物的分子式为C14H10O10
B.该分子中的所有碳原子一定在同一平面上
C.遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物
D.1mol该物质分别与NaOH溶液和H2反应时,最多消耗NaOH和H2分别为8mol、6mol
10常温下,下列对各溶液的叙述,正确的是
A.10mL0.5mol/LCH3COONa溶液与6mL1mol/L盐酸混合后c(Cl-)>c(Na+)>c(OH-)>c(H+)
B.在0.1mol/LNH4Cl溶液中,c(H+)=c(NH3・H2O)+c(OH-)
C.某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A)
|
|
A.反应达到平衡时,若两种反应物的转化率相等,则起始投入的n(NH3): n(O2)=1:1
B.反应达到平衡后,再向体系中充入O2,将提高NH3的转化率
C.反应达到平衡时,若向体系中充入稀有气体,速率增大
D.当v正(NH3): v正(NO)=1:1时,说明该化学反应已经达到平衡
12.下列说法正确的是
A.丙烯的结构简式为CH3CHCH2
B.由SO2通入硝酸钡溶液产生白色沉淀可知,BaSO3不溶于硝酸
C.在中和滴定中,既可用标准液滴定待测液,也可用待测液滴定标准液
D.用酸性高锰酸钾溶液可以鉴别乙烯和乙炔
13.用铜做电极,电解某浓度的AgNO3和Cu(NO3)2的混合溶液,一段时间后,阴极上析出1.6gCu时,不考虑溶液体积变化,则下列叙述中正确的是
A.电路中流过0.05mol电子 B.溶液中c(Cu2+)降低
C.电解质溶液质量减少 D.阳极铜消耗了1.6g
26.(14分)A、B、C、D、E五种元素。A、B、C的电子层数之和为5,A、B能形成AB3分子。C、D同主族,D、E同周期。D的最外层电子数是E最外层电子数的2倍,E的最外层电子数与其核外电子层数相同。请填写下列空白:
⑴AB3的电子式为__________
⑵C、D两元素中非金属性较强的是_____(填元素名称),可以验证该结论的是____。
A.比较这两种元素的气态氢化物的沸点
B.比较这两种元素的单质在常温下的状态
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的单质化合所得产物中两元素的价态
⑶D、E两元素形成的化合物X能与水反应,所得产物能进一步与NaOH溶液反应,则1molX完全水解后,所得产物最多能消耗______molNaOH。
⑷为了除去B2DC4稀溶液中混有的B2DC3,常采用B2C2为氧化剂,发生反应的离子方程式为___________________________________________________________。
⑸在火箭推进器中装有液态A2B4和液态B2C2,已知0.4mol液态A2B4和足量液态B2C2反应,生成气态A2和气态B2C,放出256.6kJ的热量,则该反应的热化学方程式为_____________。
27.(14分)置换、化合、复分解是三种基本反应类型,而H2O在各种化学反应中扮演不同的“角色”。下面围绕水的各反应全部来自现行教材。下列问题所涉及的答案可能有多种,只需答出一种情况即可:
⑴H2O作反应物的置换反应
①____(填化学式)和H2O能在加热或高温条件下进行
②产生O2的反应,其化学方程式:___________________________________;
⑵H2O作生成物的置换反应:
加热条件下的置换,其反应物可是_________________(填化学式)
⑶水解反应
①气体产物可用焊接金属,其化学方程式:____________________________________。
②1分子的___________(填名称)水解之后有2分子同种物质生成。
⑷化合反应:
①有碱金属元素参与的三物质化合,其化学方程式:__________________________。
②有电子得失且三物质参与的化合,其产物的颜色与状态是_____________________。
28.(14分)实验室有一瓶Na2SO3固体,可能含有NaCl、Na2SO4、BaCl2、K2CO3、K2SO4中的一种或几种杂质,通过下列实验确定该样品的成分及Na2SO3的质量分数。
①取少量样品于试管中,加水振荡,未见沉淀生成;
②透过蓝色钴玻璃观察,焰色反应无紫色;
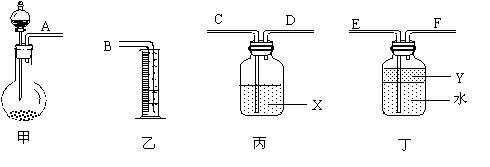 ③用下图所示仪器进行合理组装,测定产生气体的体积(SO2在硫酸中的溶解忽略不计)
③用下图所示仪器进行合理组装,测定产生气体的体积(SO2在硫酸中的溶解忽略不计)
请回答下列问题:
⑴按气流从左到右方向,正确的连接顺序为:A接___,___接____,____接B。
⑵利用所组装置,由分液漏斗向圆底烧瓶中滴加10mL水,将排入量筒中___mL液体。
⑶液体X是____________,其作用是______________________________。
⑷Y的作用是防止产生的气体溶于水,下列所给试剂符合要求的是______。
A.苯 B.四氯化碳 C.酒精 D.汽油
若称取样品3.00g,加入10.0mol/L的硫酸至过量(5mL),产生无色气体,排入量筒中液体的体积为229mL(标准状况)。
⑸对获得准确的气体体积无益的操作有_________(填序号)
①检查装置的气密性;
②连通乙、丁的导管要预先注满水;
③读数时视线与量筒内凹液面最低点相平;
④恢复到室温后再上下调整量筒位置,使乙、丁两液面相平;
⑤在甲装置胶塞上再连接一个导管,通入N2将系统中SO2全部排出。
⑹向逸出气体后的溶液中加入稍过量的BaCl2溶液,过滤、洗涤、干燥,得到白色沉淀13.98g。根据实验所得现象及数据,可知:样品中Na2SO3的质量分数是_____,含有的杂质是_______
___________。
29.(18分)有机物A、B、C、D、E、F均只含C、H、O三种元素,在一定条件下有以下转化关系:
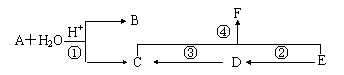 |
有以下信息可供参考:
①A分子中共有24个原子,其蒸气密度是相同状况下氢气密度的95倍。
②B分子含有苯环,苯环上有两个取代基;在加热条件下可与新制氢氧化铜悬浊液反应;与FeCl3溶液相遇不显紫色。
③A、B相对分子质量之差等于54。
根据你的推导,回答下列问题:
⑴A的分子式________;C的摩尔质量_______;E中官能团的名称_________________。
⑵反应①的类型是_________;反应②的类型是_________;
⑶D+Cu(OH)2反应的化学方程式_____________________________________;
反应④的化学方程式________________________________________。
⑷写出符合下列要求的B的同分异构体(不包括B本身);
①苯环上的一溴代物只有两种结构;②可发生银镜反应;③可与NaOH溶液反应。
_______________________________________________________。
参考答案
6.D7.B8.A9.D10.B11.B12.C13.C
 26.(14分;方程式每空3分,其它每空2分)
26.(14分;方程式每空3分,其它每空2分)
⑴ ⑵氧,C、D;⑶8;⑷H2O2+H2SO3=2H++SO2- 4+H2O
⑸N2H4(l)+2 H2O2(l)=N2(g)+4 H2O(g);△=-641.5kJ/mol
27.(14分;每空2分)本题答案有开放性,合理即可给分。
⑴①C(或Fe) ②2F2+2H2O=4HF+O2
⑵CuO(Fe2O3等其它合理答案也给分)
⑶①CaC2+2H2O=Ca(OH)2+C2H2↑ ②麦芽糖
⑷①Na2CO3+CO2+H2O=2NaHCO3 ②红褐色固体
28.(14分;第⑹问4分,其它每问2分)
⑴C、D、F、E; ⑵10;⑶浓硫酸,干燥SO2 ⑷A、D
⑸⑤ ⑹42%(或0.42);NaCl、Na2SO4
29.(18分;第⑵问每空1分,第⑶问每空3分,其它问每空2分)
⑴C11H10O3; 72g/mol;碳碳双键、羟基
⑵水解(或取代)反应;氧化反应
⑶CH2=CH-CHO+2Cu(OH)2 CH2=CH-COOH+Cu2O+2H2O
 |
CH2=CH-COOH+CH2=CH-CH2OH CH2=CH-COOCH2-CH=CH2+H2O
 |
⑷