选择题训练(3)
一、选择题(每小题只有一个正确答案,每小题4分,共32分)
1.某矿泉水标签上印有主要的矿物质成分如下(单位mg/L):Ca: 20, K: 39 , Mg: 3.0 Zn: 0.06 , F: 0.02 等。这里的Ca、K、Mg、Zn、F是指:
A.单质 B.元素 C.金属离子 D.分子
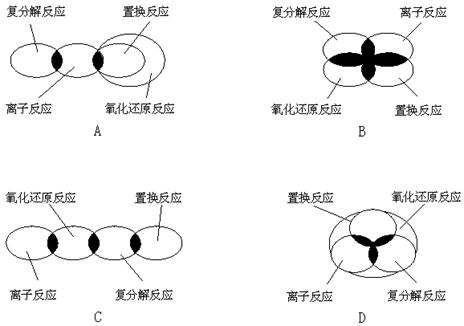
2.离子反应、复分解反应、置换反应和氧化还原反应之间用集合关系可表示为:A
3.工矿企业必须严格执行关于“三废”排放标准,并且尽可能地把“三废”变成有用的副产品,否则将会严重地污染环境。下列有关工业生产中的“三废”因任意排放,可能导致“光化学污染”的是:
A.硫酸工业废气 B.工业生产硝酸的尾气
C.工业电镀锌的废水 D.火力发电厂的废渣
4.下列变化能显著放热的是:
A.Ba(OH)2·8H2O晶体和NH4Cl晶体的反应 B.Na2O2与H2O的反应
C.灼热的碳与二氧化碳的反应 D.NH4NO3晶体溶于水
5.下列实验需使用温度计的是:
A.实验室蒸馏石油 B.用浓盐酸制氯气
C.实验室制乙炔 D.结晶硫酸铜结晶水含量的测定
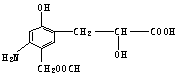 6.分析有机物的结构
6.分析有机物的结构
应具有的性质是:①缩聚反应 ②加成反应 ③取代反应 ④水解反应 ⑤中和反应 ⑥显色反应 ⑦氧化反应 ⑧还原反应 ⑨消去反应:
A.只③⑤⑥⑦ B.只④⑤⑥⑦
C.全部 D.除①④外其余都有
7. 1
mol有机物 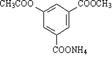 与足量NaOH 溶液充分反应,消耗NaOH 物质的量为:
与足量NaOH 溶液充分反应,消耗NaOH 物质的量为:
A.5 mol B.4 mol C.3 mol D.2 mol
8. 某种氯化镁晶体有24Mg2+、35Cl–、37Cl–、三种离子组成,在熔融状态下,使1mol这种氯化镁完全电解,测得产生的气体质量为同体积氧气质量的2.22倍。则这种氯化镁晶体中35Cl–与37Cl–与的物质的量之比为:
A.1:2 B.2:3 C.1:3 D.3:1
二、选择题(每小题4分,10小题共40分,每小题有一个或两个正确选项。)
9.下列比较正确的是:
A.熔沸点高低:NH3<PH3<AsH3<HI
B.离子半径大小:Br-<Mg2+<Cl-<F-
C.分散质微粒直径大小:Fe(OH)3胶体>NaCl溶液
D.酸性强弱:H2SO3>CH3COOH>H2CO3>H2SiO3
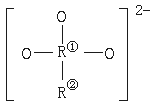
10.某盐Na2R2O3·5H2O遇酸分解,具有还原性,R2O![]() 的结构如图所示。其中两个R处于不同的价态,则R①和R②的价态分别是:
的结构如图所示。其中两个R处于不同的价态,则R①和R②的价态分别是:
A.+3,-1 B.+6,-2 C.+4,-1 D.-3,+1
11.1mol X气体跟a mol Y气体在体积可变的密闭容器中发生如下反应:
X(g)+a Y(g)![]() b Z(g) 反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是:
b Z(g) 反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是:
A、a=1,b=1 B、a=2,b=1 C、a=2,b=2 D、a=3,b=2
12. 用NA表示阿伏加德罗常数,则下列说法错误的是:
A.1 molCH5+所含的电子数为10NA B.1 molC20H42中含有61 NA个共价键
C.25℃时1 mL纯水中含有10–10NA个OH–离子 D.22.4 L的NH3中含有4 NA个原子
13. 用1kg溶剂中所含溶质的物质的量表示的溶液的浓度叫质量物质的量浓度,其单位是mol/kg。某物质的溶液的质量分数为1.96%,质量物质的量浓度为0.2 mol/kg,则该物质可断为:
A.NaHCO3 B.CaCO3 C.KHCO3 D.Na2CO3
14. 酸式盐NaHB在水溶液中,HB–的电离程度小于HB–的水解程度,下列说法正确的是:
![]() A.HB–水解方程式:HB–+H2O H3O++B2–
A.HB–水解方程式:HB–+H2O H3O++B2–
B.溶液中离子浓度大小为:c (Na+)>c(HB–)>c(OH–)>c(H+)
C.NaHB的存在抑制了水的电离
D.相同物质的量浓度溶液的pH值:Na2B>NaHB
15.体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2![]() 2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率:
2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率:
A、等于p% B、大于p% C、小于p% D、无法判断
16.某盐酸的浓度为12.0 mol·L-1,其密度为1.19 g·cm-3。现有该浓度的盐酸100 m3,则用于吸收HCl形成该盐酸的水的体积是:
A.75.2 m3 B.85.5 m3 C.90.8 m3 D.100 m3
17.某化工厂工业废水中含H2SO4的质量分数为1%,采用边排放边中和的方法将它处理使之基本呈中性,处理方法如图所示。若处理后废水pH=7,则1%NaOH溶液的流量为:A
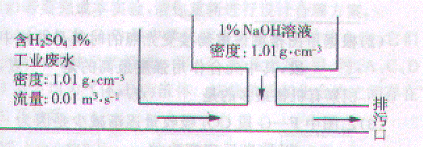
A.0.00816 m3/s B. 0.01 m3/s C.0.01632 m3/s D.0.02 m3/s
18.质量分数不等的两种硫酸钠溶液等质量混合时,其质量分数为a %,而等体积混合后的质量分数为b %;质量分数不等的两种乙醇溶液等质量混合时,其质量分数为a %,,而等体积混合后的质量分数为c %。则a、b、c的大小关系正确的是:
A.a>b>c B. b>a>c C. c>a>b D. c>a>b