08届高考化学复习有机化学模拟练习题一
注意事项:
1.第I卷46分,第II卷54分,共120分,考试时间为100分钟。
2.请将答案统一填写在答题纸上。可能用到的相对原子质量:
H—1 C—12 N—14 O—16
可能用到的相对原子质量:H—1 C—12 O—16 N—14 Na—23 K—39 I-127
第Ⅰ卷(共46分)
一、选择题(本题包括8小题,每小题2分,共16分。每小题只有一个选项符合题意)
1、下列各组物质中,全部属于纯净物的是
A、福尔马林、汽油、食醋 B、二甲苯、蔗糖、花生油
C、甘油、氯仿、无水酒精 D、淀粉、天然气、电石气
2、下列有机物分子中有三种不同的氢原子,且氢原子个数之比为3 ∶2 ∶1的是
A、CH3CHO B、CH3COOC2H5 C、CH3COOH D、CH3CH2OH
3、有机物 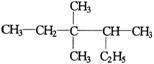 的正确命名为
的正确命名为
A、3,3,4—三甲基已烷 B、3,3—二甲基-4-乙基戊烷
C、2—乙基—3,3-二甲基—4—乙基戊烷 D、2,3,3—三甲基已烷
4、下列取代基或微粒中,碳原子都满足最外层为8电子结构的是
A、乙基(—CH2CH3) B、碳化钙 (CaC2)
C、碳正离子[(CH3)3C + ] D、碳烯 ( : CH2 )
5、不洁净玻璃仪器洗涤方法正确的是
A、做银镜反应后的试管用氨水洗涤
B、盛装醋酸的试剂瓶用酒精洗涤
C、盛装苯酚后的试管用盐酸洗涤
D、盛装油脂的试剂瓶用热的纯碱溶液洗涤
6、有机物A和B,只由C、H、O两种或三种元素组成,相同物质的量的A和B完全燃烧时,消耗氧气的物质的量相等,下列对A、B的判断错误的是
A、A与B互为同分异构体
B、与B的分子组成相差n个“CH2”
C、A与B的分子组成相差n个“CO2”
D、A与B的分子组成相差n个“H2O”
7、乙酸与2.0g 某饱和一元醇A反应,生成酯3.7g,并回收到A 0.4g,则A的相对分子质量为
A.32 B.46 C.60 D.74
8、有机物A(![]() )的同分异构体中属于酚类的结构有
)的同分异构体中属于酚类的结构有
A、6种 B、7种 C、8种 D、9种
二、选择题(本题包括10小题,每小题3分,共30分。每小题只有一个选项符合题意)
9、按反应特征与产物的结构关系,有机反应大致可分为:取代反应、消去反应、加成反应三种,下列变化中不属于取代反应的是
A、C6H5CH2Cl+NaCN —→ C6H5CH2CN+NaCl
B、2Na +2 C2H5OH—→ 2C2H5ONa + H2↑
C、CH3CH2CHO+HCN —→ CH3CH2CH(CN)OH
D、CH3COOC2H5+H2O —→ CH3COOH+C2H5OH
10、已知甲醛(![]() )分子中的四个原子是共平面的.下列分子中所有原子不可能同时存在同一平面上的是
)分子中的四个原子是共平面的.下列分子中所有原子不可能同时存在同一平面上的是
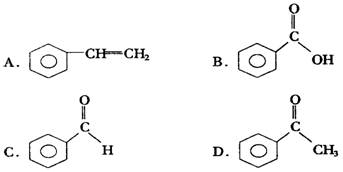
11、有机物分子中的原子(团)之间会相互影响,导致相同的原子(团)表现不同的性质。下列各项的事实不能说明上述观点的是
A、甲苯能使酸性高锰酸钾溶液褪色,而甲基环己烷不能使酸性高锰酸钾褪色
B、乙烯能与溴水发生加成反应,而乙烷不能发生加成反应
C、苯酚与溴水可直接反应,而苯与液溴反应则需要铁作催化剂
D、苯酚可以与NaOH反应,而乙醇不能与NaOH反应
12、将 ![]() 和
和![]() (甘油)以一定比例混合,测得混合物含碳51.3%,那么氧元素的质量分数是
(甘油)以一定比例混合,测得混合物含碳51.3%,那么氧元素的质量分数是
A、40% B、35% C、30% D、无法计算
13、最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”——全氟丙烷(C3F8),并提出用其“温室化火星”使其成为第二个地球的计划。有关全氟丙烷的说法不正确的是
A、分子中三个碳原子不可能处于同一直线上
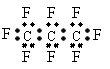 B、相同压强下,沸点:C3F8>C3H8
B、相同压强下,沸点:C3F8>C3H8
C、全氟丙烷的电子式为:
D、全氟丙烷分子中既有极性键又有非极性键
14、“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂。其中没食子儿茶素(EGC)的结构如下图所示。关于EGC的下列叙述中不正确的是
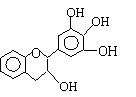 A、分子中所有的原子不可能共平面
A、分子中所有的原子不可能共平面
B、1molEGC与4molNaOH恰好完全反应
C、易发生氧化反应和取代反应,难发生加成反应
D、遇FeCl3溶液发生显色反应
15、将淀粉水解,并用新制的氢氧化铜检验其水解产物的实验中,要进行的主要操作是:①加热、②滴加稀硫酸、③加入新制的氢氧化铜悬浊液、④加入足量的氢氧化钠溶液。以上各步操作的正确排序是
A、①→②→③→④→① B、②→①→④→③→①
C、②→④→①→③→① D、③→④→①→②→①
16、下列化学方程式或离子方程式中正确的是
A、金属钠加入无水乙醇中:Na + C2H5OH → C2H5ONa + H2↑
B、过量的乙酸跟Na2CO3溶液反应:2H+ + CO32— = H2O + CO2↑
C、溴乙烷在NaOH水溶液中加热:
CH3CH2Br + NaOH →CH2=CH2↑+NaBr + H2O
![]() D、苯酚钠溶液中通入CO2:
D、苯酚钠溶液中通入CO2:
17、分子式为C10H20O2有机物A,能在酸性条件下水解生成有机物C和D,且C在一定条件下可转化成D,则A的可能结构有
A、2种 B、3种 C、4种 D、5种
18、晚会上,常见到观众手持常被称为“魔棒”的荧光棒给晚会助兴,“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式为:
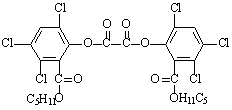
下列有关说法正确的是 ( )
A、草酸二酯属于高分子化合物
B、草酸二酯属于芳香族化合物
C、1mol草酸二酯与氢氧化钠稀溶液反应(苯环上卤素不水解),最多消耗4molNaOH
D、1mol草酸二酯与氢气完全反应,需要氢气10mol
有机化学综合练习一答题卷
一、二、选择题(共46分)
| 题 号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 答 案 | |||||||||
| 题 号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |
| 答 案 |
第Ⅱ卷(共54分)
三、实验题 (共18分)
19.(4分)下列叙述正确的是________________(选对一个给2分,多选、错选一个扣1分,本题不出现负分)。
A.不慎把苯酚溶液沾到了皮肤上,应立即用大量水冲洗。
B.甲、乙两种有机物具有相同的相对分子质量和不同结构,则甲和乙一定是同分异构体。
C.浓溴水滴入苯酚溶液中立即产生2,4,6-三溴苯酚的白色沉淀。
D.溴的苯溶液中加少量铁粉后会剧烈反应,并放出大量的热,但该现象不能说明苯和溴的取代反应就是放热反应。
E.分离沸点相差30℃以上的混溶液体,应采用的方法是分馏
F.实验室使用体积比为1:3的浓硫酸与乙醇的混合溶液制乙烯时,为防加热时反应混合液出现暴沸现象,除了要加沸石外,还应注意缓慢加热让温度慢慢升至170℃。
G.除去混在苯中的少量苯酚,加入过量溴水,过滤。
20. (14分)为探究实验室制乙烯及乙烯和溴水的加成反应。甲同学设计了如图所示的实验装置,并进行了实验。当温度升至170℃左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速褪去。甲同学认为达到了实验目的。
乙同学仔细考察了甲同学的整个实验过程,发现当温度升到100℃左右时,无色液体开始变色,到160℃左右时,混合液全呈黑色,在170℃超过后生成气体速度明显加快,生成的气体有刺激性气味。由此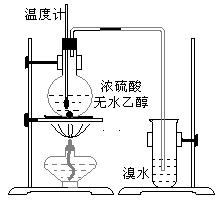 他推出,产生的气体中应有杂质,可能影响乙烯的检出,必须除去。据此回答下列问题:
他推出,产生的气体中应有杂质,可能影响乙烯的检出,必须除去。据此回答下列问题:
(1)写出甲同学实验中两个反应的化学方程式:
____________________________________、
____________________________________。
(2)乙同学观察到的黑色物质是__________,刺激性气体是__________。乙同学认为刺激性气体的存在就不能认为溴水褪色是乙烯的加成反应造成的。
原因是(用化学方程表示):__________________。
(3)丙同学根据甲乙同学的分析,认为还可能有CO、CO2两种气体产生。为证明CO存在,他设计了如下过程(该过程可把实验中产生的有机产物除净):发现最后气体经点燃是蓝色火焰,确认有一氧化碳。
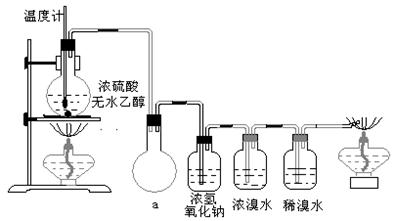
①设计装置a的作用是_____________________________________________
②浓溴水的作用是_________________________________________________,
稀溴水的作用是___________________________________________________。
四、填空题。(共22分)
21.(8分)按要求完成下列问题
(1)甲基的电子式________ _____
(2)通式为CnH2n+2的最简单同系物的分子式
(3)相对分子质量为72且沸点最低的烷烃的结构简式 ___________________
(4)一氯甲烷的电子式为
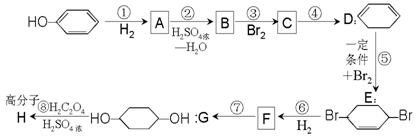 22.(14分)按以下步骤可从
22.(14分)按以下步骤可从![]() 合成
合成![]() (部分试剂和反应条件已去).
(部分试剂和反应条件已去).
请回答下列问题:
(1)B、F的结构简式为:B F 。
(2)反应①~⑦中属于消去反应的是 (填代号)。
(3)根据反应![]() ,写出在同样条件下
,写出在同样条件下
CH2=CH—CH=CH2与等物质的量![]() 发生加成反应的化学方程式:
发生加成反应的化学方程式:
。
(4)写出第④步![]() 的化学方程式(有机物写结构简式,注明反应条件).
的化学方程式(有机物写结构简式,注明反应条件).
。
(5)A—G这七种有机物分子中含有手性碳原子的是(填序号) 。
(6)核磁共振谱是测定有机物分子结构最有用的工具之一。在有机物分子中,不同位置的氢原子在质子核磁共振谱(PMR)中给出的峰值(信号)也不同,根据峰(信号)可以确定有机物分子中氢原子的种类和数目。例如:乙醛的结构式为: 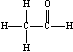 ,其PMR谱中有2个信号峰,其强度之比为3∶1。则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1∶1∶2的是
。
,其PMR谱中有2个信号峰,其强度之比为3∶1。则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1∶1∶2的是
。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
五、计算题(共14分)
23.一种气态烷烃和一种气态烯烃的混合物共10g,平均相对分子质量为25。使混合气通过足量溴水,溴水增重8.4g。通过计算回答:
① 混合物的物质的量为_________________
② 混合物中的各组分的分子式为______________________________,体积之比为___________________________
24.现有A、B两种链状饱和一元醇的混合物0.3 mol,其质量为13.8g。已知①A和B碳原子数均不大于4,且A<B;②A和B分子中均不含有支链,且都能被催化氧化生成醛。
(1)混合物中A可能的分子式 ;B可能的分子式 。
(2)若n(A):n(B)=1:1时,
A的名称 B的名称 。
(3)若n(A):n(B)≠1:1时,
A的结构简式为 ;
B的结构简式为 。
则 n(A)∶n(B) = 。
有机化学模拟练习一参考答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 答案 | C | D | A | B | D | B | A | D | AD | D | B | A | C | B | B | D | C | B |
三、实验题 (共18分)
19.(4分)DE (选对一个给2分,多选、错选一个扣1分,本题不出现负分)
20.(14分)
(1) CH3CH2OH ![]() CH2==CH2↑ + H2O
CH2==CH2↑ + H2O
CH2==CH2 + Br2
![]() Br-CH2CH2-Br
(2×2分)
Br-CH2CH2-Br
(2×2分)
(2) C(1分) SO2 (1分) Br2 + SO2 + 2H2O == 2HBr + H2SO4 (2分)
(3)①安全装置,防倒吸(2分)
②吸收乙烯、二氧化硫气体(2分) 检验乙烯、二氧化硫气体是否除净(2分)
![]()
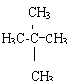 四、填空题。(共22分)
四、填空题。(共22分)
21.(8分,每空2分) (1) (2)CH4 (3)
![]() (4)
(4)
22.(14分)(每空2分)
(1)![]() ;
;
(2)② ④;
(3)![]() ;
;
(4)![]() (其它正确写法也得分);
(其它正确写法也得分);
(5)C E;
(6)BD
五.计算题(共14分)
23.0.4 mol (2分) CH4 C2H4 比为1∶3 (4分)
24.(1)CH4O(1分);C3H8O或C4H10O (1分) (2)甲醇(1分);丙醇(1分);
(3)CH3OH(2分);CH3CH2CH2CH2OH(2分);2∶1(2分)。
