08届高考理科综合二模化学部分试题
6.化学基本概念是学习化学的基础,判断下列有关化学基本概念的依据正确的是 ( )
A.胶体:是否有丁达尔现象
B.氧化还原反应:元素化合价是否变化
C.电解质和非电解质:溶于水或熔融状态下能否导电
D.同分异构体:是否具有相同的相对分子质量和不同的结构
7.假设体积可以相加,下列叙述正确的是 ( )
A.0.2 mol・L-1的盐酸,与等体积水混合后pH=1
B.pH=3的醋酸溶液,稀释至10倍后pH=4
C.95 ℃纯水的pH<7,说明加热可导致水呈酸性
D.pH=3的醋酸溶液,与pH=11的氢氧化钠溶液等体积混合后pH=7
8.用NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.71g氯气与足量的铁粉完全反应,转移的电子数为2NA
B.78g过氧化钠固体中,阴阳离子总数为4NA
C.标准状况下,2.24LCCl4所含的分子数为0.1NA
D.1 mol甲基(-CH3)所含的电子数为10NA
9.在标准状况下,将5.6 L CO2气体与250 mL 1 mol/L NaOH溶液充分反应,所得溶液pH=8.3,下列关系式中正确的是 ( )
A. c(Na+)+c(H+)=c(HCO-3)+c(CO2-3 )+c(OH-)
B. c(Na+)=c(HCO-3)+2c(CO2-3 )
C. c(Na+)>c(HCO-3)>c(OH-)>c(H+)
D. c(HCO-3)>c(Na+)>c(H+)>c(OH-)
10. 质量分数为ω的NaOH溶液,其物质的量浓度为a mol・L-1,加热蒸发水份使其质量分数变为2ω,此时,该溶液中NaOH的物质的量浓度为b mol・L-1,则a与b的关系正确的是 ( )
A.b=2a B.a=2b C.b<2a D.b>2a
11.美国天文学家在亚利桑那州一天文观察台探测到了银河系中心2.6万光年处一巨大气云中的特殊电磁波,这种电磁波表明那里可能有乙醇醛糖分子存在。下列有关乙醇醛糖(HOCH2CHO)的有关说法不正确的是 ( )
A.乙醇醛糖是一种有机物,易溶于水
B.乙醇醛糖能发生取代反应、消去反应、氧化反应以及还原反应
C.乙醇醛糖与甲酸甲酯互为同分异构体
D.1 mol 乙醇醛糖与足量的银氨溶液作用,可析出2molAg
12. 右图中,两电极上发生的电极反应为:a极:Cu2+ + 2 e-= Cu b极:Fe - 2 e-= Fe2+
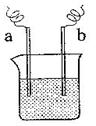 下列说法中不正确的是
( )
下列说法中不正确的是
( )
A.该装置可能是电解池
B.a极上一定发生还原反应
C.a、b可能是同种电极材料
D.该过程中能量的转换一定是化学能转化为电能
![]() 13.一定条件下,在密闭容器中存在如下反应:
13.一定条件下,在密闭容器中存在如下反应:
若改变某一个条件,而其他条件不变,对下述图像的描述正确的事 ( )
A、图像Ⅰt0时刻升高了体系的温度 B、图像Ⅰt0时刻向容器内充入了CO气体
C、图像Ⅱt0时刻一定增大了容器的压强 D、图像Ⅲ中,甲容器的温度高于乙容器的温度

26. (12分)同学们,我们学习过的化学反应有很多了,让我们对所学过的化学反应方程式做个总结吧!有一些化学反应可用下式表示
A + B ─→ C + D + H2O
请你根据下面的提示回答下列问题:
(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式: 。
(2)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B的组合是 。
(3)若A为Na2O2,B为硫酸,则C和D的化学式是 。
(4)若A、C均含有铝元素。则C可能是 。写出一个符合这个反应的化学方程式: 。
(5)若A为单质,B为第二周期某种元素的最高价氧化物的水化物,请写出符合上式的化学方程式: 。
27. (14分) A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,D与F为同一周期,A与D、C与F分别为同一主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为 ,其分子属于 (填“极性”、“非极性”)分子。D与C形成的化合物D2C2可与Y反应生成单质C,该反就的化学方程式为: 。
(2)E是非金属元素,其单质在电子工业中有重要应用,请写出工业生产单质E的化学反应方程式: 。
(3)一定条件下,A的单质气体与B的单质气体充分反应生成6.8g W气体(已知n(A):n(B)=3:1),可放出18.44 kJ热量,则该反应的热化学方程式
。W的空间构型为: 。
(4)A的单质与C的单质在KOH的浓溶液中可以形成原电池,如果以金属M和金属N为惰性电极,在电池的M极通入A的单质气体,N极通入C的单质气体,则M极的电极反应式为 。
(5)在10升的密闭容器中,通入2mol的FC2气体和3molC的气体单质,一定条件下反应后生成FC3气体,当反应达到平衡时,单质C的浓度为0.21mol/L,则平衡时FC2的转化率为 。
28.(17分)铁是日常生活中最常见的金属,某班同学在学习铁的知识时,有下列问题:
问题1:铁为何称为黑色金属?
问题2:同学们查资料得知CuO高温可以分解为Cu2O和O2,于是同学们提出问题“Fe2O3高温可以分解为FeO和O2吗?”
(1)对于问题1,同学们上网查寻,有两种解释:
A、因为在铁表面上有黑色的铁的氧化物,所以叫黑色金属。
B、因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属。
①你认为正确的说法是 。
②若有一黑色粉末,你如何鉴别是铁粉,还是Fe3O4粉末。
③若有一黑色粉末,为铁和四氧化三铁的混合物,你如何证明其中有Fe3O4(只要求简述实验方法)。
(2)对于问题2,同学们准备实验探究,他们设想了两种方法:
A:将三氧化二铁高温灼烧,看灼烧前后颜色是否变化。
B:将三氧化二铁高温灼烧,看灼烧前后质量是否变化。
①实验中应将Fe2O3放在 (填仪器名称,下同)中灼烧。冷却时应放在 中。
②方法A中,同学们认为:“如果高温灼烧后颜色由 变为 ,则说明Fe2O3确实发生了变化”。你认为能说明生成的一定为FeO吗? ,理由是 。
③方法B中,如果发生了预期的反应,固体高温灼烧前后质量比应为 ,
但是,实验结果固体灼烧前后质量比为30 :29,则高温灼烧后生成物是 。
④比较两种方法,你认为较可靠的方法是 。
29. (17分)某有机物M只含有C、H、O三种元素,有玫瑰香气的无色液体,用于配制香皂、日用化妆品香精, M的球棍模型如下图所示:
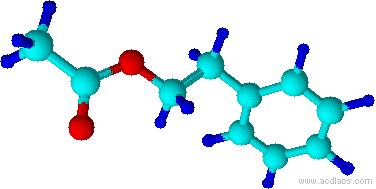
(1)请写出物质M的分子式______________________;
(2)M在一定条件下,可以发生水解反应,生成A、B两种物质,A为芳香族化合物。写出由A和B成M的化学方程式:
(3)已知A有如下转化:
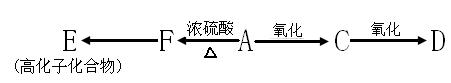
①写出E的结构简式 ;A→F属于______反应(填反应类型);
②写出C发生银镜反应的化学方程式: ;
(4)①D的同分异构体很多,其中属于酯类的芳香酯有 种。
②若D的同分异体的以下结构和性质特点:a. 与FeCl3溶液显紫色;b. 发生银镜反应
c. 苯环上只有2个取代基;请写出具有下列条件的全部同分异构体的结构简式:
化学部分参考答案及评分标准
6.B7.A8.A9.C10.D11.B12.D13.A
26. (12分)(1)Cl2+2OH-=Cl-+ClO-+H2O (2分) (2)C、浓H2SO4 (2分)
(3)Na2SO4、O2 (2分)
(4)AlCl3、或NaAlO2 (2分)
AlCl3+4NaOH=NaAlO2+3NaCl+2H2O
或NaAlO2+4HCl=AlCl3+3NaCl+2H2O (2分)(其他合理答案也可)
(5)C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O (2分)
CO2↑+4NO2↑+2H2O (2分)
(或:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,
3Cu+8HNO3(稀)![]() 3Cu(NO3)2+2NO↑+4H2O,其他合理答案也可)
3Cu(NO3)2+2NO↑+4H2O,其他合理答案也可)
27. (14分)(1)![]() (2分),极性(1分)
(2分),极性(1分)
2Na2O2+2H2O=4NaOH+O2↑(2分)
(2)SiO2+
2C ![]() Si
+ 2CO↑(未配平不得分,条件不写得1分,下同)(2分)
Si
+ 2CO↑(未配平不得分,条件不写得1分,下同)(2分)
(3)N2(g)+3H2(g)
![]() 2NH3(g);ΔH=-92.2KJ/mol (2分)三角锥形(1分)
2NH3(g);ΔH=-92.2KJ/mol (2分)三角锥形(1分)
(4)H2+ -2e+2OH-=2 H2O(2分)(5) 90%(2分)
28. ⑴ ① A (1分)
②取黑色粉末少许于试管中,加适量稀盐酸或稀硫酸,有气泡产生的原黑色粉末为铁,若无气泡产生则原粉末为Fe3O4(2分,其它合理答案亦可)
③用干燥的氢气与黑色粉末加热反应,用无水硫酸铜检测有水产生或用纯净的一氧化碳与与黑色粉末加热反应,用澄清石灰水检测有二氧化碳产生(2分,其它合理答案亦可)
(2)①坩埚(1分) 干燥器(1分)
②红棕色(1分)黑色(1分)。不能(1分),也可能为Fe3O4(2分)
③10/9(2分) ,Fe3O4(2分)
④B(1分)
29. (1)C10H12O2(2分)
(2)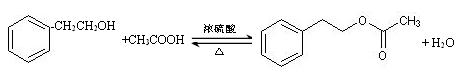 (2分)
(2分)
(3) ①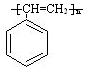 (2分) 消去 (1分)
(2分) 消去 (1分)
②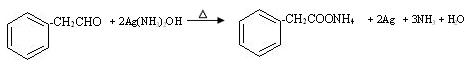 (2分)
(2分)
(4) ① 6 (2分)
② 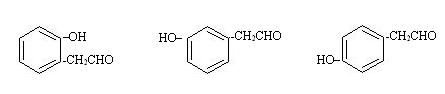 (各2分)
(各2分)