第2课时 常见物质的实验室制法(A卷)
考测点导航
1.常见气体的实验室制法是高考的重点内容,它包括所用试剂、反应原理、仪器装置和收集方法。
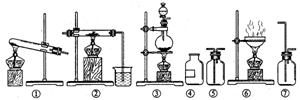 |
中学教材中按反应物的状态及反应条件可将气体制备分为五组:
![]()
![]() (1)固+固 气组:有O2、NH3等;
(1)固+固 气组:有O2、NH3等;
![]()
![]() (2)固+液 气组:有H2、O2、CO2、NH3、H2S、SO2、NO2、C2H2等;
(2)固+液 气组:有H2、O2、CO2、NH3、H2S、SO2、NO2、C2H2等;
(3)固+液 气组:有Cl2、HCl、NO等;
(4)液+液 气组:有C2H4和CO等。
(5)能用启普发生器制取的气体有:H2、CO2、H2S等。
要求熟练掌握以上各种气体的制取所需药品、化学原理、装置简图、净化方法、检验和操作注意事项。
2.实验装置的安装顺序:
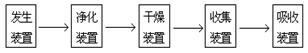
3.几种重要的无机物和有机物的制备:氢氧化铝、氢氧化亚铁、绿矾晶体、Fe(OH)3溶胶、溴乙烷、乙酸乙酯、肥皂、脲醛树脂等。
4.制备物质的合理方案的选用原则:原理正确、步骤简单、原料易得、节省原料、易于分离提纯、污染少。如制备CuSO4、Cu(NO3)2、Al(OH)3等有多种方案,但最佳方案只有一种。
典型题点击
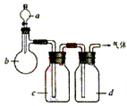 1.(2003年江苏、广东高考题) 拟用下图装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。
1.(2003年江苏、广东高考题) 拟用下图装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。
| 气体 | a | b | c | d |
| C2H4 | 乙醇 | 浓H2SO4 | NaOH溶液 | 浓H2SO4 |
| Cl2 | 浓盐酸 | MnO2 | NaOH溶液 | 浓H2SO4 |
| NH3 | 饱和NH4Cl溶液 | 消石灰 | H2O | 固体NaOH |
| NO | 稀HNO3 | 铜屑 | H2O | P2O5 |
(1)上述方法中可以得到干燥、纯净的气体是 。
(2)指出不能用上述方法制取的气体,并说明理由(可以不填满)
①气体 ,理由是 。
②气体 ,理由是 。
③气体 ,理由是 。
④气体 ,理由是 。
(本题重在考查制备气体的反应条件、气体的干燥及净化方法的选择。答题时必须全面分析、理解所给的装置意图,结合学过的实验基本操作知识,才能作出正确的选择。)
2.欲制无水氯化铝并保存备用。现有仪器如下图所示,并有铝粉、二氧化锰、水、2mol·L-1盐酸、11.9 mol·L-1盐酸、1.5 mol·L-1硫酸、固体烧碱、食盐晶体八种试剂。
设计的制取过程是:制氯气 → 加以净化和干燥氯气 → 制氯化铝
请回答下列问题:
(1)从上列仪器中选取必须的几种,连接成一个制无水氯化铝的连续装置,按前后顺序填写图的编号(不一定填满),并写出各仪器里放入的试剂的化学式。
仪器编号 、 、 、 、 ;
放入试剂 、 、 、 、 ;
(2)写出实验过程中有关反应的化学方程式
。
(该题着重考查物质制备的反应条件、原理、净化方法、尾气处理方法以及装置特征。答题时注意由反应原理正确选择试剂,按制取过程要求综合考虑、理解所给的装置,并作出判断和筛选。)
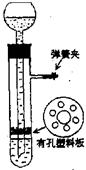 3.用图示的装置制取氢气,在塑料隔板上放粗锌粒,漏斗和带支管的试管中装有稀硫酸,若打开弹簧夹,则酸液由漏斗流下,试管中液面上升与锌粒接触,发生反应。产生的氢气由支管导出;若关闭弹簧夹,则试管中液面下降,漏斗中液面上升,酸液与锌粒脱离接触,反应自行停止。需要时再打开弹簧夹,又可以使氢气发生。这是一种仅适用于室温下随制随停的气体发生装置。
3.用图示的装置制取氢气,在塑料隔板上放粗锌粒,漏斗和带支管的试管中装有稀硫酸,若打开弹簧夹,则酸液由漏斗流下,试管中液面上升与锌粒接触,发生反应。产生的氢气由支管导出;若关闭弹簧夹,则试管中液面下降,漏斗中液面上升,酸液与锌粒脱离接触,反应自行停止。需要时再打开弹簧夹,又可以使氢气发生。这是一种仅适用于室温下随制随停的气体发生装置。
回答下面问题:
(1)为什么关闭弹簧夹时试管中液面会下降?
(2)这种制气装置在加入反应物前,怎样检查装置的气密性?
(3)从下面三个反应中选择一个可以用这种随制随停的制气装置制取的气体,填写下表中的空白。
①大理石与盐酸反应制取二氧化碳
②用二氧化锰催化分解过氧化氢制氧气
③浓硫酸与无水乙醇反应制乙烯
| 气体名称 | 收集方法 | 检验方法 |
(4)二氧化锰与浓盐酸制取氯气能否用这种装置随制随停。试说明理由。
(本题考查制气装置的工作原理。答题时要认真阅读题给信息、理解和运用信息,由仪器工作时观察到的现象领会随制随停的原理。)
新活题网站
1.下列反应适用于实验室制氢气的( )
①锌与稀硫酸反应 ②甲烷热分解 ③电解稀硫酸 ④赤热的炭与水蒸气反应
A.只有① B.①② C.①③ D.①②④
(该题意在考查对实验室制氢气掌握情况。答题时既要根据反应原理,又要考虑实验室制气体多方面要求,切不可生搬硬套课本知识。)
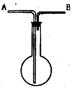
2.右图是为采用排空气法收集气体而设计的装置。它可以正置(如图)也可倒置,气体可以从A管也可以从B管导入,完全可据实验需要确定。若以此装置分别收集下列气体,其中所集得气体纯度最低的是( )
A.H2 B.CO C.O2 D.CO2
(此题考查学生对排空气法原理的理解程度。答题时要分析待收集气体对空气的相对密度大小及进气口。)
3.实验室中准备有以下主要仪器及用品,大试管、带导管的单孔塞、药匙、镊子、水槽、集气瓶、玻璃片、酒精灯、铁架台,如果药品选用合理,用以上仪器用品,能制取( )
A.氧气 B.氢气
C.氢气和二氧化碳 D.氢气、氧气、二氧化碳
(本题考查学生对常见气体的发生和收集装置是否熟悉。答题时要全面考虑,不能以偏概全。)
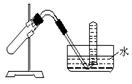 4.右图装置可用于( )
4.右图装置可用于( )
A.加热NaHCO3制CO2
B.加热硝酸铅制取二氧化氮
C.用Cu和稀HNO3反应制NO
D. 用NH4Cl与浓NaOH溶液反应制NH3
(本题考查学生对有关气体制备基础知识的掌握情况。答题时要对每个选项由发生到收集装置,逐个分析确定。)
5.由下列实验方法可以制取纯净物的是( )
A.石油减压分馏制汽油 B.蔗糖水解制葡萄糖
C.乙烯与氯化氢加成制氯乙烷 D.油脂水解制高级脂肪酸
(该题旨在考查物质制备的相关知识。答题时由发生的反应条件、程度及产物多方面共同确定。)
6.在如图所示的实验装置中,当A、B、C分别为以下不同组合的物质时,回答有关问题。
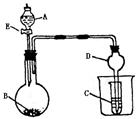 (1)当A为醋酸、B为贝壳(粉状)、C为C6H5ONa溶液时,小试管中的现象是
,其中发生的化学反应方程式是
(1)当A为醋酸、B为贝壳(粉状)、C为C6H5ONa溶液时,小试管中的现象是
,其中发生的化学反应方程式是
;
(2)当A为食盐水、B为电石、C为KMnO4溶液时,小试管中的现象是 ;A和B反应的方程式是 。
(3)当A为浓氨水、B为生石灰、C为AgNO3溶液时,小试管中的现象是 ;其中发生的离子反应方程式是 。
(4)装置D的作用是 。
(本题考查学生对常见气体反应原理及性质的掌握情况。答题时重在分析,规范表达,灵活变通。)
7.实验室可以用下图所示仪器连接起来制备纯净的二氧化碳并测定其式量。
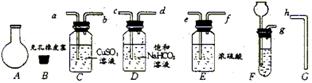 |
现用含有少量硫化亚铁的大理石和盐酸反应制备二氧化碳气体,实验步骤如下:
(1)将橡皮塞B塞在A烧瓶口,并用橡皮筋套在烧瓶的瓶颈处以标记橡皮塞所塞入瓶颈的深度,准确称其质量为m1g。
(2)连接制备和净化气体的装置,其连接顺序是:___接___,___接___,___接___,___接___。
 (3)将导管G插入烧瓶A中用向______(填“上”或“下”)排空气法收集二氧化碳气体;检验二氧化碳气体已经充满烧瓶的方法是_________________________________。若经检验,二氧化碳气体已经充满烧瓶,迅速用橡皮塞塞好烧瓶瓶口,并称其质量为m2g。
(3)将导管G插入烧瓶A中用向______(填“上”或“下”)排空气法收集二氧化碳气体;检验二氧化碳气体已经充满烧瓶的方法是_________________________________。若经检验,二氧化碳气体已经充满烧瓶,迅速用橡皮塞塞好烧瓶瓶口,并称其质量为m2g。
(4)将烧瓶口橡皮塞取下,向烧瓶内注水至标记线,再将水小心地倒入量简,测量出水的体积为 V1mL;将该体积换算成标准状况时的体积为 V2mL。
请写出二氧化碳式量的计算式
;
(5)若不将气体净化和干燥,所测定的二氧化碳式量的数值将会________________(填“偏高”或“偏低”,其理由是_________________________________________________。
(该题考查实验装置的安装顺序,实验数据的处理及误差分析。答题要把握实验装置安装顺序的一般思路,在理解的基础上作出判断、处理数据、得出结果。)
答案分析:
典型题点击
1.(1)NO
(2)①C2H4 装置中没有温度计,无法控制反应温度
②Cl2 反应生成的Cl2被C中的NaOH溶液吸收了
③NH3 反应生成的NH3被C中的H2O吸收了
讲析:由所给装置图和题意可知:①发生装置适用于固+液(或液+液)反应(可加热或不加热);②对不同气体,洗气、干燥所用试剂应有所不同。A选项中制C2H4,装置中没有温度计,无法控制反应温度;B选项中反应生成的Cl2被装置C中的NaOH溶液吸收了;C选项中反应生成的NH3被装置C中的H2O吸收了。
2.(1) ③ 、 ⑦ 、 ⑤ 、 ② 、 ;
MnO2 NaCl Al,NaOH
![]() 和浓HCl 、和H2O 、浓硫酸 、 和H2O 、 ;
和浓HCl 、和H2O 、浓硫酸 、 和H2O 、 ;
(2)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
![]() Cl2+2NaOH=NaCl+NaClO+
H2O
Cl2+2NaOH=NaCl+NaClO+
H2O
2Al+3Cl2 2AlCl3
讲析:实验室制取氯气应选用MnO2和11.9mol·L-1盐酸 (浓盐酸)共热,而不应选2mol·L-1盐酸(稀盐酸);所制氯气中含(HCl和H2O)必须先通过食盐水(除HCl),再通过浓硫酸(除H2O),得到的纯净氯气通入②中发生反应,并注意吸收多余的尾气。装置接口要匹配,洗气时应“长进短出”。
3.(1)关闭弹簧夹时,反应产生的气体使试管内液面上的压力增加,所以液面下降。
(2)塞紧橡皮寨,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于试管内的水面,停止加水后,漏斗中与试管中的液面差保持不再变化,说明装置不漏气。 (3)
| CO2 | 向上排空气法 | 通入澄清石灰水使石灰水变浑浊 |
(4)因为:此反应需要加热 MnO2是粉末状的
新活题网站
1.C 2.B 3.D 4.C 5.C
讲析:1.实验室制备气体要操作简单,容易分离,经济实惠,切实可行。甲烷在高温下才能分解成H2和C,实验室难以办到。赤热的炭与水蒸气反应生成CO和H2,难以分离。4.加热固体,试管口应略向下倾斜(A、B错),NH3、NO2溶于水或与水反应(B、D错)。
![]() 6.(1)出现浑浊
6.(1)出现浑浊
![]() ONa+CO2+H2O→
OH+NaHCO3
ONa+CO2+H2O→
OH+NaHCO3
(2)紫红色褪去 CaC2+2H2O→Ca(OH)2+C2H2↑
(3)出现浑浊,最后消失
Ag++NH3·H2O→AgOH+NH4+
AgOH+2NH3·H2O=Ag(NH3)2++OH-+2H2O
(4)防止液体倒吸
7.(2)g接a,b接c,d接e,f接h。或g接c,d接a,b接e,f接h。
(3)上;用燃着的木条放在瓶口,若火焰熄灭,则证明CO2已经充满。
![]()
(5)偏低:因为含有H2S、HCl、H2O等杂质气体的式量均小于CO2的式量。
