高三化学复习单元测试(6)—氧族元素 环境保护
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,满分108分.考试时间:60分钟.可能用到的原子量: H:1 C:12 O:16 S:32 N:14 Cu:64 Fe:56 Ag:108
第Ⅰ卷(选择题,共48分)
一、选择题(每小题只有一个选项符合题意,每小题4分,共12题)
1. (05全国卷Ⅲ)6.现有以下几种措施:①对燃烧煤时产生的尾气进行除硫处理,②少用原煤做燃料,③燃煤时鼓入足量空气,④开发清洁能源。其中能减少酸雨产生的措施是
A.①②③ B.②③④ C.①② ④ D.①③④
2.(05江苏)10.下列对物质用途的描述中,错误的是
A 浓硫酸可用于干燥NH3、H2、O2等气体 B 二氧化硫可用来漂白纸浆、毛、丝等
C 氟化钠可用于预防龋齿 D.铝可用于冶炼某些熔点较高的金属
3.(05江苏)6.下列有关环境保护的说法中错误的是
A 含氮、磷化合物的生活污水大量排放可使水体富营养化
B 各国工业大量排放二氧化硫是全球气候变暖的主要原因
C 劣质装修材料中的甲醛、苯、氡气等对人体有害
D 废旧电池中的汞、镉、铅等重金属盐对土壤和水源会造成污染
4..(05江苏)2.保护环境是每一个公民的责任,下列做法:① 推广使用无磷洗涤剂;② 城市生活垃圾分类处理;③推广使用一次性木质筷子;④推广使用清洁能源;⑤过量使用化肥、农药;⑥推广使用无氟冰箱。其中有利于保护环境的是
A.①②④⑤ B.②③④⑥ C.①②④⑥ D.③④⑤⑥
5.(05北京)6.高压电机、复印机工作时会产生臭氧,该气体有强氧化性。下列叙述中不正确的是 A.臭氧和氧气是氧的同素异形体 B.臭氧可使湿润的KI淀粉试纸变蓝
C.臭氧的存在对人体有益无害 D.臭氧是很好的消毒剂和脱色剂
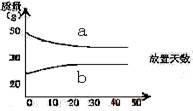 6.(05上海)8、浓硫酸和2mol/L的稀硫酸,在实验室中敞口放置。它们的质量和放置天数的关系如右图,分析a、b曲线变化的原因是( )
6.(05上海)8、浓硫酸和2mol/L的稀硫酸,在实验室中敞口放置。它们的质量和放置天数的关系如右图,分析a、b曲线变化的原因是( )
A、a升华、b冷凝 B、a挥发、b吸水
C、a蒸发、b潮解 D、a冷凝、b吸水
7. (05广东)25、下列关于过氧化氢的说法正确的是
A. 过氧化氢具有杀菌消毒作用,是强酸 B. 过氧化氢是离子化合物
C. 过氧化氢可以发生分解反应 D.过氧化氢是水的同分异构体
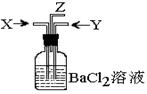 8.(05上海)21、碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是
8.(05上海)21、碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是
A.气瓶中产生的沉淀是碳酸钡 B.Z导管出来的气体中无二氧化碳
C、气瓶中产生的沉淀是硫酸钡 D、Z导管口有无色气体出现
9.(05上海)20、水蒸气中常含有部分(H2O)2,要确定(H2O)2的存在,可采用的方法是
A、1L水蒸气冷凝后与足量金属钠反应,测产生氢气的体积
B、1L水蒸气通过浓硫酸后,测浓硫酸增重的质量
C、该水蒸气冷凝后,测水的pH
D、该水蒸气冷凝后,测氢氧原子比
10.(05上海)22、含8.0g NaOH的溶液中通入一定量H2S后,将得到的溶液小心蒸干,称得无水物7.9g,则该无水物中一定含有的物质是
A、Na2S B、NaHS C、Na2S和NaHS D、NaOH和NaHS
11.(05天津)13.下列实验操作或事故处理中,正确的做法是
A.银镜反应实验后附有银的试管,可用稀H2SO4清洗
B.在中学《硫酸铜晶体里结晶水含量测定》的实验中,称量操作至少需要四次
C.不慎将浓H2SO4沾在皮肤上,立即用NaOH溶液冲洗
D.在250mL烧杯中,加入216mL水和24g NaOH固体,配制10% NaOH溶液
12.(05北京)12.下列实验操作中,先后顺序正确的是
A.稀释浓硫酸时,先在烧杯中加入一定体积的浓硫酸,后注入蒸馏水
B.为测定硫酸铜晶体的结晶水含量,称样时,先称取一定量的晶体,后放入坩锅中
C.为检验酸性溶液中的Cl-和SO42-,先加硝酸银溶液,滤去沉淀后加硝酸钡溶液
D.在制取干燥纯净的氯气时,先使氯气通过水(或饱和食盐水),后通过浓硫酸
第I卷答题表 班考号 姓名
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答案 |
第Ⅱ卷(非选择题共60分)
13. (14分)(1)实验证明铜不能在低温下与O2反应,也不能与稀H2SO4共热发生反应,但工业上却是将废铜屑倒入热的稀H2SO4中并通入空气来制备CuSO4溶液。
铜屑在此状态下被溶解的化学方程式为______________________________________________。
(2) 在过氧化氢跟稀硫酸的混合溶液中,加入铜片常温下就生成蓝色溶液。写出有关化学方程式__________________________________________________。
(3) 硫酸具有以下(A)-(E)所示的性质,试选择正确答案编号填在①-②所示变化的相应空格处:
(A)在水中电离,并呈强酸性;(B)高沸点难挥发;(C)浓硫酸具有吸水性;(D)浓硫酸具有脱水性;(E)浓硫酸具有强氧化性;(F)浓硫酸溶于水放出大量热。
①铜片与浓硫酸共热产生二氧化硫气体_________________。
②将稀硫酸滴在一张纸片上,再烘干(纸片不接触灯焰),发现纸片中滴过酸液的部位先变黑最后留下一个洞_________________________。
③蔗糖晶体中滴入适量的浓硫酸,再在滴有浓硫酸处加滴2-3滴水。发现加水处立即黑,黑色区不断扩大,最后变成一块疏松的焦炭,并伴有刺激性气味气体产生。_________。
 14.(10分) 检验SO42-应向被测溶液中先加入适量的___,如果无明显变化,再滴入 溶液,观察到有____生成,可判断原溶液中含有SO42-。如果向被测溶液中先滴加BaCl2溶液,有白色沉淀生成,再滴加稀盐酸,沉淀不消失,则该溶液除可能含SO42-外,还可能含有___。如果向被测溶液中滴加Ba(NO3)2溶液,有白色沉淀生成,再滴加稀硝酸,白色沉淀不消失,则该溶液除可能含有SO42-外,还可能含有___。
14.(10分) 检验SO42-应向被测溶液中先加入适量的___,如果无明显变化,再滴入 溶液,观察到有____生成,可判断原溶液中含有SO42-。如果向被测溶液中先滴加BaCl2溶液,有白色沉淀生成,再滴加稀盐酸,沉淀不消失,则该溶液除可能含SO42-外,还可能含有___。如果向被测溶液中滴加Ba(NO3)2溶液,有白色沉淀生成,再滴加稀硝酸,白色沉淀不消失,则该溶液除可能含有SO42-外,还可能含有___。
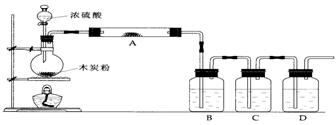
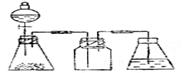
15. (16分)根据下图回答问题:
(1)上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法证明该装置不漏气。_______________________________ 。
(2)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:_______________________ 。
(3)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用:A中加入的试剂和作用是___________________;B中加入的试剂和作用是___________________;D中加入的试剂和作用是___________________。
(4)实验时,C中应观察到的现象是________________________________________________。
16.(05广东)20、(20分)研究性学习小组进行SO2的制备及性质探究实验。
(1)根据反应Na2SO3(固)+H2SO4(浓)= Na2SO4 + SO2↑+ H2O,制备SO2气体。
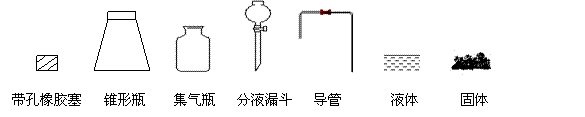 ①用下列简图,在方框中画出制备并收集SO2的实验装置(含试剂)示意图。
①用下列简图,在方框中画出制备并收集SO2的实验装置(含试剂)示意图。

②实验过程中,使用分液漏斗滴加浓硫酸的操作是_____________________________。
(2)将SO2气体分别通入下列溶液中:①品红溶液,现象是__________________ ;
②溴水溶液,现象是________________________;③硫化钠溶液,现象是_____________________。(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象很不明显,但又不存在气密性问题。请你推测可能的原因并说明相应的验证方法(可以不填满)。
①原因_____________________;验证方法__________________________ 。
②原因_____________________;验证方法_________________________ 。
③原因_____________________;验证方法__________________________ 。
高三化学复习单元测试(6)—氧族元素 环境保护参考答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答案 | C | A | B | C | C | B | C | C | AB | A | B | D |
13. (1)2Cu+O2+2H2SO4=2CuSO4+2H2O。(2)Cu+H2O2+H2SO4=CuSO4+2H2O。(3) ①A和E。②BDE。③C、F、D、E。
14. 盐酸;氯化钡;Ag+;SO32-。
15.(1)反应前先用小火加热烧瓶,B、C、D瓶中有气泡冒出,停止加热后,水会升到导管里形成一段水柱,证明装置不漏气。
(2)2H2SO4(浓)+C![]() 2H2O+2SO2+CO2
2H2O+2SO2+CO2
(3)A:无水硫酸铜。检验水。B:品红溶液。检验二氧化硫。D:澄清石灰水。检验二氧化碳。
(4)酸性高锰酸钾溶液的颜色不褪尽。
16. 20.(1) ①如图配置
②打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,缓慢滴加。
(2) ①溶液褪色②溶液褪色③有浅黄色沉淀(或溶液变浑浊)
(3)①Na2SO3 变质取待测试样于试管中,加适量蒸馏水配成溶液,先滴入足量稀盐酸,再滴入BaCl2 ,溶液有白色沉淀生成,则证明该Na2SO3 固体变质
②不是浓硫酸用洁净玻璃棒蘸取待测试样,涂白纸不变黑,则证明该溶液不是浓硫酸
