��������05-06ѧ��ȵڶ�ѧ�ڸ�����ѧ�ܸ�ϰģ����Ծ�
���л���ѧ�������𰸣�
�������Ӣ������ʦ���У�������ˣ���ӱ������һ�У�
������ʱ��120���ӡ�����150�֣�
| ��� | �� | �� | �ܷ� | |||||||
| 1-22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 | ||
| �÷� | ||||||||||
| ������ | ||||||||||
�����õ������ԭ��������H��1��C��12��O��16��Cl��35.5��Na��23��Ca��40��Fe 56��Cu��64
�ڢ������ѡ���⡡��66�֣�
һ��ѡ����(�������22С�⣬ÿС��3�֣���66�֡�ÿС��ֻ��һ��ѡ��������⡣)
1.CCTV���Ƽ�������������2004��3���п�Ժ�״���CO2�ϳɿɽ������Ͼ۶�����̼���������˵���������ǣ�������
A.�۶�����̼���ϵ�ʹ�û������ɫ��Ⱦ��
B.�۶�����̼������ͨ���Ӿ۷�Ӧ�Ƶõ�
C.�۶�����̼������ɱ���Ϊͬ���칹�塡
D.�۶�����̼������ɱ������ڴ�����
2.2004��ŵ������ѧ��������������ɫ�е���λ��ѧ�ң��Ա��������ڵ����ʽ����о����������Ĺ��ס����й��ڵ����ʵ������У�����ȷ���ǣ�������
A.ijЩ��������Ũ�������û���
B.��Ȼ������ˮ������ղ����Ǧ�����������
C.�ؽ�������Һ���������Һ����ʹ�����ʱ���
D.���ö����ЧӦ����������Һ��ʳ��ˮ
3.2005��1�£�ŷ����ֵĻݸ�˹��̽�����״γɹ���½���ǵ�������ǡ�������������ѧ�Ҷ�̽�������ص����ݽ����˷����������������Ĵ������к���95%�ĵ��������������Ϊ���������̼�⻯������й���̼�⻯�����������ȷ���ǣ�������
A.̼�⻯�����ͨʽΪCnH2n+2������������ B.̼�⻯�����еĻ�ѧ�����Ǽ��Լ�
C.��Ȳ�ͱ��Ǻ�̼����ߵ�̼�⻯������� D.ʯ�͵���Ҫ�ɷ���̼�⻯����
4.���и�ѡ������������������������������ǣ�������
A.��������NO2���Ͷ���������NO2���������� B.�����ᣨHNO2�������������NO2����
C.�Ǽ�����CH2OH���ͼ�������CH3O���� ��D.�ǻ�����OH������������OH����
5.�ڡ���ɫ��ѧ���ա��У�����״̬�Ƿ�Ӧ���е�ԭ��ȫ��ת��Ϊ���ƵõIJ����ԭ��������Ϊ100%�����з�Ӧ����������ԭ��������Ϊ100%���ǣ�������
���û���Ӧ���ڻ��Ϸ�Ӧ���۷ֽⷴӦ���ܸ��ֽⷴӦ����ȡ����Ӧ���ӳɷ�Ӧ������ȥ��Ӧ����Ӿ۷�Ӧ�������۷�Ӧ����������Ӧ
A.�٢ۢܡ����� B.�ݢߢᡡ�� ��C.�ڢޢࡡ����D.�ڢߢ�
![]()
��ϵ�л������У�̼Ԫ�ص��������������ֵ�ǣ�������
A.32%������ B.46.6%���� ��C.85.7%������D.��ȷ��
7.��ij���ۻ������к���C��H��O��N����Ԫ�أ�����n(C)��n(N)��n(O)�ֱ��ʾC��N��O��ԭ����Ŀ����Hԭ����Ŀ�����ڣ��� ��
A.2n(C)��2n(N)��2�������� B.2n(C)��2n(N)��n(O)����
C.3n(C)��2n(O)��2������ ��D.2n(C)��n(N)��2
8.ø�ǵ����ʣ�������е����ʵ����ԣ�ø�ܴ������л���ѧ��Ӧ�����б�ʾ�¶�T�뷴Ӧ����v�Ĺ�ϵ�����ߣ���ø�μӵ��ǣ��� ��
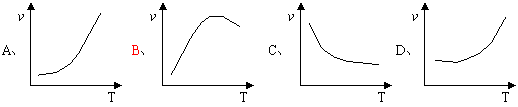 |
9.�л��������ԭ��(��ԭ����)����Ӱ��ᵼ�����ǻ�ѧ���ʵĸı䡣����������˵�������۵���ǣ��� ��
A.��������NaOH��Һ��Ӧ�����Ҵ�����
B.����ɷ���������Ӧ���������
C.��ϩ�ɷ����ӳɷ�Ӧ�������鲻��
D.�����ʵ����ĸ��ͺ��Ҵ��ֱ������������Ʒ�Ӧ�����Ͳ�����H2��
10.��![]() �����д���ͬһƽ���ϵ�ԭ�����������ǣ�������
�����д���ͬһƽ���ϵ�ԭ�����������ǣ�������
A. 18���������� B. 20������������ C. 21���������� D.23
11.2005��ŵ������ѧ�������衰��ϩ�����ֽⷴӦ�о������������ס�����λ��ѧ�ҡ���ϩ�����ֽⷴӦ����ָ�ڽ����⡢�ɵȴ����������£�̼̼˫�����Ѳ�������ϵĹ��̡���2����ϩ��RCH=CHR���������������û����������µ�ϩ��RCH=CHR��R��CH=CHR���������ʽΪC4H8��ϩ���У���ȡ���ַ�����ϩ�����ֽⷴӦ����������ϩ����������һ������У�����ϩ��������Ϊ��������
A.5�֡��� B.4�֡������� C.3 �֡����� D.2��
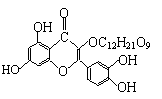 12.��Ȼά����P�����ڻ��������У�����һ��Ӫ������������ṹ����ͼ��ʾ���������˵������ȷ���ǣ��� ��
12.��Ȼά����P�����ڻ��������У�����һ��Ӫ������������ṹ����ͼ��ʾ���������˵������ȷ���ǣ��� ��
A.��Ȼά����P��FeCl3��Һ�ܷ�����ɫ��Ӧ
B.��Ȼά����Pһ���ܷ���ˮ�ⷴӦ
C.��Ȼά����Pһ���ܷ����ӳɷ�Ӧ
D.��Ȼά����Pһ���ܷ���ȡ����Ӧ
13.���и������������Ժ��ֱ�����ϣ�ֻҪ�ܵ����ʵ���һ������ȫȼ��ʱ�������������Ƕ�ֵ���ǣ����� ��
A. CH2=CH2��C2H5OH��HOCH2CH2COOH������B. CH2O��C2H4O2��C6H12O6
C. C6H6��C5H10��C6H6O�������������������� D. H2��CO��CH3OH
14.ij���ۻ����ﺬ̼���⡢������Ԫ�أ������й����ĸ���ԭ�裬�Ҷ�λ����������Ķ��㣬ÿ������ԭ�Ӽ䶼��һ��̼ԭ�ӡ���֪��������̼̼������Ҳû��̼̼˫������û�����ķ���ʽΪ( �� )
A.CH8N4�� ������ B.C4H8N4 ��������C.C6H10N4������ D. C6H12N4
15.��ϩ�Ʒ���һ�ּ�����ҩ��ṹ���£������й�����������ȷ���ǣ��� ��
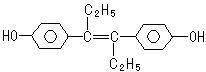
A. ��ҩ��������л��ܼ���ȡ��������
B.����NaOH��NaHCO3������Ӧ
C.1mol���л��������5mol Br2������Ӧ
D.���л�������У�������16��̼ԭ�ӹ�ƽ��
16.�ҹ���ѧ�����ߺϳ�������ṹ���ӵ���Ȼ�л�������磺Ҷ���ء�Ѫ���ء�ά����B�ȣ�Ҷ���صĽṹ��ͼ��ʾ�������й�˵����ȷ���ǣ��� ��
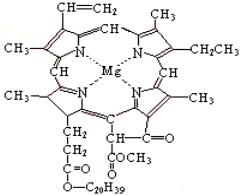
A.Ҷ�������ڸ߷��ӻ�����
B.Ҷ���ط����к����������͵�˫��
C.Ҷ���ز����ڷ�����
D.��һ�������£�Ҷ�����ܼӳɡ�ˮ�⡢�����ȷ�Ӧ
17.������10�����ʷ�Ϊ����
A�飺�ٱ��ӣ������ᣬ��ţ�ͣ��ܱ����ᣬ������������
B�飺����ˮ����ȩ�����������Һ�����Ȼ�����Һ��������ơ�
A����������һ�ָ�B�����ʾ��ܷ�Ӧ��B����������1�ָ�A�����ʾ��ܷ�Ӧ�������������ʷֱ���(�� )
A. �٢ࡡ B. �ۢ⡡ C. �٢ޡ� D. �ڢ�
18.�л���ķ���ʽΪC9H18O2�������������¼�ˮ��Ϊ�Һͱ������л������ͬ���¶Ⱥ�ѹǿ�£�ͬ�������Һͱ���������ռ�����ͬ����Ŀ��ܽṹ��(�� )
A.8�֡�������������������������B.14�֡�����������������������C.16�֡�����������������������D.18��
19.����ˮ�����߲ˡ�����Ʒ�и�����ά����C�������ԵĿ�˥�����ã����ױ�����������ij����С�����õ�ζ�����ij��֭��ά����C�ĺ������仯ѧ����ʽΪ��
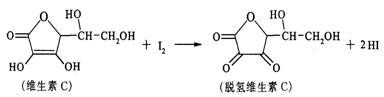
����˵����ȷ���ǣ�����������
A.������ӦΪȡ����Ӧ��������������B.�ζ�ʱ��������ƿ
C.�ζ�ʱ���õ�����Һ��ָʾ��������D.ά����C�ķ���ʽΪC6H9O
20.Ӣ��ý��05��4��15�ձ�������¶�������к��е�������������������������ˮ�����ɸ��������ȼ��飩���������ܵ��¸β��������°�֢����֪�������Ľṹ��ʽ���£��й�˵������ȷ���ǣ�������
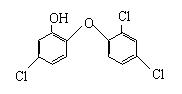
A.�������ķ���ʽΪ��C12H7Cl3O2
B.����������ͬ���칹��
C.��������������������Һ��Ӧ
D.������������ˮ
21.�����л���������ͬ���칹����ǣ�������
A.�ұ���һ�ȴ���
B.����ʽΪC4H8O2���л���
C.����ʽΪC4H10�����Ķ���ȡ����
D.����ʽΪC3H9N���л������Nԭ������������������ԭ������
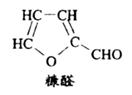
22.�������г���ľ�Ǵ�����ζ����ľ�Ǵ����Է�ֹȣ�ݣ�ľ�Ǵ��Ľṹ��ʽΪ����ͼ�������й�
ľ�Ǵ���˵����ȷ���ǣ�������
A.ľ�Ǵ��ǡ��ֵ��ǣ�����ѿ�ǻ�Ϊͬϵ��
B.ľ�Ǵ����ܽ���ˮ��һ��������������ᷢ��������Ӧ
C.ľ�Ǵ����л�ԭ�ԣ��ܱ�����Cu��OH��2����
D.ľ�Ǵ���ȥ������ˮ�ɵÿ�ȩ(�ṹ������ͼ)
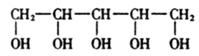 ����������
����������
�ڢ��������ѡ���⡡��84�֣�
����(�������2С�⣬��20��)
23.(10��)
��1������ʵ�������������ȷ����___________������ţ�
A.�Ҵ��к�������ˮ�ɼ�����ʯ���������Ƶ���ˮ�Ҵ�
B.����ˮ�Ҵ���Ũ���ᰴ�����3��1��ϣ�������170����ȡ��ϩ
C.����ˮ����Ũ����������
D.�ڼ�������Һ�м���ŨHNO3���Ⱥ�����ɻ�ɫ����
E.��֬������Ӧ��Ӧ������м���ʳ�οɽ������������
F.ֲ���ͺ��ѻ����Ϳ�����ˮ����
��2����֬��NaOHˮ��Һ���Ⱥ�����֬�Ƿ���ȫˮ��ķ�����
____________________________________________________________��
��3�����ж�ʧ��ǩ�ĵ��ۺ���������ƿ��Һ���������ַ������Լ���
����һ��
��������
��������
24.��10�֣����õ���ȩˮ��Һ������ֲ������ϲ�Ϊ��ɫ��״Һ�壬�²�Ϊˮ��Һ.�ݲⶨ���ϲ�����Ϊ��ȩ�Ļ�״�ۺ���![]() �����ķе��ˮ�ķе�ߣ���������ȩ������ȩ�ķе���20.8�棬������Һ���ױ���������������ķе���117.9�棬�Ӿ��õ���ȩˮ��Һ����ȡ��ȩ(�Եõ���ȩˮ��Һ)�����������·�Ӧ��
�����ķе��ˮ�ķе�ߣ���������ȩ������ȩ�ķе���20.8�棬������Һ���ױ���������������ķе���117.9�棬�Ӿ��õ���ȩˮ��Һ����ȡ��ȩ(�Եõ���ȩˮ��Һ)�����������·�Ӧ��![]()
![]() n
n![]() ����.
����.
�Իش��������⣺
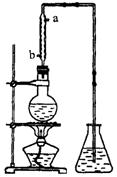
��1���ȷ�������õ�![]() �����������ǣ������������Һ©���У����÷ֲ���������²�Һ������ձ��У�Ȼ��_________.
�����������ǣ������������Һ©���У����÷ֲ���������²�Һ������ձ��У�Ȼ��_________.
��2�����һ��ʵ��֤�����õ���ȩ�Ƿ�������д����Ҫ�������衢ʹ�õ��Լ���ʵ������ͽ��ۣ���_�������������������������������������������������� _____________.
��3����n��3ʱ����д��![]() �Ľṹ��ʽ___________________________.
�Ľṹ��ʽ___________________________.
��4����ȡ��ȩ��װ����ͼ����ƿ�е�Һ����![]() ��6mol��L
��6mol��L![]() �Ļ���
�Ļ���
��ƿ��ʢ������ˮ�����Ȼ���������ڣ�![]() �����ֽ⣬���ɵ����嵼��
�����ֽ⣬���ɵ����嵼��
��ƿ��.
��������������ˮ�Ľ�����________���a����b����.
��ʵ����������������Ľ��У���Һ���к�ɫ���ʺʹ̼�����ζ��������.���û�ѧ����ʽ��ʾ��һ����_________________________.
�۵���ƿ�ڵ��ܿ�����Խ��Խ��ʱ��������ȩ��������������ʵ�����.���ʵ��װ�õĵ�һ�������ǣ�____________________________.
����(�������3С�⣬��28��)��
25.��10�֣��л���Ľṹ��ʽ���£�����ͨ����ͬ�Ļ�ѧ��Ӧ�ֱ��Ƶýṹ��ʽΪ��~��������
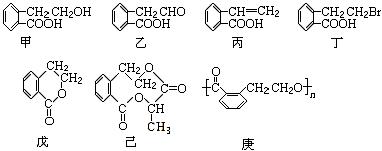
��ش��������⣺
��ָ����Ӧ�����ͣ��ס��������������� ���ס�����������������
���ڼס������������У���Ϊͬ���칹����������������� (����ţ���ѡ�۷֣���ͬ)���ɿ���������������������� ��
����֪HCHO����������ԭ�Ӷ���ͬһƽ���ڣ�������������������ԭ���п��ܶ���ͬһƽ���ڵ������������������� ��
26.��8�֣�����ʽΪC3H6O3�������ж���ͬ���칹�壬��д����������Ҫ��ĸ���ͬ���칹��Ľṹ��ʽ��˵�����ٲ�����ͬһ̼ԭ�����������ǻ�������Ȳ�����ȷ�����ͬ��ԭ�ӻ�ѧ������ͬ�����顢����ȷ�����ͬ��ԭ�ӻ�ѧ���������֡�
��1��������û�м�����1 mol������������Na��Ӧ����1 mol H2����������NaHCO3��Һ��Ӧ����Ľṹ��ʽΪ_________�������ܷ���������Ӧ����Ľṹ��ʽΪ_______________��
��2���ҷ���������ͬ��ԭ�ӵĻ�ѧ������ͬ���Ҳ������Na��Ӧ�����ҽṹ��ʽΪ��_______________��
��3����������̼�����ֱ������ֻ�ѧ��������Ļ�ѧ������ͬ���ұ������Na����Ӧ������ṹ��ʽΪ_______________��
27.(10��) A��һ�ֺ�̼���⡢������Ԫ�ص��л��������֪��A��Է�������Ϊ144������̼����������Ϊ50%��A����ʹ��ˮ��ɫ��A������ˮ���������������¿ɷ���ˮ�ⷴӦ���õ�B�ͼ״���B��̼���⡢��ԭ�Ӹ�����Ϊ1��1��1��������û��֧������������������Һ������Ӧ��
��1��A�ķ���ʽ������������������
��2��B�������������ŵ������������������������� ���������������������� ��
��3����B������ͬ�����ŵ�ͬ���칹��Ľṹ��ʽ������������������������ ��
��4����B��ȡA�Ļ�ѧ����ʽ�ǣ������������������������������������� ����������
�ġ�(�������2С�⣬��24��)��
28.(9��)��ϩ����Ŀǰũҵ�������ձ�ʹ�õ�ֲ���������ڼ����Դٽ����߲ˡ�ˮ�������ȵ���������зdz��õ�Ч������ϩ���Ĺ�ҵ����������ϩ��Ϊԭ�Ͼ����в�����еģ�������ϩת��Ϊ�ȴ��Ҵ���ͼʾ������;������
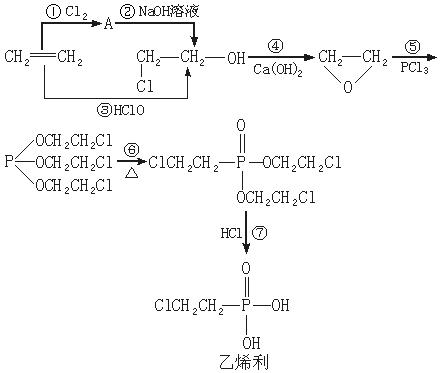
��ش��������⣺
��1���л���ѧ�Ļ�����Ӧ�����У�A.�ӳɷ�Ӧ��B.��ȥ��Ӧ��C.ȡ����Ӧ��D.���ŷ�Ӧ���֡��������ŷ�Ӧ��ָ��CH2=CH��OH![]()
![]() ��һ�෴Ӧ������Ӧ�Ĺ���ֻ��ԭ���ڷ����ڵĽ�Ϸ�ʽ�����������С���ָ���ϳ�·�������з�Ӧ�����Ļ������ͣ�����ţ�����_______________����_______________����_______________��
��һ�෴Ӧ������Ӧ�Ĺ���ֻ��ԭ���ڷ����ڵĽ�Ϸ�ʽ�����������С���ָ���ϳ�·�������з�Ӧ�����Ļ������ͣ�����ţ�����_______________����_______________����_______________��
��2��д����Ӧ����ʽ����_______________����____________��
��3����ϩ������ȡ���̽Ϻõ���������ɫ��ѧ������������ԭ�ϵ�ԭ�������ʸߣ�ԭ���е�ԭ�Ӿ����ܶ��ת������Ʒ�У����������������������������������е��л������д�ṹ��ʽ��_______________�Ϳ����ڸúϳ����ظ����á�
29.(15��)���������۾����ɾۼ���ϩ��������(HEMA)�Ƴɳ�����Ƭ����ϳ�·�߿����ǣ�
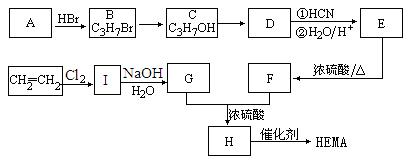
��֪��![]()
������CH3COOCH2CH2OH����������������
�����
��1��A��D��E�Ľṹ��ʽ�ֱ�Ϊ��A�������������� ��D���������������� ��E���������������� ��
��2��д������ת���Ļ�ѧ����ʽ��I��G������������������������������������������ ��
G+F��H�������� �������������������������������������������������������� ��
H��HEMA�������������������������������������������������������������� ��
�塢������ (��12��)
30.(12��)��CH4�����ʵ�������Ϊx��CH4��C2H2�Ļ������a mol��������������ȼ�գ�����Ӧ�����õ����建��ͨ��100ml 1.0mol/LNaOH��Һ�У�Ȼ��������Һ�ڵ�����С�����ɣ��ù���m g����ͨ������ش�
����a=0.05����m��ȡֵ��Χ��_________________��m��x�Ĺ�ϵ��________________��
����a=0.06����m��x�Ĺ�ϵ��______________________________________________��
���
1.B��2.C��3.D��4.D��5.C��6.C��7.D��8.B��9.A��10.C��11.B��12.B��13.A��14.D��15.B��16.C��17.A��18.C��19.C��20.D��21.D��22.B
23.(1)ADE��(2��)����
(2)������������ȣ�ȡ������������ˮ�У����͵���ˮ����ȫ��(2��)
(3)��6�֣�
����һ����һ��ǿ��������Һ�����й����ġ�ͨ·����Ϊ���ۣ�����������Ϊ�����ǣ�
����������ȡ������Һ���Թܣ��ֱ����������ˮ������������Ϊ���ۣ�û����ɫ�仯Ϊ�����ǣ�
����������ȡ������Һ������һ���������Ʊ���Cu��OH��2���ȣ�����ש��ɫ�����ļ�Ϊ�����ǡ�
24.��1�����ϲ����״Һ��![]() �ӷ�Һ©�����Ͽڵ���(2��)
�ӷ�Һ©�����Ͽڵ���(2��)
��2��ȡ�����²�ˮ��Һ���μ�ʯ��ָʾ��������Һ�Ժ�ɫ����˵��������ȩ�������������������𰸾��÷֣�(2��)
��3��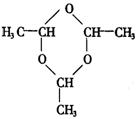 ��(2��)
��(2��)
��4����b (1��)����![]() (2��)��
(2��)��
���ȴ���ƿ�г������ܣ����ⷢ������.(1��)
25.����ȥ�� ȡ��(±��) �� �����졡���졢������ �� �� �� ����2�֣�
26.��8�֣���1��![]() ��2�֣�
��2�֣�![]() ����2�֣�
����2�֣�
��2��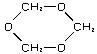 ��2�֣�
��2�֣�
��3��![]() ��2�֣�
��2�֣�
27.��10�֣��� C6H8O4����2�֣�
�� ̼̼˫���� ��2�֣������Ȼ���2�֣�
�� CH2=C(COOH)2��������2�֣�
��
HOOCCH=CHCOOH + 2CH3OH ![]() CH3OOCCH=CHCOOCH3
+ 2H2O�� ��2�֣�
CH3OOCCH=CHCOOCH3
+ 2H2O�� ��2�֣�
28.��1��A��D C������1�֣�
��2��CH2=CH2+Cl2![]() CH2Cl��CH2Cl����2�֣�
CH2Cl��CH2Cl����2�֣�
![]() +PCl3
+PCl3![]() P��OCH2CH2Cl��3�� ��2�֣�
P��OCH2CH2Cl��3�� ��2�֣�
��3��CH2ClCH2Cl����2�֣�
29.��15�֣���CH2=CHCH3����CH3COCH3����(CH3)2C(OH)COOH��������2�֣�
��2��CH2ClCH2Cl��2H2O![]() HOCH2CH2OH��2HCl��������
����3�֣�
HOCH2CH2OH��2HCl��������
����3�֣�
HOCH2CH2OH +CH2=C(CH3)COOH
![]() CH2=C(CH3)COOCH2CH2OH+H2O��
CH2=C(CH3)COOCH2CH2OH+H2O��
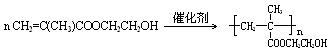
30.(12��)�� �� 5.3��m��8.4����(3��)�������� m=8.4-3.1x���� (3��)
�� ��0��x��1/3��m=8.4 (3��)��
��1/3��x��1��m=9.64-3.72x��(3��)