阳泉一中高考化学复习单元过关《化学平衡》试卷
(时间:50分钟。满分100分)
可能用到的原子量: H: 1 O: 16 N: 14 Na: 23 Cl: 35.5 C: 12 Ca: 40 Cu:64
S: 32 Fe: 56 Mg: 24 P: 31 Zn:65
一、选择题(下列各题只有1-2个选项符合题意。每小题4分,共60分。请将答案填在答题卡上)
1、下列措施,一定不能加快化学反应速率的是
A.增大压强 B.升高温度 C.加催化剂 D.增大体积
![]() 2、 对于反应:4NH3(g)
+ 5O2(g) 4NO(g) + 6H2O(g), 下列为四种不同情况下测得的反应速率,其中能表明该反应进行最快的是
2、 对于反应:4NH3(g)
+ 5O2(g) 4NO(g) + 6H2O(g), 下列为四种不同情况下测得的反应速率,其中能表明该反应进行最快的是
A.VNH3 = 0.2mol·L-1·s-1 B.VO2 = 0.24 mol·L-1·s-1
C. VH2O = 0.25 mol·L-1·s-1 D. VNO = 0.15 mol·L-1·s-1
![]() 3、在N2+3H2 2NH3的反应中,经过t秒钟后,NH3的浓度增加了0.6mol/L,在此期间,正反应速率V(H2)=0.45mol/(L·S),则t值为:
3、在N2+3H2 2NH3的反应中,经过t秒钟后,NH3的浓度增加了0.6mol/L,在此期间,正反应速率V(H2)=0.45mol/(L·S),则t值为:
A. 1秒 B. 1.5秒 C. 2秒 .D. 2.5秒
![]() 4、在密闭容器中通人一定量的HI气体,使其在一定条件下发生反应:2HI H2+I2 (气) 。下列叙述中一定属于平衡状态的是:
4、在密闭容器中通人一定量的HI气体,使其在一定条件下发生反应:2HI H2+I2 (气) 。下列叙述中一定属于平衡状态的是:
A. HI、H2、I2的浓度相等 B. 混合气体的颜色不变化时
C. 混合气体的总压不变时 D. v(HI):v(H2):v(I2)=2:1:1时
![]() 5、 密闭容器中,反应xA(g) +
yB(g) zC(g)达平衡时,A的浓度为0.5mol/L, 若保持温度不变,将容器的容积扩大到原来的2倍,达新平衡时A的浓度降为0.3mol/L。下列判断正确的是:
5、 密闭容器中,反应xA(g) +
yB(g) zC(g)达平衡时,A的浓度为0.5mol/L, 若保持温度不变,将容器的容积扩大到原来的2倍,达新平衡时A的浓度降为0.3mol/L。下列判断正确的是:
A. x+y < z B. 平衡向正反应方向移动 C. B的转化率降低 D. C的体积分数下降6、向0.1mol/L氨水中逐渐加入一定量的水,始终保持增大趋势的是:
A. NH3·H2O的浓度 B. OH -的浓度 C. NH4+ 的数目 D. NH4+的浓度
7、下列可逆反应中,正反应是吸热反应的是:
![]() A.
2NO2 (气) 2NO(气)+O2
(气),降温,颜色加深。
A.
2NO2 (气) 2NO(气)+O2
(气),降温,颜色加深。
![]() B.
NO2+SO2 NO+SO3,降温,SO3的体积分数增加。
B.
NO2+SO2 NO+SO3,降温,SO3的体积分数增加。
![]() C.
CS2+2H2O CO2+2H2S,升温,CO2的平衡浓度增大。
C.
CS2+2H2O CO2+2H2S,升温,CO2的平衡浓度增大。
![]() D.PCl3+Cl2 PCl5,降温,PCl3转化率增大。
D.PCl3+Cl2 PCl5,降温,PCl3转化率增大。
![]() 8、在一个6L的密闭容器中,放入3LX(气)和2LY(气),在一定条件下发生下列反应4X(气)+3Y (气) 2Q(气)+nR(气)。达到平衡后,容器内温度不变,混合气体的压强比原来增加5%,X的浓度减小1/3,则该反应式中n值是
8、在一个6L的密闭容器中,放入3LX(气)和2LY(气),在一定条件下发生下列反应4X(气)+3Y (气) 2Q(气)+nR(气)。达到平衡后,容器内温度不变,混合气体的压强比原来增加5%,X的浓度减小1/3,则该反应式中n值是
A. 3 B. 4 C. 5 D. 6
9、在25℃、1.01×105Pa状态下,相同容积的甲、乙两个密闭容器,甲中盛放N2,乙中盛放NO2和N2O4混合气体。若将甲、乙两容器同时冷却降温到0℃,则此时甲、乙两容器内的压强关系是
A.P甲>P乙 B.P甲<P乙 C.P甲=P乙 D.P甲=P乙=1.01×105Pa
![]()
|
|
10、下列表示可逆反应:2A(气)+B(气) D(气)+Q(Q>0)的图示中正确的是
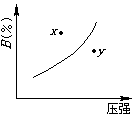 A. B. C. D.
A. B. C. D.
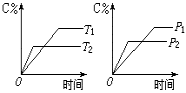
11、![]() 对于mA(固)+nB(气) pC(气)+Q的可逆反应,在一定温度下B的百分含量与压强的关系如图所示,则下列判断正确的是
对于mA(固)+nB(气) pC(气)+Q的可逆反应,在一定温度下B的百分含量与压强的关系如图所示,则下列判断正确的是
A.m+n<p B. x点的状态是v正>v逆
C. n>p D.x点比y点的反应速度慢
12、下列能用勒沙特列原理解释的是
①棕红色NO2加压后颜色先变深后变浅
②.FeCl3溶液加热后颜色加深 ③.Fe(SCN)3溶液中加入固体KSCN后颜色变深 ④氯水宜保存在低温、避光条件下 ⑤乙酸乙酯在碱性条件下水解比在酸性条件下水解更有利 ⑥. SO2催化氧化成SO3的反应,往往加入过量的空气
⑦向AgCl悬浊液中加入KI溶液有黄色沉淀生成
A.①②⑤⑥ B.②③④⑦. C.①③⑤⑦ D.全部
 13、 可逆反应mA(s)+nB(g)
13、 可逆反应mA(s)+nB(g)![]() pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图(T2>T1),根据图中曲线分析,判断下列叙述中正确的是
pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图(T2>T1),根据图中曲线分析,判断下列叙述中正确的是
A.到达平衡后,若使用催化剂,C的质量分数增大
B.平衡后,若升高温度,平衡则向逆反应方向移动
C.平衡后,增大A的量,有利于平衡向正反应方向移动
D.化学方程式中一定n>p+q
![]() 14、某容积可变的密闭容器中放入一定量的A和B的混合气体,在一定条件下发生反应:A(气)+2B(气) 2C(气)。若维持温度和压强不变,当达到平衡时,容器的体积为V,此时C气体的体积占40%,则下列推断正确的是
14、某容积可变的密闭容器中放入一定量的A和B的混合气体,在一定条件下发生反应:A(气)+2B(气) 2C(气)。若维持温度和压强不变,当达到平衡时,容器的体积为V,此时C气体的体积占40%,则下列推断正确的是
A.原混合气体的体积为1.1V B. 原混合气体体积为1.2V
![]()
 C.反应达到平衡时,气体A消耗了0.2V D.反应达到平衡时,气体B消耗了0.2V
C.反应达到平衡时,气体A消耗了0.2V D.反应达到平衡时,气体B消耗了0.2V
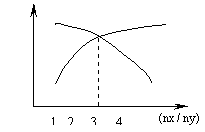
15、一定条件下,将X和Y两种物质按不同比例放入密闭容器中,反应达平衡后,测得X、Y转化率与起始时两种物质的量之比nx/ny 的关系如图,则X和Y反应的方程式可表示为
![]()
![]() A.X+3Y 2Z B.3X+Y 2Z
A.X+3Y 2Z B.3X+Y 2Z
![]()
![]() C.3X+2Y Z D.2X+3Y 2Z
C.3X+2Y Z D.2X+3Y 2Z
阳泉一中高考化学复习单元过关-《化学平衡》
班级 姓名 成绩
选择题答题卡
| 1 |
| 2 |
| 3 |
| 4 |
| 5 |
| 6 |
| 7 |
| 8 |
|
| 9 |
| 10 |
| 11 |
| 12 |
| 13 |
| 14 |
| 15 |
|
| |
二、填空题(共24分)
![]() 16、(5分)在密闭容器中进行可逆反应: CO(气)+NO2(气) CO2(气)+NO(气)+热量,达到平衡后,只改变其中一个条件,对平衡的影响是:
16、(5分)在密闭容器中进行可逆反应: CO(气)+NO2(气) CO2(气)+NO(气)+热量,达到平衡后,只改变其中一个条件,对平衡的影响是:
(1)增大容器的体积,平衡 ,反应混合物的颜色 。
(2)通人CO2气体,平衡 ,反应混合物的颜色 。
(3)加入催化剂,平衡 。
17、(5分)在一定条件下,反应A(气)+B(气)![]() C(气)+Q达到平衡后,根据下列图象判断
C(气)+Q达到平衡后,根据下列图象判断
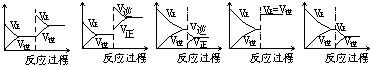
A. B. C. D. E.
(1)升温,达到新的平衡的是( ) (2)降压,达到新的平衡的是( )
(3)减少C的量,移向新平衡的是( ) (4)增加A的量,移向新平衡的是( )
(5)使用催化剂,达到平衡的是( )
18、(6分)现有可逆反应A(气)+B(气)![]() 3C(气),下图中甲、乙、丙分别表示在不同的条件下,生成物C在反应混和物中的百分含量(C%)和反应时间的关系:
3C(气),下图中甲、乙、丙分别表示在不同的条件下,生成物C在反应混和物中的百分含量(C%)和反应时间的关系:
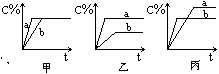
(1)若甲图中两条曲线分别表示有催化剂和无催化剂时的情况,则_ __曲线是表示有催化剂时的情况。
(2)若乙图中的a曲线表示200℃和b曲线表示100℃时的情况,则此可逆反应的正反应是_ __ __热反应。
(3)若丙图中两条曲线分别表示不同压强下的情况,则__ __曲线是表示压强较大的情况。
![]() 19、(8分)对可逆反应,aA(气)+bB(气) cC(气)+dD(气)达到平衡时各物质的量浓度满足以下关系 :
19、(8分)对可逆反应,aA(气)+bB(气) cC(气)+dD(气)达到平衡时各物质的量浓度满足以下关系 :![]() 。
。
![]() 现有反应:CO(气)+H2O(气) CO2(气)+H2(气)+热量。在850℃时,K=1。
现有反应:CO(气)+H2O(气) CO2(气)+H2(气)+热量。在850℃时,K=1。
(1)若升高温度到950℃时,达到平衡时K__ ___l (填“大于”、“小于”、或”等于”)
(2)850℃时,若向一容积可变的密闭容器中同时充入1.0molCO,3.0molH2O,1.0molCO2和xmolH2,则:
当x=5.0时,上述反应向___________________(填“正反应”或“逆反应”)方向进行。
若要使上述反应开始时向正反应方向进行,则x应满足和条件是________
__________。
(3)在850℃时,若设x=5.0 和x=6.0,其它物质的投料不变,当上述反应达到平衡后,测得H2的体积分数分别为a%,b%,则a___ __b(填“大于、小于或等于”)
三、简答题(共6分)
20、(4分)今年是勒沙特列(Le Chatelier1850-1936)诞生150周年。请用勒沙特列原理解释如下生活中的常见现象:打开冰镇啤酒瓶把啤酒倒入玻璃杯,杯中立即泛起大量泡沫。
![]() 21、(4分)已知N2(气)+3H2(气) 2NH3(气) (正反应为放热反应)。为什么在合成氨工厂,通常采用20MPa –50MPa的压强和500℃左右的温度?
21、(4分)已知N2(气)+3H2(气) 2NH3(气) (正反应为放热反应)。为什么在合成氨工厂,通常采用20MPa –50MPa的压强和500℃左右的温度?
四、计算题(共10分)
22、(5分)以N2和H2为原料,在一定温度下的密闭容器中进行合成氨的反应。一段时间后,反应达平衡,此时测得平衡体系中NH3为4mol,起始与平衡时的压强之比为13:8,且
[H2]起始:[H2]平衡=4:1,求N2和H2的转化率。
![]() 23、(5分)在一定条件下,可逆反应A2+B2 2C,达到化学平衡状态,经测得平衡时:[A2]=0.5 mol /L,[B2]=0.1 mol /L,[C]=1.6
mol /L,若A2,B2,C的起始浓度分别用amol/L,bmol/L,cmol/L表示,要维持相同的平衡状态,请回答:
23、(5分)在一定条件下,可逆反应A2+B2 2C,达到化学平衡状态,经测得平衡时:[A2]=0.5 mol /L,[B2]=0.1 mol /L,[C]=1.6
mol /L,若A2,B2,C的起始浓度分别用amol/L,bmol/L,cmol/L表示,要维持相同的平衡状态,请回答:
(1)a,b应满足的关系是:
(2)a的取值范围是: 。