08高考化学易错易漏选择题专题训练(四)
总分共64分 测试时间30分钟
一、选择题(本题包括8小题,每小题4分,共32分。每小题只有一个选项符合题意。)
1、最近发现了一种新的氧微粒O4,对于这种微粒,下列说法正确的是
A、它是氧的一种新的同位素 B、它的摩尔质量为64
C、它是氧的一种新的同素异形体 D、它的氧化性比O3差
2、下列变化属于物理变化的是
A.熔融态的氯化钠导电 B.用加热的方法分离氯化钠固体和氯化铵固体
C.在氢氧化铁胶体中加入硫酸镁溶液,析出红褐色沉淀 D.将过氧化钠固体溶于水中
3、下列说法或表示法正确的是
A、等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B、由C(石墨)→C(金刚石):ΔH = +119 kJ· mol—1可知,金刚石比石墨稳定
C、在稀溶液中:H++OH-===H2O;ΔH=-57.3 kJ· mol—1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ
D、在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)===2H2O(l);ΔH=+285.8 kJ· mol—1
4、(2007全国卷天津考题 )13.天津是我国研发和生产锂离子电池的重要基地。锂离子电池正极材料是含锂的二氧化钴(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。电池反应为LiCoO2 + C6 ![]() CoO2 + LiC6 ,下列说法正确的是
CoO2 + LiC6 ,下列说法正确的是
A.充电时,电池的负极反应为 LiC6 - e- == Li + C6
B.放电时,电池的正极反应为 CoO2 + Li+ + e- == LiCoO2 ,
C.羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质
5、下列离子方程式正确的是
A、 将0.1mol/LHCl溶液缓缓滴入1 mol/L 50mLNa3PO4溶液中: 3H+ + PO43— = H3PO4
B、将1 mol·L—1 NaAlO2溶液和1.5 mol·L—1的HCl溶液等体积互相均匀混合
6AlO2— + 9H+ + 3H2O = 5Al(OH)3↓+ Al3+
C、向1 mol·L—1明矾溶液50mL中滴入数滴0.1mol·L—1Ba(OH)2溶液
Al3++2SO42—+2Ba2++3OH—=Al(OH)3↓+2BaSO4↓
D、将少量SO2气体通入NaClO溶液中:SO2+H2O+ ClO—=SO42—+Cl—+2H+
6、物质的量浓度相同的NaCl溶液和NaClO溶液中,下列关系正确的是
A、NaCl溶液中离子的总浓度和NaClO溶液中离子的总浓度相等
B、NaCl溶液中离子的总浓度大于NaClO溶液中离子的总浓度
C、NaCl溶液中离子的总浓度小于NaClO溶液中离子的总浓度
D、NaCl溶液的pH大于NaClO溶液的pH
7、两个硫酸分子可以脱去一分子水生成焦硫酸(H2S2O7)。已知硫酸的分子中有4个硫氧键,则焦硫酸分子中硫氧键的数目是
A、 4 B、 6 C 、 7 D、 8
8、一定条件下,4g和14g的混合气体体积为448mL,相同状况下,8gA和17gB的混合气体体积为672mL,A、B可能是下列各组的
A.乙烯和乙炔 B.乙炔和苯 C.甲烷和甲醇 D.环己烷和1—丁烯
二、选择题(本题包括8小题,每小题4分,共32分。每小题只有一个或两个选项符合题意。若正确答案包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给4分,但只要选错一个,该小题就0分。)
 9.Inorganic
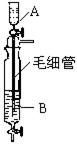
Syntheses一书中,有一如右图所示的装置,用以制备某种干燥的纯净气体。该装置中所装的药品正确的是
9.Inorganic
Syntheses一书中,有一如右图所示的装置,用以制备某种干燥的纯净气体。该装置中所装的药品正确的是
A、A中装浓硫酸,B中装浓盐酸
B、A中装浓盐酸,B中装浓硫酸
C、A中装氢氧化钠浓溶液,B中装浓氨水
D、A中装浓氨水,B中装氢氧化钠浓溶液
10.某温度下,某容积恒定的密闭容器中发生如下可逆反应: CO(g)+H2O(g)![]() H2(g)+CO2(g)
H2(g)+CO2(g) ![]() H>0当反应达平衡时,测得容器中各物质均为n mol,欲使H2的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是
H>0当反应达平衡时,测得容器中各物质均为n mol,欲使H2的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是
A、升高温度 B、加入催化剂
C、再加入n molCO和n molH2O
D、再加入2n molCO2和2n molH2
11、下列各组中,两种气体的分子数一定相等的是
A.质量相等,密度不等的C2H4和N2 B.温度相同,体积相同的O2和N2
C.压强相同,体积相同的O2和N2 D.体积相等,密度相等的CO和C2H4
12、经硫酸酸化的高锰酸钾溶液和过氧化氢溶液混合后,发生反应的化学方程式如下:2KMnO4 + 5H2O2 + 3H2SO4 = 2MnSO4 + K2SO4 + 5O2↑+ 8H2O 下列对此反应的分析正确的是
A.过氧化氢作还原剂,硫酸作氧化剂 B.过氧化氢既作还原剂又作氧化剂
C.过氧化氢作还原剂,硫酸起酸化作用 D.高锰酸钾作氧化剂,氧气为氧化产物
13、第ⅡA的铍在一定条件下可形成化合物Na2BeO2。下列有关铍及其化合物的叙述正确的是
A、氧化铍不能溶于盐酸 B、氢氧化铍易溶于水
C、单质铍可溶于氢氧化钠溶液生成氢气 D、Na2BeO2溶液呈碱性
14、能正确表示下列化学反应的离子方程式的是
A、稀硝酸与锌的反应:2H+ + Zn = H2↑ + Zn2+
B、二氧化氮通入水中:3NO2 + H2O = 2H+ + 2NO3— + NO
C、过氧化钠和水反应:Na2O2 + H2O = 2Na+ + 2OH—+O2↑
D、过量的二氧化碳通入少量澄清石灰水中:CO2 + OH— = HCO3—
15、膦(PH3)又称为磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含有。它的分子是三角锥形,以下关于PH3的叙述正确的是
A.PH3是非极性分子 B.PH3分子中有未成键的电子对
C.PH3是一种强氧化剂 D.PH3分子中的P—H键是极性键
16.用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U型管的质量差,实验测得m(H)∶m(O)>1:8。下列对导致这一结果的原因的分析中,一定错误的是
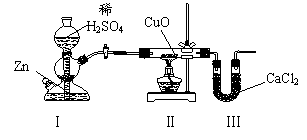 A.Ⅰ、Ⅱ装置之间缺少干燥装置
A.Ⅰ、Ⅱ装置之间缺少干燥装置
B.Ⅲ装置后缺少干燥装置
C.Ⅱ装置中玻璃管内有水冷凝
D.CuO没有全部被还原
参考答案
1、 C
2、 C
3、 C
4、 C
5、 B
6、 B
7、 D
8、 C
9、 B
10.D
11.AD
12.CD
13.CD
14.BD
15.BD
16.D