高考热点专题测试卷:专题九 化学实验
说明:本试卷共分两卷,第Ⅰ卷为选择题,把正确答案序号填在题后答题卡内.第Ⅱ卷为非选择题,直接在本卷内作答.
第Ⅰ卷(共83分)
一、选择题:每小题3分,5小题共15分.每小题只有一个选项正确.把正确选项的代号填在题后答题卡中.
1.可用滴瓶存放较长时间的试剂是( )
A.溴水 B.![]() 溶液 C.NaOH溶液 D.浓盐酸
溶液 C.NaOH溶液 D.浓盐酸
2.向某待测无色溶液中滴入酚酞试剂,结果溶液呈红色,由此可得出的结论是( )
A.溶液中溶有NaOH B.溶质可能是![]()
C.溶液中一定不含![]() 离子 D.溶液呈碱性
离子 D.溶液呈碱性
3.有一NaOH溶液长期存放在试剂瓶中,结果瓶底溶液呈浑浊状,其原因主要是( )
A.吸收空气中![]() 所致 B.NaOH与玻璃作用,而后吸收
所致 B.NaOH与玻璃作用,而后吸收![]() 所致
所致
C.NaOH中含有![]() D.溶液中的水分部分蒸发
D.溶液中的水分部分蒸发
4.欲量取![]() ,最好选用( )
,最好选用( )
A.酸式滴定管 B.10 mL移液管
C.50 mL量筒 D.100 mL量筒
5.先将甲物质放于托盘天平右盘进行称量,再将乙物质放在左盘进行称量,若两次都使用了游码,且砝码和游码的读数均相等,甲、乙两物质的质量( )
A.小于 B.等于 C.大于 D.不能确定
二、选择题:本题包括8小题,每小题4分,共32分.每小题有一个或二个选项符合题意.若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给4分,但只要选错一个,该题就为0分.把正确选项的代号填在题后答题卡中.
6.①加热时试管中盛液量不超过1/3容积;②制溴苯时圆底烧瓶上方要安装一根长玻璃导管;③加热时烧杯内盛液量不超过![]() 容积;④用高锰酸钾制氧气时试管中靠近试管口处要塞一团棉花;⑤制乙烯时要在烧瓶里放些碎瓷片.在这五种实验操作中,主要是为了保证不使液体喷出的是( )
容积;④用高锰酸钾制氧气时试管中靠近试管口处要塞一团棉花;⑤制乙烯时要在烧瓶里放些碎瓷片.在这五种实验操作中,主要是为了保证不使液体喷出的是( )
A.①②④ B.①③④ C.①③⑤ D.①②⑤
7.下列操作,不妥的是( )
A.用托盘天平称量氢氧化钠时,需在左、右托盘上各放一块质量相等的滤纸.
B.用25 mL滴定管量取25 mL的氢氧化钠溶液时,需将调好零点的滴定管内所有液体放出.
C.用10 mL移液管量取10 mL氢氧化钠溶液时,不必把残留尖嘴部分的液体用吸球吹出.
D.用量筒量取一定量体积的液体配制一定物质的量浓度的溶液时,不用将量筒用蒸馏水洗涤后再移入容量瓶.
8.酒精灯不易点燃或燃烧不好,可能的原因有:①酒精灯不用时没盖上灯帽.②灯芯外露部分已烧焦炭化.③灯内的酒精只占灯容积的1/2.叙述正确的是( )
A.①②③ B.只有① C.①② D.只有②
9.下列实验操作中,主要不是从安全因素考虑的是( )
A.酒精灯在不使用时,必须盖上灯帽.
B.给试管里的固体加热时,试管口应略向下倾斜,外壁干燥后再预热.
C.给试管里的液体加热时,试管口应略向上倾斜(约45°角),外壁干燥后再预热.
D.用氢气还原氧化铜时,应先通一会儿氢气,再加热氧化铜.
10.下列各组溶液,只用组内溶液互相混合的方法就可鉴别的是( )
A.NaOH、![]() 、
、![]() 、
、![]()
B.![]() 、
、![]() 、
、![]() 、NaCl
、NaCl
C.NaCl、![]() 、
、![]() 、HCl
、HCl
D.![]() 、
、![]() 、
、![]() 、HCl
、HCl
11.下列有关使用托盘天平的叙述,不正确的是( )
A.称量前先调节托盘天平的零点;
B.称量时左盘放被称量物,右盘放砝码;
C.潮湿的或具有腐蚀性的药品,必须放在玻璃皿里称量,其他固体药品可直接放在天平托盘上称量;
D.用托盘天平可以准确称量至0.01 g;
E.称量完毕,应把砝码放回砝码盒中.
12.有些固体药品长期存放时,若因密封不严,则瓶内会逐渐积聚一定量液体,以下各组中的每种药品都有可能出现这种现象的一组是( )
A.无水硫酸铜,生石灰,烧碱 B.红磷,烧碱,无水氯化钙
C.纯碱,芒硝,熟石灰 D.氯化镁,明矾,氯化钠
13.下列实验操作,正确的是( )
①中和滴定时,用标准液润洗滴定管,用待测液润洗移液管和锥形瓶,并在锥形瓶内滴入l mL指示剂
②配制物质的量溶液时,将称量好的溶质溶于盛有适量水的烧杯中,待溶解后立即倾入容量瓶中,继续进行洗涤和定容
③用NaOH溶液和可溶性铝盐溶液大量制取![]()
④制取![]() 时,吸取NaOH溶液的胶头滴管的末端应插入
时,吸取NaOH溶液的胶头滴管的末端应插入![]() 溶液中,再逐渐注入NaOH溶液
溶液中,再逐渐注入NaOH溶液
⑤蔗糖加稀硫酸水解后,将水解液滴入银氨溶液,水浴加热后即可见银镜
A.①②③ B.②⑤ C.④ D.以上都不正确
三、选择题:本题包括9个小题,每小题4分,共36分.每小题只有一个选项符合题意.把正确选项的代号填在题后答题卡中.
14.为了区别五瓶无色溶液:HCl、![]() 、
、![]() 、NaCl、
、NaCl、![]() ,四位学生都没有用酒精灯,三位学生另用了试剂,一位学生没有另用任何试剂.其中操作步骤一定最少的是( )
,四位学生都没有用酒精灯,三位学生另用了试剂,一位学生没有另用任何试剂.其中操作步骤一定最少的是( )
A.甲另用了酚酞试剂 B.乙另用了NaOH溶液
C.丙另用了石蕊试液 D.丁不另用任何试剂
15.将![]() 溶到100mL水中,要求计算溶液的物质的量浓度.(O、Na的原子量已知)( )
溶到100mL水中,要求计算溶液的物质的量浓度.(O、Na的原子量已知)( )
A.以上所给条件已经足够 B.还必须再给出放出气体的体积
C.还必须再给出生成溶液的体积 D.还必须已知![]() 的密度
的密度
16.在实验室欲用托盘天平称量某物质的质量,称量前发现天平指针偏向左侧(托盘内无任何其他物质),这时可考虑进行的操作有:①使游码移至标尺的零刻度处;②旋转螺母,调节天平至平衡;③将左右托盘对调;其正确的是( )
A.①或② B.① C.③①② D.①或③
17.现有磷酸钠、盐酸、碳酸钾和氯化钡4种溶液,分别盛于1~4号的4个试剂瓶中,但不知道哪一个试剂瓶盛何种溶液.若取2号和3号的溶液混合时,则有气体产生;将1号和3号的溶液混合时,则有沉淀产生.由此可知盛磷酸钠溶液的试剂瓶的编号是( )
A.1号 B.2号 C.3号 D.4号
18.下列物质的制备过程中,要经过5个步骤的是( )
A.以黄铁矿、空气、水、磷灰石为原料,制取过磷酸钙
B.以海水、盐酸、石灰石为原料,提炼金属镁
C.以电石、食盐、水为原料制聚氯乙烯
D.以氨、空气、水为原料制硝铵
19.下列实验操作会导致实验结果偏低的是( )
(1)配制100 g 10%的![]() 溶液,称取
溶液,称取![]() 晶体溶于90 g水中
晶体溶于90 g水中
(2)测定![]() 晶体中结晶水的百分含量时,所用的晶体已经受潮.
晶体中结晶水的百分含量时,所用的晶体已经受潮.
(3)配制一定摩尔浓度的![]() 溶液,定容时仰视容量瓶的刻度线.
溶液,定容时仰视容量瓶的刻度线.
(4)用98%的浓![]() 配制1∶5稀
配制1∶5稀![]() 时,把14 g98%的浓
时,把14 g98%的浓![]() 溶于54 g水中
溶于54 g水中
A.只有(1) B.只有(2)
C.(2)(3)(4) D.(1)(3)(4)
20.根据以下叙述制备氯化铜
先将浓盐酸用蒸气加热至80℃左右,慢慢加入含有FeO杂质的CuO粉,充分反应,使其溶解,发生以下反应
![]()
![]()
已知pH≥9.6时,![]() 可析出
可析出![]() pH≥6.4时,
pH≥6.4时,![]() 可析出
可析出![]()
pH=3~4时,![]() 可析出
可析出![]()
在除去溶液中的![]() 时,可采用的方法是( )
时,可采用的方法是( )
A.可直接加碱,调整溶液的pH≥9.6
B.加入纯铜粉,将![]() 还原为Fe
还原为Fe
C.先将![]() 氧化成
氧化成![]() ,再调整溶液pH至3~4
,再调整溶液pH至3~4
D.通入![]() 使
使![]() 直接沉淀
直接沉淀
21.在一定条件下,萘可以被硝硫混酸硝化生成二硝基物,它是1,5二硝基萘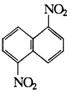 和1,8-二硝基萘
和1,8-二硝基萘 的混合物,后者可溶于质量分数大于98%的硫酸,而前者不能.利用这一性质可以将这两种异构体分离.
的混合物,后者可溶于质量分数大于98%的硫酸,而前者不能.利用这一性质可以将这两种异构体分离.
将上述硝化产物加入适量的98%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1,8-二硝基萘,应采用的方法是( )
A.蒸发浓缩结晶 B.向滤液中加水后过滤
C.用![]() 溶液处理滤液 D.将滤液缓缓加入水中
溶液处理滤液 D.将滤液缓缓加入水中
22.某溶液含有较多的![]() 和少量的
和少量的![]() ,若用该溶液制取芒硝,可供选择的操作有
,若用该溶液制取芒硝,可供选择的操作有
①加适量![]() 溶液,②加金属钠,③结晶,④加过量NaOH,⑤加强热脱结晶水,⑥过滤.正确的操作步骤是( )
溶液,②加金属钠,③结晶,④加过量NaOH,⑤加强热脱结晶水,⑥过滤.正确的操作步骤是( )
A.②⑥③ B.④⑥①③ C.④⑥③⑤ D.②⑥①③⑤
答题卡
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| 分值 | 3分 | 3分 | 3分 | 3分 | 3分 | 4分 | 4分 | 4分 | 4分 | 4分 | 4分 |
| 选项 | |||||||||||
| 题号 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 |
| 分值 | 4分 | 4分 | 4分 | 4分 | 4分 | 4分 | 4分 | 4分 | 4分 | 4分 | 4分 |
| 选项 |
第Ⅱ卷(共67分)
四、本题包括2小题,共12分
23.(6分)设计最佳方案,用24 g KCl和一定量的![]() 制取
制取![]() (不同温度下KCl、NaCl、
(不同温度下KCl、NaCl、![]() 、
、![]() 在水中的溶解度请查溶解度表).
在水中的溶解度请查溶解度表).
24.(6分)实验室制备少量碘乙烷:将红磷粉末放入乙醇里,在不断振荡下逐次加入细粒的![]() ,则有反应:
,则有反应:
![]()
![]()
![]()
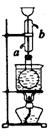
待反应缓和后用下图装置进行水浴加热约半小时,反应可基本完成,这时反应液中已无固体颗粒![]() 和红磷,然后要加入一些物质X,并拔出直立冷凝管,装上附有60°弯玻璃管的瓶塞;将导管接于横放的冷凝管上,水浴加热蒸馏出粗制的碘乙烷,此粗产品中混有乙醇并溶有
和红磷,然后要加入一些物质X,并拔出直立冷凝管,装上附有60°弯玻璃管的瓶塞;将导管接于横放的冷凝管上,水浴加热蒸馏出粗制的碘乙烷,此粗产品中混有乙醇并溶有![]() (纯碘乙烷为无色难溶于水的液体,沸点72.3℃)
(纯碘乙烷为无色难溶于水的液体,沸点72.3℃)
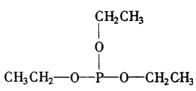
(1)![]() 应是哪一类有机物?写出其结构简式.
应是哪一类有机物?写出其结构简式.
(2)物质X可能是什么?为什么要用它?
(3)装置中竖直冷凝管有何作用?冷凝水从________口进,________口出.
(4)怎样除去粗制品中的乙醇和碘?(指出加入的试剂和操作名称)
五、本题包括2小题,共18分
25.(9分)某化学课外小组用海带为原料制取了少量碘水.现用![]() 从碘水中萃取碘并用分液漏斗分离两种溶液.其实验操作可分解如下几步:
从碘水中萃取碘并用分液漏斗分离两种溶液.其实验操作可分解如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50 mL碘水和![]() 加入分液漏斗中,并盖好玻璃塞;
加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时施开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层水溶液;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
H.静置、分层.
就此实验,完成下列填空:
(1)正确操作步骤的顺序是:(用上述各操作的编号字母填写)________→_______→________→A→G________→E→F
(2)上述E步骤的操作中应注意________________.上述G步骤操作的目的是______
_________.
(3)能选用![]() 从碘水中萃取碘的原因是_______________.
从碘水中萃取碘的原因是_______________.
(4)下列物质,不能作为从溴水中萃取溴的溶剂的是________.
A.热裂汽油 B.苯 C.酒精 D.正庚烷
26.(9分)有常用玻璃仪器组成的下列六种实验装置(根据需要可在其中加入液体或固体)

(1)能用做干燥二氧化硫气体的装置有________(填代号,下同)
(2)既能用于收集氯气又能用于收集一氧化氮气体的装置有________
(3)在氯气和铁反应实验中,能添加在制气和化合反应装置之间以除去氯气中氯化氢等杂质气体的装置有________
(4)在乙烯与溴水反应制二溴乙烷的实验中,能添加在制乙烯装置和加成反应装置之间,达到控制气流使其平衡目的的是________
(5)若用C装置做二氧化硫与烧杯中氢氧化钠溶液反应实验,则其中广口瓶的作用是________.
六、本题包括2小题,共17分.
27.(7分)有机物的C、H含量常用燃烧和与CuO灼烧等方法使之生成![]() 和水,测它们的质量求得有机物中碳和氢的百分含量,现有某固态有机物在加热情况下鼓入足量的氧气使其完全燃烧,今有如下仪器.
和水,测它们的质量求得有机物中碳和氢的百分含量,现有某固态有机物在加热情况下鼓入足量的氧气使其完全燃烧,今有如下仪器.
(1)为确定某固体有机物的最简式(实验式)下述仪器中最少需要的种类有________种,它们是________,其中要一前一后用两次的是________,(填仪器编号)其作用前者为________;后者为________.但为完成测定还缺少的一种重要仪器名称是________.

(2)为确定固体有机物是烃还是其含氧衍生物,实验依据是________.
(3)为确定其分子式还需知道下述中的
A.熔、沸点 B.定温、定压下蒸气密度
C.固定有机物的体积 D.重要的化学性质
28.(10分)某化学课外小组设计了如下图所示的实验装置,进行气体性质实验.图中箭头表示气体流向.A表示一种纯净、干燥的气体,B是另一种气体,反应进行一段时间后,装置乙中有红棕色气体生成.实验中所用的药品和干燥剂只能从下列物质中选取:![]() 、
、![]() 、
、![]() 、
、![]() 、NaCl、无水
、NaCl、无水![]() 、
、![]() 、碱石灰等固体和
、碱石灰等固体和![]() 、蒸馏水.
、蒸馏水.
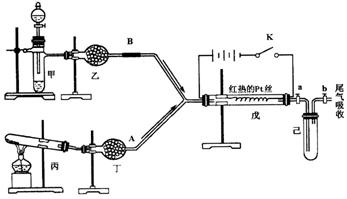
根据图中装置和反应现象请回答:
(1)丙中发生反应的化学方程式为______________
(2)丁中的干燥剂应选 ________,不选另一种干燥剂的理由是________.
(3)甲中发生反应的化学方程式为____________________
(4)戊中发生的主要反应的化学方程式为____________________,此反应是(吸热、放热)________反应,可能发生的什么现象可以证明你的判断________.
(5)当乙中充满红棕色气体后,停止给丙加热,并关闭a、b两个活塞,若将已浸入冰水中,则乙中会出现的现象是_______________,简述产生此现象的原因______________.
七、本题包括2小题,共20分
29.(8分)实验室常用燃烧分析法来测定有机物中碳和氢的质量分数,这种方法是用氧化铜作催化剂,在750℃时,用氧气流将样品氧化成![]() 和
和![]() ,再根据
,再根据![]() 和
和![]() 的质量求出有机物中碳和氢的质量分数.现用下列各仪器装置来确定乙炔分子中碳、氢两种元素的质量比.
的质量求出有机物中碳和氢的质量分数.现用下列各仪器装置来确定乙炔分子中碳、氢两种元素的质量比.
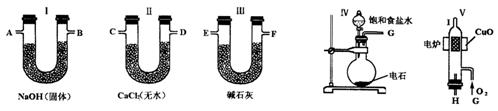
回答下列问题:
(1)若产生的气体由左向右流向,各装置导管的连接顺序是:________接________、________接________、________接________、________接________、________接________.
(2)装置Ⅰ的作用是_______;装置Ⅱ的作用是________;装置Ⅲ的作用是________.
(3)装置Ⅳ中的化学方程式________________________;装置Ⅴ中的化学方程式________________.
(4)实验前称得Ⅰ、Ⅱ两装置的质量分别变为![]() 和
和![]() ,实验完毕,称得Ⅰ、Ⅱ两装置的质量分别变为
,实验完毕,称得Ⅰ、Ⅱ两装置的质量分别变为![]() 和
和![]() ,则乙炔分子中碳原子和氢原子的原子个数比为________(列出算式).
,则乙炔分子中碳原子和氢原子的原子个数比为________(列出算式).
30.(12分)某工厂排出的废水中含有少量的![]() 、
、![]() 、
、![]() 、
、![]() 及一些悬浮的泥沙等不溶物.请你设计一个既经济又合理的方法回收Ag和
及一些悬浮的泥沙等不溶物.请你设计一个既经济又合理的方法回收Ag和![]() (晶体),要求按先后次序写出实验步骤,并说明每一个步骤的实验目的(不必写化学方程式,也不必对回收的Ag和
(晶体),要求按先后次序写出实验步骤,并说明每一个步骤的实验目的(不必写化学方程式,也不必对回收的Ag和![]() 进行洗涤、干燥).
进行洗涤、干燥).
参考答案
1.B 2.D 3.B 4.D 5.A 6.C 7.AB 8.C 9.A 10.AD 11.CD
12.B 13.C 14.C 15.C 16.C 17.D 18.C 19.D 20.C 21.D 22.B
23.本题考查学生称量、加热、溶解、结晶等基本操作,同时要求理论联系实际确定有关化学方程式和计算溶解度.
通过计算知:用50 mL
70℃热水与24 gKCl制几乎饱和的溶液,再用25 mL 70℃热水与![]() 配制成饱和溶液,将此两种溶液混合、搅匀、静止、冷却,将陆续析出
配制成饱和溶液,将此两种溶液混合、搅匀、静止、冷却,将陆续析出![]() 晶体,至20℃时,减压过滤使
晶体,至20℃时,减压过滤使![]() 分离出来.
分离出来.
24.(1)无机酸酯
(2)X可能是沸石(或碎瓷片);防止暴沸
(3)回流冷凝易挥发的反应物:a;b
(4)用足量水洗涤,分液除去乙醇,加稀NaOH溶液,分液除去碘.
25.(1)C→B→D→A→G→H→E→F
(2)使漏斗下端管口紧靠烧杯内壁;及时关闭活塞,不要让上层液体流出;使漏斗内外空气相通以保证(G)操作时漏斗里液体能够流出.
(3)![]() 与水不互溶;而且碘在
与水不互溶;而且碘在![]() 中的溶解度比在水中大很多.
中的溶解度比在水中大很多.
(4)A、C
提示:(4)热裂汽油中含有不饱和气态烃如丙烯、丁烯与溴发生加成反应.
26.(1)AEF (2)AB (3)AF(或AEF) (4)D (5)安全瓶防止碱液倒吸
27.(1)4 a、d、f、h h吸收![]() 吸收
吸收![]() 天平
天平
(2)试样质量=碳元素质量+氢元素质量为烃
试样质量>碳元素质量+氢元素质量为烃的含氧衍生物
(3)B
28.(1)![]()
(2)碱石灰;无水![]() 只能吸水,不能吸收
只能吸水,不能吸收![]() .
.
(3)![]() (或
(或![]() )
)
(4)![]() ;放热;反应开始后断开电键K,铂丝能继续保持红热.
;放热;反应开始后断开电键K,铂丝能继续保持红热.
(5)气体颜色变浅;![]() 发生反应:
发生反应:![]()
![]()
![]() ,属于放热反应,达到平衡后,若降低温度,平衡向右移动,
,属于放热反应,达到平衡后,若降低温度,平衡向右移动,![]() 浓度减少,
浓度减少,![]() 浓度增大,而
浓度增大,而![]() 无色,所以气体颜色变浅.
无色,所以气体颜色变浅.
29.本题考查学生乙炔的制取方法、干燥、氧化原理及产物的吸收测定顺序.由于制得的乙炔气含水对燃烧及产物测定有影响,故制得的乙炔气体必须先干燥,然后再进行题中的催化氧化,乃至测定产物的质量.所以(1)G、E、F、H、I、C、D、A
(2)吸收燃烧产生的![]() 气体;吸收产生的水蒸气;吸收乙炔中的水蒸气.
气体;吸收产生的水蒸气;吸收乙炔中的水蒸气.
(3)![]()
![]()
(4)![]()
30.解析:过程如下:

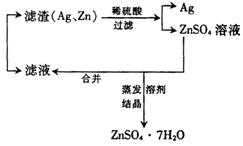
答案:①将废水过滤,目的是除去其中的悬浮泥沙等不溶物;
②往①的滤液中加入足量锌粉,将其中的![]() 置换出来;
置换出来;
③过滤②中的不溶物,滤出Ag和过量的锌粉;
④往③的滤渣中加入过量的稀硫酸,使其中的锌粉转化为![]() 而进入溶液;
而进入溶液;
⑤过滤,将④中没溶解的Ag滤出回收;
⑥将③、⑤得到的滤液合并,蒸发浓缩,使![]() 析出后回收.
析出后回收.