选择题训练(1)
一、选择题(每小题只有一个正确答案)
1.往溴的苯溶液中加入少量铁屑能迅速反应,其过程如下:
3Br2+2Fe=2FeBr3;Br2+FeBr3=FeBr4-+Br+(不稳定);
![]() +Br+→[
+Br+→[![]() ];[
];[![]() ]+FeBr4-→
]+FeBr4-→![]() +HBr+FeBr3;
+HBr+FeBr3;
由上反应可知:![]() +Br2→
+Br2→![]() +HBr中的催化剂为
+HBr中的催化剂为
A Fe B FeBr3 C Br+ D FeBr4-
2.在恒温恒容的容器中进行反应H2![]() 2H―Q,若反应物浓度由0.1mol/L降到0.06mol/L需20s,那么由0.06mol/L降到0.024mol/L,需反应的时间为
2H―Q,若反应物浓度由0.1mol/L降到0.06mol/L需20s,那么由0.06mol/L降到0.024mol/L,需反应的时间为
A、等于18s B、等于12s C、大于18s D、小于18s
3.第二次世界大战期间,某国有支侦查小分队到德国法西斯一座十分隐蔽且又戒备森严的军火厂。上级要求小分队在三天内必须炸毁它,结果他们用十多只涂有化学药剂的老鼠完成了任务。据你推测这种化学药剂是
A、TNT B、KMnO4和H2SO4 C、黑火药和甘油 D、白磷的CS2溶液
4.定向爆破建筑物时,应同时定向切断钢筋和炸碎水泥,除要用适宜的火药以外,还需用 A.氧炔焰 B.铝热剂 C.液氧 D.电弧
5.生石灰中往往含有CaCO3和SiO2杂质,若检验是否存在这两种杂质,最适宜的试剂是 A、氟化氢 B、浓硫酸 C、盐酸 D、苛性钠
6.NCl3的电子式为![]() ,则NCl3与H2O反应时,最初的生成物一定有
,则NCl3与H2O反应时,最初的生成物一定有
A、NH3 B、HNO2 C、HCl D、NH4Cl
7.2007年4月,某地发生了导致四人死亡、一百多人中毒的食用熟牛肉中毒事件,经过对该牛肉的检测,发现某盐的含量比国家允许标准高800多倍,该盐可能是
A、NaCl B、NaNO2 C、NaNO3 D、BaSO4
8.铝和镓的性质相似,如M(OH)3都是难溶的两性氢氧化物。在自然界镓常以极少量分散于铝矿,如Al2O3中。用NaOH溶液处理铝矿(Al2O3)时,生成NaAlO2、NaGaO2;而后通入适量CO2,得Al(OH)3沉淀,而NaGaO2留在溶液中(循环多次后成为提取镓的原料)。发生后一步反应是因为
A、镓酸酸性强于铝酸 B、铝酸酸性强于镓酸
C、镓浓度小,所以不沉淀 D、Al(OH)3是难溶物
9.1999年美国《科学》杂志报道:在40GPa高压下,用激光器加热到1800K,人们成功制得了原子晶体干冰,下列推断不正确的是
A、原子晶体干冰有很高的熔点、沸点,有很大的硬度
B、原子晶体干冰易气化,可用作制冷材料
C、原子晶体干冰硬度大,可用作耐磨材料
D、每摩尔原子晶体干冰中含4mol C―O键
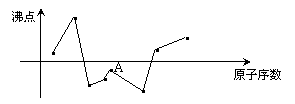 10.右图中曲线表示原子序数在前20号中的某些元素的原子序数
10.右图中曲线表示原子序数在前20号中的某些元素的原子序数
(按递增顺序连续排列)和单质沸点的关系,
其中A点表示的元素是
A、Si B、Al C、F D、S
11.体积相同,浓度均为0.1mol/L的氢氧化钠溶液、氨水分别加水稀释m倍、n倍,溶液pH值都释成9,则m和n的关系为
A.4m=n B. m=n C.m<n D.m>n
12.设NA表示阿伏加德罗常数的数值,下列说法正确的是
A.由2H和18O所组成的水11g,其中所含的中子数为5NA
B.标准状况下,1L庚烷完全燃烧后,所生成气态产物的分子数为7/22.4NA
C.在1L0.1mol/L的HCOOH溶液中,所含HCOO-与HCOOH粒子数之和为0.1NA
D.SiO2晶体中,1mol硅原子与4NA个氧原子形成共价建
13、下列操作中,能使电离平衡H2O![]() H++OH-,向右移动且溶液呈酸性的是:
H++OH-,向右移动且溶液呈酸性的是:
A、向水中加入NaHSO4溶液 B.向水中加入Al2(SO4)3溶液
C.向水中加入Na2CO3溶液 D.将水加热到100°C,使pH=6
14、测定阿伏加德罗常数的实验方法中有一种电解法:以石墨为电极电解CuCl2溶液,当电流为I A,通过时间为t min,阴极增重m g(设一个电子的电量为q C,铜的相对原子质量为M),则阿伏加德罗常数可表示为:
A.2mIt/Mq B.30MIt/mq C..MIt/2mq D 60MIt/mq