2001北京市著名重点中学高考模拟试卷精选化学(第十二模拟)
第Ⅰ卷 (选择题 共83分)
一、选择题(本题包括5小题,每小题3分,共15分。每小题只有一个选项符合题意)
1.以农副产品为原料可制得高分子材料
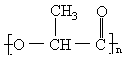 ,它能在乳酸菌作用下迅速降解,有希望用于制造一次性饭盒。有关该高分子的判断正确的是
,它能在乳酸菌作用下迅速降解,有希望用于制造一次性饭盒。有关该高分子的判断正确的是
[ ]
A.相对分子质量一定是偶数
B.相对分子质量一定是奇数
C.由其单体经加聚反应而得
D.属于特殊的多酮糖类
2.下列实验的措施中不正确的是 [ ]
A.容量瓶使用前必须先检查瓶塞是否漏水
B.用棕色的滴瓶盛放新制的浓溴水
C.刚制备完醛酚树脂的试管中的残污可用酒精洗掉,但将污迹加热后却不能用酒精洗掉
D.用12mol/L盐酸可洗去制氯气后瓶中的黑色污迹
![]()
是 [ ]
A.Cl2
B.NaCl
C.NaClO3
D.H2O
4.一定量的镁、铝合金,用足量的盐酸溶解后,再加入过量的NaOH溶液,然后滤出沉淀物,加热灼烧,得白色粉末,干燥后称量,这些粉末与原合金的质量相等,则合金中铝的质量分数是 [ ]
A.20%
B.40%
C.58.6%
D.60%
5.在25℃时,在浓度为1mol/L的(NH4)2SO4、(NH4)
![]()
c(单位为mol/L)。下列判断正确的是 [ ]
A.a=b=c
B.a>b>c
C.a>c>b
D.c>a>b
二、选择题(本题包括8小题,每小题4分,共32分,每小题有一个或两个选择符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个是正确的给2分,选两个且都正确的给4分,但只要选错一个,该小题就为0分)
6.某金属氧化物化学式为M2O3,电子总数为50,每个M离子具有10个电子,已知其中氧原子核内有8个中子,M2O3的相对分子质量为102,M核内的中子数是 [ ]
A.10
B.13
C.21
D.14
7.往P盐溶液中通入过量Cl2,再滴加Ba(NO3)2溶液和稀HNO3,溶液中有白色沉淀,则P盐可能是 [ ]
A.AgNO3
B.Na2CO3
C.Na2SO3
D.NaNO3
8.下列各物质的溶液中通入CO2看不到明显现象的一组是
[ ]
A.Na2SiO3和C6H5ONa
B.CaCl2和NaOH溶液混合
C.CaCl2和Ba(NO3)2
D.NaAlO2和Ca(ClO)2
9.下列各组物质气化或熔化时,所克服的微粒间的作用(力),属同种类型的是 [ ]
A.碘和干冰的升华
B.二氧化硅和生石灰的熔化
C.氯化钠和铁的熔化
D.苯和己烷的蒸发
10.把0.05摩NaOH固体分别加入下列100毫升液体中。溶液的导电性基本不变的是 [ ]
A.自来水
B.0.5摩/升的盐酸
C.0.5摩/升的醋酸
D.0.5摩/升的氨水
11.下列有关稀有气体的描述不正确的是 [ ]
①原子的最外层电子数都有8个 ②其原子与下周期第ⅠA族、ⅡA族的阳离子具有相同的电子层结构③有些稀有气体能跟某些物质反应 ④原子半径比同周期的元素的原子大
A.只有①
B.①和③
C.①和②
D.②和④
12.下列离子方程中,正确的是 [ ]
A.醋酸与小苏打溶液反应:
![]()
B.硫氢化钠的水解:
HS-+H2O ![]() H3O++S2-
H3O++S2-
C.铁与三氯化铁溶液反应:
Fe+Fe3+====2Fe2+
D.铝与氢氧化钠溶液反应:
![]()
13.在2NO2 ![]() N2O4的可逆反应中,下列状态属平衡状态的是
N2O4的可逆反应中,下列状态属平衡状态的是
[ ]
A.混合物中,NO2的百分含量不再改变的状态
B.NO2的分子数与N2O4分子数的比值为2∶1的状态
C.体系的颜色不再发生变化的状态
D.NO2全部转变成N2O4的状态
三、选择题(本题包括9小题,每小题4分,共36分。每小题只有一个选项符合题意。)
14.某主族元素X和Y,已知X的原子序数为a,X2+离子比Y-离子少8个电子,则Y的原子序数是 [ ]
A.a+b
B.a+8
C.a+5
D.a+7
15.通常情况下,磷单质比氮气化学性质活泼,其理由是
[ ]
A.氮气是双原子分子
B.原子半径P>N
C.氮分子中有三个共价键,其键能很大
D.相对原子质量P>N
16.把下列四种X的溶液,分别加进四个盛有10毫升,2摩/升的盐酸的烧杯中,并均加水稀释至50毫升,此时X和盐酸缓和地进行反应,其中反应速度最大的是 [ ]
A.10毫升、2摩/升
B.20毫升、2摩/升
C.10毫升、4摩/升
D.20毫升、3摩/升
17.已知由AgNO3溶液和稍过量的KI溶液制得AgI胶体,当把它和Fe(OH)3胶体相混合时,便析出AgI和Fe(OH)3的混合沉淀。由此可推断 [ ]
A.该AgI胶粒带正电荷
B.该AgI胶粒在电泳时向阴极移动
C.该AgI胶粒带负电荷
D.Fe(OH)3胶粒在电泳时向阳极移动
18.用两根铂丝做电极插入KOH溶液中,再向两个电极上分别通甲烷气和氧气可形成原电池――燃料电地,根据两极反应的实质判断,
![]()
的一极,在下列叙述中正确的是 [ ]
A.阴极:4H2O+2O2+8e=8OH-
B.正极:4H2O+2O2+8e=8OH-
C.阴极:4OH--4e=2H2O+O2↑
D.正极:4OH--4e=2H2O+O2↑
19.1mol氯化钙中含有 [ ]
A.1mol氯化钙分子
B.约6.02×1023个氯离子
C.2mol氯离子
D.约3×6.02×1023个电子
20.二氧化碳中混有少量氯气和氯化氢杂质,为了除去杂质而获得较纯的二氧化碳气体,应选用的最好方法是 [ ]
A.通过NaOH溶液
B.通过饱和NaHCO3溶液
C.通过蒸馏水
D.通过CuSO4溶液
21.硫酸铵在强烈条件下分解,生成氨,二氧化硫,氮气和水,反应中生成的氧化产物和还原产物的物质的量
之比是 [ ]
A.1∶3
B.2∶3
C.1∶1
D.4∶3
22.甲烷分子中的四个氢原子都可以被取代。若甲烷分子中的四个氢被苯基取代,则可得到的分子如右图,对该分子的描述,不正确的是 [ ]
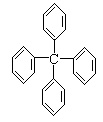
A.分子式为C25H20
B.所有碳原子都在同一平面上
C.此分子属非极性分子
D.此物质属芳香烃类物质
第Ⅱ卷(非选择题 共67分)
四、(本题包括2小题,共20分)
23.(6分)现有一固体混合物,其中可能含有MgCO3、Na2SO4、Ba(NO3)2、AgNO3和CuSO4。它溶于水后得一无色溶液和白色沉淀,此白色沉淀可溶于稀盐酸并冒气泡,而无色溶液遇盐酸无反应,其焰色反应火焰呈黄色。
故一定存在的物质有____;一定不存在的物质有____;可能存在的物质有____。
24.(14分)某化学课外小组所做实验的示意图如图12-1所示。
图中“→”表示气体流向,M是一种纯净而干燥的气体,Y为另一种气体,E内有棕色气体产生。
实验所用的物质,只能由下列物质中选取:Na2CO3、Na2O2、NaCl、Na2O、CaCl2、(NH4)2CO3、碱石灰等固体及蒸馏水。
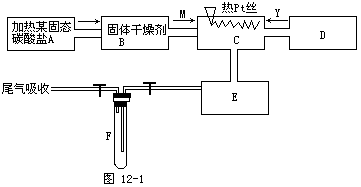
据此实验,完成下列填空:
(1)A中所用装置的主要仪器有____。
(2)B中所选的干燥剂是____,其作用是____。
(3)C中发生的主要反应的化学方程式是____。
(4)制取Y气体的D装置所用的主要仪器是____,制取Y气体的化学方程式是____。
(5)当F中充有一定量气体后,D停止送气,A停止加热,并立即关闭两个活塞,这时若将F汉入冰水中,可看到F中的现象是____,其原因是____。
五、(本题包括2小题,共17分)
25.(9分)甲、乙、丙三位同学设计了一个实验结果各自都认为自己的试样中含有SO42-离子。甲的实验为:

(1)乙认为甲的实验不严谨,因为试样A中若含有____离子(仅填一种),也会有此现象。乙的实验为:
![]()
(2)丙认为乙的实验也不严谨,因为试样B中若含有____(仅填一种),也会有此现象。丙的实验为:
![]()
若丙方案合理,则回答:
(3)其中试剂Ⅰ是____,现象Ⅰ是____。
试剂Ⅱ是____,现象Ⅱ是____。(若你认为丙方案不合理,以上回答可以不填)。
26.(8分)与水的离子积Kw=[H+]・[OH-]相似,FeS饱和溶液中也有离了积KSP=[Fe2+]・[S2-]。已知t℃时FeS的KSP=6.25×10-18,则t℃时饱和FeS溶液的物质的量浓度为____。又知t℃时H2S饱和溶液中[H+]2[S2-]=1.0×10-22,现将适量FeS投入H2S饱和溶液中要使[Fe2+]达到1mol・L-1,则应将溶液的pH调节到____。如已知CuS的离子积KSP=9.1×10-36,现将适量CuS放入H2S饱和溶液中,要使[Cu2+]达到0.01 mol・L-1时,应使该溶液的[H+]达到____。由此说明CuS在一般酸中能否溶解?
六、(本题包括2小题,共15分)
27.(10分)醛可与NaHSO3饱和溶液发生加成反应,生成水溶性的α-羟基磺酸钠:
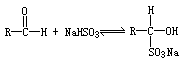
反应是可逆的。在通常条件下有70%~90%的原料向正反应方向转化。
(1)若氯苯中含有杂质苯甲醛,要除去此杂质,可作用的试剂是____,反应的化学方程式为:____;分离的方法是____。
(2)若使CH3-CHOH-SO3Na转化为乙醛,可采用的试剂是____,反应的化学方程式为____,分离的方法是____。
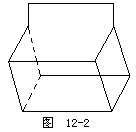
28.(5分)蓝烷的化学式为C10H12,其结构如图12-2,则其一氯代物有____种。
七、(本题包括2小题,共15分)
29.(6分)混有食盐杂质的明矾样品,为求明矾的质量分数,称取样品3.00g,溶于适量蒸馏水中,再加入足量氯化钡溶液,充分反应后,过滤、洗涤、干燥,得干燥的固体2.33g,求样品中明矾的质量分数。
30.(9分)在273℃、202kPa时,将44.8升NH3与128克O2混合后,充入一密闭容器,加Pt并升温至700℃,充分反应后,冷却到室温。
(1)在室温下得到的产物是什么?
(2)若该产物密度为1.44克/毫升,则其百分比浓度和物质的量浓度各为多少?(保留3位有效数字)