高考化学复习大预测卷
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Na 23 Al 27 Mg 24
Cu 64 Fe 56 Cr 52
第一卷(选择题 共64分)
一、单项选择题(本题包括8小题,每小题4分,共32分。每小题只有一个选项符合题意)
1.禽流感是禽流行性感冒的简称,它是一种由甲型流感病毒的一种亚型(也称禽流感病毒)引起的传染性疾病,被国际兽疫局定为甲类传染病。10月25日国家禽流感参考实验室确诊,湘潭县射埠镇湾塘村出现了H5N1亚型高致病性禽流感疫情,在疫区村民家里到处都洒满了石灰,甚至是低矮树木的叶子上都洒上了石灰,很是醒目。根据有关化学知识,判断下列说法不正确的是
A.石灰之所以可以杀灭H5N1亚型高致病性禽流感病毒,是由于石灰与水产生的氢氧化钙显碱性,病毒为蛋白质,可以使蛋白质变性,而使病毒失去活性
B.饱和石灰水中加入生石灰,在温度不变的情况下,pH不变
C.饱和石灰水中加入生石灰,在温度不变的情况下,Ca2+的物质的量不变
D. 给饱和石灰水溶液升高温度,c(OH—)的浓度降低.
2.2005年诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学原理为
①2MoS2 +
7O2 ![]() 2MoO3 + 4SO2;
②MoO3 + 2NH3·H2O = (NH4)2MoO4
+ H2O;
2MoO3 + 4SO2;
②MoO3 + 2NH3·H2O = (NH4)2MoO4
+ H2O;
③(NH4)2MoO4
+ 2HCl = H2MoO4↓+ 2NH4Cl; ④H2MoO4 ![]() MoO3 + H2O;
MoO3 + H2O;
⑤ 用还原剂将MoO3还原成金属钼。 则下列说法正确的是
A.MoS2煅烧产生的尾气可直接排空
B.MoO3是金属氧化物,也是碱性氧化物
C.H2MoO4是一种强酸
D.利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为3:3:2
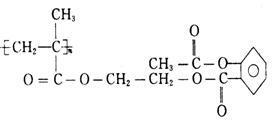
3.奥运吉祥物福娃外材为纯羊毛线,内充物为无毒的聚酯纤维
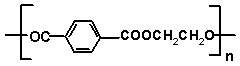
下列说法正确的是
A.羊毛与聚酯纤维的化学成分相同 B.聚酯纤维和羊毛一定条件下均能水解
C.该聚酯纤维单体为对苯二甲酸和乙醇 D.由单体合成聚酯纤维的反应属加聚反应
![]() 4. “绿色化学实验”进课堂,某化学教师为“氯气与金属钠反应”设计了如下装置与操作以替代相关的课本实验。实验操作:钠与氯气反应的装置可作如下图改进,将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是
4. “绿色化学实验”进课堂,某化学教师为“氯气与金属钠反应”设计了如下装置与操作以替代相关的课本实验。实验操作:钠与氯气反应的装置可作如下图改进,将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是
A. 反应生成的大量白烟是氯化钠晶体
B. 玻璃管尾部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气
C. 钠着火燃烧产生苍白色火焰
D. 若在棉球外沿滴一滴淀粉碘化钾溶液,可据其颜色变化判断氯气是否被碱液完全吸收
5.若不断地升高温度,实现"雪花→水→水蒸气→氧气和氢气"的变化。在变化的各阶段被破坏的粒子间的相互作用依次是
A.氢键;分子间作用力;非极性键 B.氢键;氢键;极性键
C.氢键;极性键;分子间作用力 D.分子间作用力;氢键;非极性键
6.肼(N2H4)是火箭发动机的一种燃料,反应时N2O4为氧化剂,生成N2和H2O(g).已知:N2(g)+2O2(g)=N2O4(g); △H=+8.7kJ.mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g); △H=-534.0kJ.mol-1
下列表示肼跟N2O4反应的热化学反应方程式,正确的是
A.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g); △H=-542.7kJ.mol-1
B. 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g); △H=-1059.3kJ.mol-1
C. N2H4(g)+![]() N2O4(g)=
N2O4(g)=![]() N2(g)+2H2O(g); △H=-1076.7kJ.mol-1
N2(g)+2H2O(g); △H=-1076.7kJ.mol-1
D.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g); △H=-1076.7kJ.mol-1
7.下列物质的除杂方式:①SO2中混有的SO3杂质可以让混合气体通过浓硫酸除去;②MnO2中混有的少量有机物,可以用加热的方法除去;③乙烯中混有的SO2气体可以通过溴水除去;④金属铜中含有的少量银和锌可以通过电解精炼的方式除去;⑤KNO3中含有的少量NaCl可以通过重结晶的方法除去,其中合理的是
A.①②④⑤ B. 全部 C. ①②③④ D. ②③④⑤
8.分类方法在化学学科的发展中起到了非常重要的作用。下列分类标准合理的是
① 根据酸分子中含有的H原子个数将酸分为一元酸、二元酸等
② 根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
③ 根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
④ 根据反应中的热效应将化学化学反应分为放热反应和吸热反应
A.①③ B.②④ C.①②④ D.②③④
二、不定项选择题(本题包括8小题,每小题4分,共32分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个该小题就为0分)
9. 漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为:5HClO2 = 4ClO2↑+ H+ + Cl- + 2H2O。向NaClO2溶液中滴加H2SO4,开始反应缓慢,随后反应迅速,其原因是
A.在酸性条件下亚氯酸的氧化性增强 B.溶液中的H+起催化作用
C.ClO2逸出,使反应的生成物浓度降低 D.溶液中的Cl-起催化作用
10.下列离子方程式中错误的是
A.过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
B.NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O
C.苯酚钠溶液中通入少量CO2:![]() -O-+CO2+H2O→
-O-+CO2+H2O→![]() -OH+HCO3-
-OH+HCO3-
D.FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
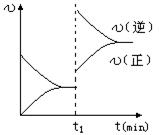 11.右图为某化学反应的速率与时间的关系示意图。在t1时刻升高温度或者增大压强。速率的变化都符合的示意图的反应是
11.右图为某化学反应的速率与时间的关系示意图。在t1时刻升高温度或者增大压强。速率的变化都符合的示意图的反应是
A.2SO2(g)+O2(g) ![]() 2SO3(g); △H<0
2SO3(g); △H<0
B. 4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g); △H<0
4NO(g)+6H2O(g); △H<0
C. H2(g)+I2(g) ![]() 2HI(g); △H>0
2HI(g); △H>0
D. C(s)+H2O(g) ![]() CO(g)+H2(g); △H>0
CO(g)+H2(g); △H>0
12.将饱和一元醇与饱和一元羧酸混合后,再加入浓硫酸加
热,结果只生成碳原子个数分别为4、5、6的三种酯,则下列说法不正确的是
A.若羧酸分子中的碳原子数分别为3个和4个时,则醇分子中碳原子分别为1个和2个
B.若羧酸分子中的碳原子数分别为2个和3个时,则醇分子中碳原子分别为2个和3个
C.甲酸和甲醇在混合物中不能同时存在
D.若羧酸分子中的碳原子数分别为2个和3个时,则醇分子中碳原子分别为3个和4个
13.已知氧元素有16O、18O两种核素,按中学化学知识要求,下列说法正确的是
A.Na2O2与H218O反应时产生18O2气体
B.向2SO2(g)+O2(g)![]() 2SO3(g)的平衡体系中加入18O2,结果18O只出现在产物中
2SO3(g)的平衡体系中加入18O2,结果18O只出现在产物中
C.CH3COOH和CH3CH218OH发生酯化反应时,产物中分子式为H218O
D.用惰性电极电解含有H218O的普通水时,阳极可能产生三种相对分子质量不同的氧分子
14.阿伏加德罗常数约为6.02×1023mol-1。下列叙述正确的是
A.1L0.1mol/L的FeCl3溶液中,H+的数目约为6.02×1015
B. 1mol金刚石中含有C-C键的数目约为6.02×1023
C. 7.8gNa2O2中含有的阴离子数目约为6.02×1022
D. 标准状况下,1L甲醇完全燃烧后生成的CO2分子个数约为(1/22.4)×6.02×1022
15.一定质量的铜和足量的硝酸反应,所放出的气体与标准状况下的氧气1.12L混合后再通入水中,恰好被完全吸收,则铜的质量为
A.3.2g B.4.8g C.6.4g D.10.8g
16.用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.1mol
Cu2 (OH)2CO3后恰好恢复到电解前的浓度和pH(不考虑CO2的溶解)。则电解过程中共转移电子的物质的量为
A.0.4mol B.0.5mol C.0.6mol D.0.8mol
第Ⅱ卷(非选择题 共86分)
三、(本题包括2小题,共22分)
17.(8分)(1)下列实验操作或对实验事实的叙述正确的是___________(填序号))
①用碱式滴定管量取20.00 mL 0.10mol/L KMnO4溶液;
②用托盘天平称取10.50 g干燥的NaCl固体;
③各放一张质量相同的滤纸于天平的两托盘上,将NaOH固体放在左盘纸上称量;
④配制Al2(SO4)3溶液时,加入少量的稀硫酸;
⑤将未经湿润的pH试纸浸到某溶液中,过一会取出与标准比色卡比较测得该溶液的pH;
⑥中和滴定中,锥形瓶用蒸馏水洗净后可直接往其中注入一定量的待测溶液;
(2)回答下列问题.
①某同学将甲烷气体长时间通入溴水中,溴水颜色 (填写“变深”、“变浅”、“不变”)。 其主要原因是 。
②在试管中装有四氯化碳和水两种液体,静置分层后,如果不知道哪一层液体是“水层”,试设计一种最简便的判断方法:
18.(14分) SO2是大气污染物之一,为粗略地测定周围环境中SO2的含量,某学生课外活动小组设计了如下实验装置:
注:单向阀原理说明:当推注射器活塞时,①关闭,②打开;
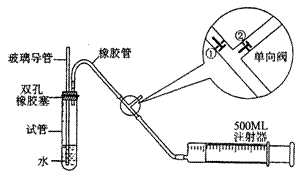 当拉注射器活塞时,①打开,②关闭。
当拉注射器活塞时,①打开,②关闭。
(1)检查该装置的气密性时,先在试管中装入适量的水(保证玻璃导管的下端浸没在水中),然后___________________(填写操作方法)时,将会看到__________(填写实验现象),则证明该装置的气密性良好。
(2)向试管中加入0.0005mol·L-1的碘水1.0mL,用适量的蒸馏水稀释后再加入2~3滴淀粉溶液,配制成溶液A。测定指定地点的空气中SO2的含量时,推拉注射器的活塞反复抽气,A溶液由_________色变为_________色时反应恰好完全进行,此时停止抽气,该反应的化学方程式为_____________________________________________。
(3)我国环境空气质量标准中对每次空气质量测定中SO2的最高浓度限值(mg·m—3):一级标准:0.15 二级标准:0.50 三级标准:0.70。该学生课外活动小组分成第一小组和第二小组,使用相同的实验装置和溶液A,在同一地点、同时测量空气中SO2的含量。当反应恰好完全进行,记录抽气次数如下(假设每次抽气500mL)。请将下表填写完整(计算时保留2倍有效数字):
| 分 组 | 第一小组 | 第二小组 |
| 抽气次数 | 120 | 140 |
| SO2含量/mg·m—3 |
判断该地点的空气中SO2的含量属于________(填数字)级标准,________(“第一”或“第二”)小组的测定结果正确,另一小组实验结果产生较大偏差的原因是(两个小组所用装置和药品均无问题)_________________________________________。
四、(本题包括2小题,共18分)
19.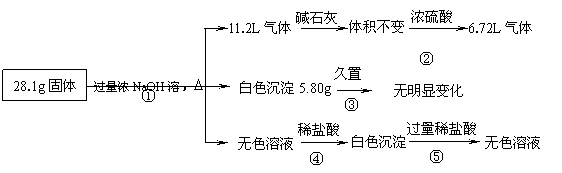 (10分)某固体混合物可能由Al、(NH4)2SO4、MgCl2、AlCl3、FeCl2中的一种或几种组成,现对该混合物作如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):
(10分)某固体混合物可能由Al、(NH4)2SO4、MgCl2、AlCl3、FeCl2中的一种或几种组成,现对该混合物作如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):
回答下列问题:
⑴混合物中是否存在FeCl2 否___(填“是”或“否”);
⑵混合物中是否存在(NH4)2SO4 是___(填“是”或“否”),你的判断依据是 气体通过浓硫酸减少4.4 8L 。
⑶写出反应④的离子反应式: AlO-+H++HO ==Al(OH__ 。
⑷请根据计算结果判断混合物中是否含有AlCl3(说出你的计算依据,不要求写计算过程) 由题中信息可推得一定含有g,所以一定没题中信息可推得一定含有g含含,所以一定没有A有A
lCl 题中信息可推得一定含有g,所以一定没含有A 。
⑸把AlCl3溶液中加热浓缩蒸干,不能得到AlCl3晶体,请你设计一个可行的简易实验方案,怎样从溶液中得到较纯的AlCl3结晶。往浓盐酸后,再加热浓 缩析出晶体
______________________________________________________________________ 。
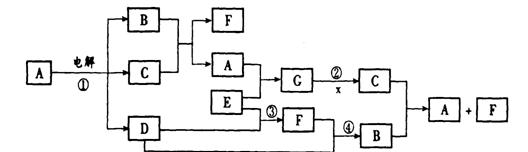 20.(8分)下图是一些常见物质间的转化关系图,图中所有物质含有的元素中只有一种不是短周期元素,所有反应物、生成物及溶液中的水均未标出,反应②中还有3种产物未标出,x是室内装潢材料中产生的主要有害气体之一,G是由四种元素组成的强碱。
20.(8分)下图是一些常见物质间的转化关系图,图中所有物质含有的元素中只有一种不是短周期元素,所有反应物、生成物及溶液中的水均未标出,反应②中还有3种产物未标出,x是室内装潢材料中产生的主要有害气体之一,G是由四种元素组成的强碱。
回答下列问题:
(1)写出下列物质的化学式:B 、C ;
(2)列举两种能氧化x的物质(单质、化合物各一种) 、 ;
(3)写出反应①②的离子方程式:
①
② 。
五、(本题包括1小题,共10分)
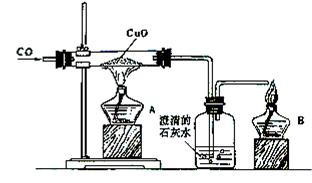 21.(10分)课题式课堂教学是“研究性学习”的方式之一,其基本模式为:提出课题→确定研究方案→解决问题→总结和评价。右图是关于“CO的化学性质”的课题式课堂教学“解决问题”阶段中,甲同学设计的证明“CO具有还原性”的实验装置。
21.(10分)课题式课堂教学是“研究性学习”的方式之一,其基本模式为:提出课题→确定研究方案→解决问题→总结和评价。右图是关于“CO的化学性质”的课题式课堂教学“解决问题”阶段中,甲同学设计的证明“CO具有还原性”的实验装置。
(1)气体验纯后开始进行实验,实验时应先点燃 处
(填“A”或“B”)的酒精灯。
(2)反应一段时间后,可观察到洗气瓶中的现象为 ,加热的玻璃管里的现象为 。
(3)酒精灯B的作用是 。
(4)乙同学提出甲同学设计的装置太复杂,认为可将酒精灯合二为一,去掉B,而将尾气导管口旋转到A的火焰上即可,乙同学的设计是否合理? (填“合理”或“不合理”),理由是
。
(5)丙同学质疑“CO能否使澄清的石灰水变浑浊”,该同学设计CO通入CuO之前,应先通过澄清石灰水,以排除CO与澄清石灰水反应。试对此作出评价,认为丙的设计 (填“必要”或“不必要”),理由是
。
(6)丁同学认为甲同学的设计的装置中的尾气处理还可以有其他的方法,请你为丁同学设计一种合理的尾气处理方法 。
六、(本题包括2小题,共18分)
22.(8分)请认真阅读下列4个反应:
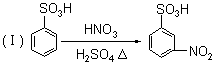
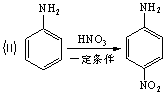
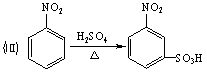
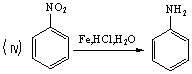
利用这些反应原理,按以下步骤(反应条件及有关试剂已略去)可以从烃A合成甲基橙指示剂。
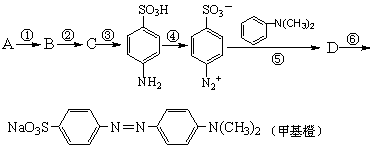
⑴写出A、C、D的结构简式:
A ,C ,D
⑵写出反应①和②的化学方程式:
①
②
 23.(10分)阿司匹林的化学名称为乙酰水杨酸,也叫乙酰基柳酸、醋柳酸,其分子结构如下:
23.(10分)阿司匹林的化学名称为乙酰水杨酸,也叫乙酰基柳酸、醋柳酸,其分子结构如下:
(1)阿司匹林的一种同分异构体中含有苯环和两个羧基,且苯环上只有一个侧链,则阿司匹林的这种同分异构体的结构简式为 。
(2)杨柳中含有一种化学式为C13H18O7的水杨苷。水杨苷在人体内能发生水解反应而生成水杨醇和葡萄糖(反应物和生成物的物质的量均相等)。已知水杨醇遇Fe3+呈紫色,并可被氧化为水杨酸(邻羟基苯甲酸)。试写出水杨醇的结构简式 ,
它不可能具有的化学性质(发生的化学反应)有 。(填序号)。
A.酯化反应 B.消去反应 C.加成反应 D.氧化反应 E.加聚反应 F.还原反应
(3)水杨酸和乙酸酐[(CH3CO)2O]反应制得乙酰水杨酸。试写出该反应的化学方程式 。(有机物写结构简式)
(4)以苯酚为原料合成水杨酸,为阿司匹林的大量生成开辟了广阔的前景。其生产阿司匹林的流程如下:
(分子式为C7H5O3Na)
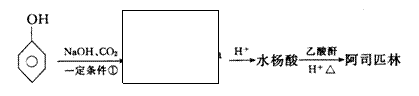 |
写出方框中物质的结构简式(直接写在方框中)并完成反应①的化学方程式 。
(5)为了更好地发挥阿司匹林的药效,人们将其连在高分子载体上,使之在人体内持续水解释放出乙酰水杨酸,称为长效阿司匹林,
|
则该物质1 mol与足量的NaOH溶液
完全反应,消耗的NaOH的物质的量为
mol。
七、(本题包括2小题,共18分)
24.(6分)六价铬对人体有害,含铬废水要经化学处理后才能排放,方法是用绿矾
(FeSO4·7H2O)把废水中的六价铬还原为三价铬离子,再加入过量石灰水,使铬离子转变 为
Cr(OH)3沉淀。其主要反应化学方程式为:
H2Cr2O7+6FeSO4+6H2SO4=3Fe2(SO4)3+Cr2(SO4)3+7H2O,现用上述处理1×104L含铬(+6价)78mg/L的废水,试回答:
(1)处理后,沉淀中除Cr(OH)3外还有_________________(用化学式表示)
(2)需用绿矾多少千克?
25.(12分)CO和CO2都可以合成甲醇: CO+2H2→CH3OH CO2+3H2→CH3OH+H2O
CO、CO2和H2可通过下列反应制备:
A: CH4+H2O(g) →
CO+3H2 B:CO+H2O(g)
→ CO2+H2
反应A的产物合成甲醇时H2过量,反应B的产物合成甲醇时H2不足。为了充分利用原料可将两个反应的产物混合使用。
(1)反应A和反应B的产物气体混合的最佳比例(用同温同压下气体体积比表示)
| x的取值范围 | y 的值或y与x的函数关系 |
(2)设取A的产物与B的产物混合气体67.2L(标准状况),其中CO的体积分数为x ,得到甲醇的物质的量y(纵坐标)随CO体积分数变化的函数关系式并作出图象(假定CO先与H2反应,CO完全反应后,CO2才与H2反应)。