������2005---2006ѧ��ȵ�һѧ������ѧ�����ʲ���
��һ��ѧ����
���Ծ��ֵ�I����ѡ���⣩�͵�II������ѡ���⣩�����֣�ȫ���ܷ�100�֡����ʱ��100���ӡ����Խ���������II���ʹ��һ�����ء�
���ڢ����ѡ���⡡��48�֣�
ע�����
1���ش�I��ǰ����������ڴ�������������Ժš���Ŀ���ƵȺ��֡������øֱʻ�Բ�����д��ȷ������2BǦ����Ϳ���Ժš�
2��ÿС��ѡ����ȷ�𰸺���2BǦ�ʰѴ���϶�Ӧ��ѡ����Ϳ��Ϳ�ڡ�����Ķ�������Ƥ���ɾ�����ѡͿ�����𰸡��罫��д��������ϣ�һ�ɲ����֡�
�����õ������ԭ��������H��1��C��12��N��14��O��16�� Na��23��Al��27��S��32��
Cl��35.5 K��39��Ca��40��Fe��56��Cu��64 I��127����Ba��137��
һ��ѡ�������������12С�⣬ÿС��2�֣���24�֡�ÿС��ֻ��һ��ѡ��������⣩
1������˵����ȷ����
�� A. ú�ĸ����������仯
�� B. ʯ���ѽ����ҪĿ�����Ʊ����������
C. ʯ�ͷ����ܵõ���ͬ�е㷶Χ�IJ���, ÿһ����ֶ��Ƕ������Ļ����
�� D. ú�к��б����ױ��ȣ������ø�����ٷ���ķ��������Ƿ������
2. ��m A + n B ![]() p C�ķ�Ӧ�У�m��n��pΪ�����ʵļ��������ֲ��Cÿ����
p C�ķ�Ӧ�У�m��n��pΪ�����ʵļ��������ֲ��Cÿ����
����a mol/L��Bÿ���Ӽ���1.5a mol/L��Aÿ���Ӽ���0.5a mol/L����m��n��pΪ
A��2��3��2��������������B��2��3��3����������C��1��3��2����������D��3��1��2

3��ijѧ�����ֵ�ƿ����Һ���������������ͼ��ʾ�������й��ˣ�����IJ����У����� ��
A��4��������B��3������
��C��2��������D��1��
4.��NAΪ����٤��������ֵ�������й�˵������ȷ����
�� A��45gˮ�к��е�ˮ��������2.5NA
�� B����״���£�33.6LCO�к��е�ԭ������3NA
�� C��0.5L0.2mol/L��NaCl (aq)�к��е�Na������0.1NA
�� D��1molCH3+��̼�����ӣ��к�������ĿΪ10NA
5.������������ȷ���ǡ����������������������������������������� ���� ��
A�����������ӱ���ԭһ���õ������ĵ���
B����������ԭ��Ӧ�У��ǽ�������һ����������
C��ijԪ�شӻ���̬��Ϊ����̬ʱ����Ԫ��һ������ԭ
D��������Ԫ�ص����Ӳ�һ������������
6. X��Y��Z���ǽ�������XͶ��Z����������Һ��,X�ı�����Z������ X ��Y���ԭ���ʱ��YΪ��صĸ�����X��Y��Z���ֽ����Ļ�����˳��Ϊ���������������� ������ ��
���� A��X>Y>Z�������� B��X>Z>Y�������� C Y>X>Z������D��Y>Z>X
7.���и���������ǿ������Һ�д������棬����Һ����ɫ�����ǣ�������
A��K+��MnO4-��Cl-��SO42-������ B��Na+��AlO2-��NO3-��CO32-
C��Na+��H+��NO3-��Cl-��������D��Na+��SO42-��HCO3-��Cl-
8.�й���ϩ����������������ϩ����ˮ��ɵ��Ҵ�������ϩ�ܷ����Ӿ۷�Ӧ�� ����ϩ������ˮ�����ӳɷ�Ӧ ����ϩ����ɫ��ζ������ˮ�����塡������ȷ���ǣ�------- ������ ��
�� A��ֻ�Тڡ����� B���ٺۡ͢� ���� C���ں͢� ������D���ڢۢ�
9.����4�ֻ�����ֱ�������ܵõ�2�����������----------------- ������ ��
�� ��CH3CH=C(CH3)CH2CH3 ��CH3CH2CH=CHCH2CH3����CH2=C(CH3)CH2CH2CH3
�� ��CH3CH=CHCH(CH3)CH3��������
A���٢ڡ��� B���ۢܡ��� C���٢ۡ����� D���ڢ�
10. �����������л����ʽ�������п��ܻ�Ϊͬϵ���һ���ǡ����������������� ��������
A��16��30��42��56�������������� B��16��28��40��52
��������C��16��32��48��54���������� ����D��16��30��58��72
11. ����ijЩ���ӵļ��鼰����һ����ȷ���ǣ��� ��
A������ϡ���������ɫ���壬������ͨ�����ʯ��ˮ�У���Һ����ǣ�һ����CO32¯
B�������Ȼ�����Һ�а�ɫ�����������ټ����ᣬ��������ʧ��һ����SO42¯
C����������������Һ�����ȣ�������������ʹʪ���ɫʯ����ֽ������һ����NH4+
D������̼������Һ������ɫ�������ټ������ɫ������ʧ��һ����Ba2+
12.��10��ʱij��ѧ��Ӧ����Ϊ0.1 mol/(L•s)�����¶�ÿ����10�淴Ӧ�������ӵ�ԭ����
2����Ϊ�˰Ѹ÷�Ӧ������ߵ�1.6 mol/(L•s)���÷�Ӧ����ʲô�¶��½��У���������
A��30�桡���������������� B��40�桡��������������C��50�桡������������ D��60��
����ѡ�������������8С�⣬ÿС��3�֣���24�֡�ÿС����һ��������ѡ��������⡣����ȷ��ֻ����һ��ѡ���ѡʱ������Ϊ0�֣�����ȷ�𰸰�������ѡ�ֻѡһ������ȷ�ĸ�2�֣�ѡ�����Ҷ���ȷ�ĸ�3�֣���ֻҪѡ��һ������С���Ϊ0�֣�
13.����ʵ������У���ȷ���ǣ�������
A��Ϊ��ʹ�������ʼӿ죬���ò����ڹ�������������裬����Һ������
B���þƾ��Ƹ��Թܼ���ʱ��Ҫ�������ȵ��Թܷ��ھƾ��ƻ����������
C��Ϊ���ٹ������ʵ��ܽ�ɲ��÷��顢�����衢���ȵȷ���
D��Ϊ�����������ʵ��ܽ�ȣ�����ȡ���衢���ȵȴ�ʩ
14. ����˵���д�����ǣ��� ��
A��ԭ�Ӽ������ӵĺ�����Ӳ������ڸ�Ԫ������������
��B��Ԫ�����ڱ��дӢ�B�嵽��B��10�е�Ԫ�ض��ǽ���Ԫ��
��C���������ϡ������ԭ�ӵ���������������8��
D��ͬһԪ�صĸ���ͬλ�ص��������ʺͻ�ѧ������ȫ��ͬ
15.�������ӷ���ʽ�У���д��ȷ���ǣ�������
�� A��̼�������Һ��ϡ���ᷴӦ��Ca(HCO3)2+2H+=Ca2++2H2O+CO2��
�� B���������������������Һ��Ӧ��SiO2+2OH-=SiO32-+ H2O
�� C�����������������Һ��Ӧ��H2SiO3+2OH-=SiO32-+2H2O
�� D������̼������Һ��ͨ�������CO2��CO32-+H2O+CO2=2HCO3-
16.ij���������������¿��Է���ˮ�ⷴӦ������������A��B����A��B����Է���������ȣ������ʿ����ǡ����������������������������������������� (����)
A. �����ǡ���������B.Ӳ֬�������
C. ��������(HCOOC2H5)����������������D.����
17. ��ԭ������11�������ӵ�17����������ݱ��ϵ�������(����)
A.���Ӳ��������ࡡ���� B.ԭ�Ӱ뾶������
C.���������ֵ������D.�ӹ赽�ȸ��۴�-4��-1��
|
�����ʽΪ
�� A. C14H10���������� B. C14H22
����C. C18H30���������� D. C16H26
19.�ڷ�Ӧ3BrF3��5H2O=HBrO3��9HF��Br2��O2��������0.3molH2O����������ˮ��ԭ��BrF3�����ʵ����ǡ��������������� ���� ��
A��0.15mol ������B��0.2mol�� ���� C��0.3mol ������D��0.4mol
20.��ag�����Ͻ��ĩ����������ϡ�����У�����������Һ�м��������NaOH��Һ��ֽ�����ˣ����õ��ij���ϴ�ӡ�������գ����õ�ag����ɫ��ĩ����ԭ�Ͻ���������������Ϊ
����A��70�������������� B��30������������ ��C��47.6�������������� D��52.4��
�ڢ������ѡ��������52�֣�
| �� �� | �� | �� | �� | �� | �� �� | ����� |
| �� �� |
|
|
|
|
|
|
| �÷� | ������ |
�����������2С�⣬��14��
21.��5�֣� ����ֲ��纣���������к��зḻ�ĵ�Ԫ�أ���Ԫ���Ե����ӵ���ʽ���ڡ�ʵ������ �Ӻ�������ȡ����������£�
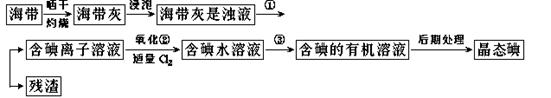 (1)ָ����ȡ��Ĺ������йص�ʵ��������ƣ�������������
��������������
��
(1)ָ����ȡ��Ĺ������йص�ʵ��������ƣ�������������
��������������
��
д�����̢ڡ����йط�Ӧ�����ӷ���ʽ������ ������������������������������ ��
(2)��ȡ��Ĺ����У��ɹ�ѡ����л��Լ���(���� )��
A.�ױ����ƾ����������������������������� B.CCl4����
C.���͡����ᡡ�������������������������� D.�ѻ����͡���
(3)Ϊʹ�������е�����ת��Ϊ����л���Һ��ʵ��������ձ�������������ƿ���ƾ��ơ����ܡ�Բ����ƿ��ʯ�����Լ���Ҫ�ļг���������Ʒ����ȱ�ٵIJ��������������������� ��
22.��9�֣���һ������������ͨ���ۺ�ˮ������Ӧ�����Եõ�������������������ֿ��Ծ����˷�Ӧ���淴Ӧ�����ɿ�����ϸ�����ۡ��������۾��кܸߵķ�Ӧ���ԣ��ڿ�������ײ��������ʱ��ȼ�գ������׳ơ�������������ֱ���ͼ��ʾ�����������װ�ã���ȡ��������������͡�����������ʵ���б���ʹ����ͨ���ۺ�6 mol/L���ᣬ�����Լ���ѡ(װ���б�Ҫ������̨�����С���Ȧ��ʯ�����������豸����ͼ�о�����ȥ)��
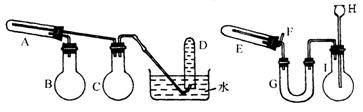
����д���пհף�
(1)ʵ�����ʱ�Թ�A��Ӧ������Լ����������� ����ƿB�������������������� ����ƿC�������� ������������ ��
(2)ʵ��ʱ��U��G��Ӧ������Լ����������� ������©��H��Ӧ������������ ��
(3)����װ���У���ʵ��ʱ��Ҫ���ȵ�������(���������Ӧ����ĸ)�������� ��
(4)��ƿI�з����ķ�Ӧ��ʱҪ������������ͭ��Һ����Ŀ���������������� ��
(5)�Թ�E�з�����Ӧ�Ļ�ѧ����ʽ�������������� ��
(6)Ϊ�˰�ȫ����E���еķ�Ӧ����ǰ����F���ڴ����������������� ��
| �÷� | ������ |
�ġ��������2С�⣬��14��
23.��5�֣�����������Ԫ��A��B��C��D��ԭ������������������A��Cͬ���壬B��C��Dͬ���ڣ�Aԭ�ӵ������������Ǵ�����������3����B�Ƕ�����Ԫ����ԭ�Ӱ뾶��������Ԫ�ء��Իش��������⣺
(1)A��Ԫ�ط����������� ��D��ԭ�ӽṹʾ��ͼ�������������� ��
(2)A��B��C����Ԫ���γɵļ����ӵİ뾶�ɴ�С��˳������������ ��
(3)A��B��C��D�γɵĻ�����B2A2��CD2��D2A��DA2�и�ԭ�Ӷ����������8���ӽṹ���� ������������ (��д����Ļ�ѧʽ )������
(4)CA2��DԪ�صĵ�����ˮ��Һ�з�Ӧ�Ļ�ѧ����ʽ�������������� ��
24.��9�֣��ҹ���������������µ�����ȼ�ϡ��������Ҵ����͡��Ҵ��������ƾ������������ס�С�������Ϊԭ�Ͼ����͡�������Ƴɵġ��Ҵ���һ����ˮ���ټ����������ͺ��γɱ���ȼ���Ҵ����������Ҵ����;��ǰѱ���ȼ���Ҵ������Ͱ�һ�����������γɵij���ȼ�ϡ�����й�֪ʶ���ش��������⣺
(1)��������ʯ�ͷ������õĵͷе�������������е�̼ԭ����һ����C5~C11��Χ�ڣ������飬��ṹ��ʽ����ͬ���칹��ֱ�Ϊ__________��__________��__________��
(2)�Ҵ����ɺ����ۡ�(C6H10O5)n����ũ��Ʒ�����ס�С������Ⱦ����͡�������á���д���ɵ������Ҵ��Ļ�ѧ����ʽ��
������������������������������������������������������������
������������������������������������������������������������
(3) ˾���Ƿ�ƺ�ݳ�����ͨ�����������������м��������������õĻ�ѧ��Ӧ���£�2CrO3(��ɫ)+3C2H5OH+3H2SO4===Cr2(SO4)3(��ɫ)+3CH3CHO+6H2O
������Ӧ�е���������__________����ԭ����__________��
| �÷� | ������ |
�塢�������2С�⣬��12��
25��(4��)д������ϩΪԭ����ȡ���������ķ�Ӧ����ʽ
 |
26��(8��) �ɵ���A�뻯����B���ַ�δ��ɵĻ�����һ�������¿ɰ���ͼ��ʾ����ת����
��ش�
��1����Ӧ�ٵĻ�ѧ����ʽ ����������������������������������������
ʵ���ҽ��и÷�Ӧʱ����Ҫ�����Լ�����������������������������������
��2����Ӧ�ڵ����ӷ���ʽ ����������������������������������������
��3����Ӧ�ܵ����ӷ���ʽ ���������������������������������������� ��
| �÷� | ������ |
�����������2С�⣬��12��
27��(6��) ȡ��״����CH4����O2�Ļ������840mL����ȼ����ȼ�պ�������ù�����ʯ�����գ���ʯ������0.600g�����㣺
��1����ʯ�����պ���ʣ������������״���£�
��2��ԭ���������CH4��O2�������
28����6�֣���ȸʯ��ʯ������Ȼ����ڵ�����̼������ͭ�����ǵĻ�ѧ��ɿɱ�ʾΪ��xCuCO3��yCu(OH)2��x��yΪ��������x��2��y��2��
��1����ȸʯ��ʯ��ֱ���������ᷴӦʱ����ȸʯ���ĵ���������ʵ��������ɵ�CO2�����ʵ���֮��Ϊ4:1��ʯ����Ϊ3:1�����������ǵĻ�ѧ��ɣ�д����ѧʽ��
��ȸʯ__________________________��ʯ��__________________________��
��2�����п�ȸʯ��ʯ������Ʒ��ȡ���ݵ���������Ʒ����һ���м���������ᣬ����CO2 3.36 L����״���£���������һ����Ʒʹ����ȫ�ֽ⣬�õ�CuO 20 g����ͨ������ȷ���û�����п�ȸʯ��ʯ������ʵ���֮�ȡ�
2005��2006ѧ��ȵ�һѧ����ĩ��ѧ����
��һ��ѧ�ο���
һ��ѡ�������������12С�⣬ÿС��2�֣���24�֣�
| �� 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| C | C | A | D | D | C | B | D | A | D | C | C |
����ѡ�������������8С�⣬ÿС��3�֣���24�֣�
| 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| BC | AD | BC | C | AB | A | B | B |
�����������2С�⣬��14��
21����5�֣�.(1)���ˣ���ȡ��Cl2+2I��=I2+2Cl����(2)B������(3)��Һ©����������1�֣�
22����9�֣�(1)��ͨ���ۣ�����ˮ��������ֹ������ (2)���Թ������� 6 mol/L HCl
(3) A��B��E (4)�ӿ�H2�����ٶ� (5)Fe3O4+4H2��3Fe+4H2O (6)����H2���ȣ�����1�֣�
�ġ��������2С�⣬��14��
23����5�֣�����1��O ��Cl��ԭ�ӽṹʾ��ͼ��������2��S2- > O2- > Na+����������������������������
��3��Na2O2,SCl2,Cl2O������4��SO2 +Cl2 + 2H2O = 2HCl + H2SO4����(��1��)
24����9�֣���1�� CH3��CH2��CH2��CH2��CH3�� CH3CH(CH3)CH2CH3��C(CH3)4(��1��)
��2����(C6H10O5)n+nH2O![]() nC6H12O6�� C6H12O6��2CO2+2C2H5OH����2�֣�
nC6H12O6�� C6H12O6��2CO2+2C2H5OH����2�֣�
��3�� CrO3��C2H5OH����(��1��)
�塢�������2С�⣬��12��
25����4�֣�CH2��CH2��H2O ![]() CH3CH2OH��
CH3CH2OH��
2CH3CH2OH��O2![]() 2CH3CHO��2H2O��
2CH3CHO��2H2O��
��2 CH3CHO+O2![]() 2CH3COOH
2CH3COOH
|
CH3COOH+CH3CH2OH ![]() CH3COOC2H5+H2O
����1�֣�
CH3COOC2H5+H2O
����1�֣�
26����8�֣���1��![]() ����þ���������
����þ���������
������2��![]()
������3��![]() ����2�֣�
����2�֣�
�����������2С�⣬��12��
27����1��ʣ����������336mL����2��V��CH4����V��O2����1��4 (��3��)��
28����1����ȸʯ�Ļ�ѧʽΪ CuCO3•Cu(OH)2
��ʯ��Ļ�ѧʽΪ 2CuCO3•Cu(OH)2
����2����ȸʯ��ʯ�����ʵ���֮��Ϊ1:1����2�֣�