高一化学竞赛试题(山东科技版)
(满分100分 时间120分钟)
命题组稿:朱敬华
434300 湖北省公安教研室
可能用到的相对原子质量:
H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32
Cl-35.5 K-39 Fe-56 Cu-64 Zn-65 Ag-108 Ba-137
一、选择题(本题包括18小题,每题2分,共36分,每题有1~2个选项符合题意。多选错选不得分,有两个答案的只选一个且答对者得1分)
1.有关化学用语正确的是 ( )
A. 乙烯的最简式是C2H4 B. 乙醇的最简式是C2H6O
C. 四氯化碳的电子式![]() D. 臭氧的分子式O3
D. 臭氧的分子式O3
2.我国有些煤矿的坑道中具有丰富的可燃性气体。目前已建成利用坑道气的发电厂,这样既充分利用了能源,又保证了煤矿的安全生产,坑道中的可燃性气体是
A.H2 B.CO C.CH4 D. CH4 和CO的混合气体
3.以下关于乙醇、乙酸、酯、油脂、糖类、蛋白质等物质的说法正确的是 ( )
A.都是有机化合物 B.都可溶于水
C.都是纯净物 D.水溶液均呈酸性
4.下列物质使用合理的是
(A) 在制玻璃的原料中再加入Co2O3制成蓝色玻璃 (B)用加酶洗衣粉洗涤毛料服装
(C)用甲醛溶液浸泡海产食品 (D)用酚醛树脂制作高弹力运动鞋
5.由解放军总装备部军事医学研究所研制的小分子团水,解决了医务人员工作时的如厕难题。新型小分子团水,具有饮用量少、渗透力强、生物利用度高、在人体内储留时间长、排放量少的特点。一次饮用125 mL小分子团水,可维持人体6小时正常需水量。下列关于小分子团水的说法正确的是
(A)水分子的化学性质改变 (B)水分子中氧氢键长缩短
(C)水分子间作用力减小 (D)水分子间结构、物理性质改变
6.下列关于物质及其用途的关联中不正确的是( )
A.乙醇—燃料 B.油脂—制造肥皂
C.淀粉—酿酒 D.蛋白质—生产葡萄糖
7.2005年1月,欧洲航天局的惠更斯号探测器首次成功登陆土星的最大卫星——土卫六。科学家对探测器发回的数据进行了分析,发现土卫六的大气层中含有95%的氮气,剩余的气体为甲烷和其他碳氢化合物。下列关于碳氢化合物的叙述正确的是( )
A. 碳氢化合物的通式为CnH2n+2 B. 石油的主要成分是碳氢化合物
C. 乙炔是含碳量最高的碳氢化合物 D. 碳氢化合物中的化学键都是极性键
8.对可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述正确的是 ( )
4NO(g)+6H2O(g),下列叙述正确的是 ( )
A. 达到化学平衡时,4![]() 正(O2)=5
正(O2)=5![]() 逆(NO)
逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C. 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D. 化学反应速率关系是:2![]() 正(NH3)=3
正(NH3)=3![]() 正(H2O )
正(H2O )
9.某同学在做苯酚的性质实验时,将少量溴水滴入苯酚溶液中,结果没有发生沉淀现象,他思考了一下,又继续在反应混合液中滴入足量的氢氧化钠溶液,此时他发现
(A) 溶液中仍无沉淀 (B) 溶液中产生白色沉淀
(C) 先产生沉淀后沉淀溶解 (D) 溶液呈橙色
10、食用味精的主要成分是谷氨酸钠,它对应的氨基酸是谷氨酸,谷氨酸可以从下列哪种食物的消化过程中生成( )
A.葡萄糖 B.淀粉 C.油脂 D.蛋白质.
 11、2004年7月德俄两国化学家共同宣布,在高压下氮气会发生聚合得到高聚氮,这种高聚氮的N-N键的键能为160kJ/mol(N2的键能为942kJ/mol),晶体片段结构如右图所示。又发现从N2可制取出N5、N3。含N5+离子的化合物及N60、N5极不稳定。则下列说法错误的是
11、2004年7月德俄两国化学家共同宣布,在高压下氮气会发生聚合得到高聚氮,这种高聚氮的N-N键的键能为160kJ/mol(N2的键能为942kJ/mol),晶体片段结构如右图所示。又发现从N2可制取出N5、N3。含N5+离子的化合物及N60、N5极不稳定。则下列说法错误的是
(A)按键型分类,该晶体中含有非极性共价键
(B)含N5+离子的化合物中既有离子键又有共价键
(C)高聚氮与N2、N3、N5、N5+、N60互为同素异形体
(D)这种固体的可能潜在应用是烈性炸药或高能材料
12.有编号为1、2、3、4的四瓶无色液体,仅知道是苯、甲苯、氯苯和二甲苯中的分别一种,现在要求甲、乙、丙、丁四位同学进行鉴别,而且每人只鉴别两瓶,告诉学生两瓶鉴别都正确得满分,只有一瓶正确的可以及格。四位同学的结果如下:
| 甲 | 1号为甲苯 | 4号为二甲苯 | 老师评价:四位同学都及格,但是没有一个满分。 |
| 乙 | 1号为氯苯 | 3号为甲苯 | |
| 丙 | 1号为苯 | 2号为甲苯 | |
| 丁 | 4号为甲苯 | 2号为氯苯 |
根据实验结果及老师的评价,以下对四瓶无色液体的成分判断正确的是
(A)1号是苯 (B)2号是二甲苯 (C)3号是氯苯 (D)4号是甲苯
13.生活中的一些问题常涉及到化学知识,下列叙述正确的是( )
.... A.糯米中的淀粉一经发生水解反应,就酿造成酒
.... B.我们所吃的豆腐中主要含有蛋白质
.... C.棉花和蚕丝的主要成分都是纤维素
.... D.“非典”元凶冠状病毒是一种油脂
14.下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是
A. NH4Cl![]() NH3+HCl
NH3+HCl
B. NH3+CO2+H2O =NH4HCO3
C. 2NaOH+Cl2=NaCl+NaClO+H2O
D. 2Na2O2+2CO2=2Na2CO3+O2
15.由—CH3,—OH,—COOH,—C6H5四种基团两两组合而成的有机化合物中,其中水溶液能使石蕊试剂变红的有 (A)2种 (B)3种 (C)4种 (D)5种
16.有关化石燃料的说法正确的是 ( )
A. 化石燃料是可再生的,因此在地球上的蕴藏量也是无限的
B. 化石燃料虽然在地球上的蕴藏量有限,但形成化石燃料的速率相当快,所以化石燃料相当于无限的
C. 化石燃料的形成是非常复杂的,所需时间也很长,但化石燃料在地球上的蕴藏量是无限的
D. 化石燃料在地球上的蕴藏量是有限的,而且又都是经过亿万年才能形成的非再生资源
17.加拿大阿尔贡天文台在星际间发现了HC9N链状分子,其结构式为:CH≡C-C≡C-C≡C-C≡C-C≡N,这是人类发现的最重星际有机分子,有关该分子的说法不正确的是
(A)该物质属于不饱和烃
(B)该分子碳、氮原子均满足八电子结构
(C)该分子所有原子处在一条直线上
(D)1mol该物质在一定条件下可与8molH2发生加成反应
18. 在沥青中含稠环芳香烃,其中偶数个苯环的可视为同系物。如:

此顺推还有D、E、F……等,在该系列化合物中含碳的最大质量分数是:
(A)100% (B)93.75% (C)56% (D)97.3%
二、填空和简答题(本题共包括6小题,共35分)
19.(4分)酚酞是常用的酸碱指示剂,(1)酚酞的化学式为: 。
(2)从结构上看酚酚可看作【 】
A 烯烃 B 芳香族化合物 C 醇类物质
D 酚类物质 E 酯类物质
20.(4分)某种炸药的化学式为C8N8O16,据信是迄今最烈性的非核爆炸品。
(1)写出它的爆炸反应方程式。
(2)解释它具有强烈爆炸性的原因。
21.(6分)被称为“魔棒”的荧光棒已成为节日之夜青少年的喜爱之物,其发光原理是利用过氧化氢氧化草酸酯产生能量,该能量被传递给荧光物质后便发出荧光.回答下列问题:
(1)有人说,发光的魔棒不能凑近石油气之类的可燃性气体,否则会导致爆炸,是否正确?说明理由。
(2)通过挤压,使过氧化氢与草酸酯混合反应,导致魔棒发光,一段时间后,光的亮度降低,此时,把魔棒往手心上敲打几下,亮度会重新增大,原因是什么?(提示:草酸酯是一种有较高粘度的有机化合物)
(3)在设计魔棒时,其连续发光的能力在8-12h,如果在发光中途,把它放入冰箱的冷冻室中,发光便会停止或基本停止.把魔棒从冷冻室中取出静止一会儿,它又会连续发光,原因是什么?
22.(5分)请用勒沙特列原理解释如下生活中的常见现象:打开冰镇啤酒瓶把啤酒倒入玻璃杯,杯中立即泛起大量泡沫。
23.(4分)公元前,古埃及国王胡夫的一位厨师不小心把刚熬好的羊油碰翻在灶坑旁,与草木灰合在一起。当他将羊油和草木灰用手捧出去后,洗手时发现洗得特别干净,试解释其原因?
A.升高反应温度;B.增大反应容器内的温度;C.增大反应容器的体积;D.降低反应的温度;E.减小反应容器的压强;F.减小反应容器的体积;
24.(12分)有机物A(C6H8O4)为食品包装纸的常用防腐剂。A可以使溴水褪色。A难溶于水,但在酸性条件下可发生水解反应,得到B(C4H4O4)和甲醇。通常状况下B为无色晶体,能与氢氧化钠溶液发生反应。
(1)A可以发生的反应有 (选填序号)。
① 加成反应 ② 酯化反应 ③ 加聚反应 ④ 氧化反应
(2)B分子所含官能团的名称是 、 。
(3)B分子中没有支链,其结构简式是 ,B的具有相同官能团的同分异构体的结构简式是 。
(4)由B制取A的化学方程式是 。
(5)天门冬氨酸(C4H7NO4)是组成人体蛋白质的氨基酸之一,可由B通过以下反应制取:
| B |
| C |
| 天门冬氨酸 |
天门冬氨酸的结构简式是 。
 三、实验题:(本题包括两小题,共12分)
三、实验题:(本题包括两小题,共12分)
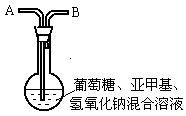
25.(4分)化学中有许多有趣的实验,如下介绍的“蓝瓶子”实验就是一例。
在250 mL平底烧瓶中依次加入2g氢氧化钠、100mL蒸馏水、2g葡萄糖(粉末),振荡使其溶解。滴入4~6滴0.2%的亚甲基蓝溶液,塞上瓶塞(如图),振荡烧瓶,溶液呈蓝色。静置,约3分钟后蓝色消失,变为无色。再次振荡,无色溶液又呈蓝色。可反复多次。为探究是什么原因引起的,有人做了以下实验。
(1)从烧瓶中取出溶液注满一支试管,塞上橡皮塞。试管中的溶液由蓝色变为无色,再振荡试管溶液不能变蓝。
(2)在原烧瓶中经A处鼓入空气,又慢慢变蓝了。静置片刻后,蓝色又消失。再次鼓入空气,又慢慢变蓝。
(3)为了进一步弄清是何种成分引起的,他又继续探索。从A处改通纯净的N2、CO2,都不能使烧瓶中的无色溶液变蓝。把制得的氧气从A处通入,发现上述无色溶液慢慢变为蓝色,到此为止,“蓝瓶子”实验原理有了科学结论,请总结“蓝瓶子”实验的变色原理:
。
26.(8分)某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如右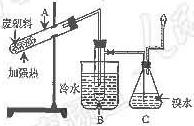 图。加热聚丙烯废塑料得到的产物如下表:
图。加热聚丙烯废塑料得到的产物如下表:
| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
(1)试管A中残余物有多种用途,如下列转化就可可制取高聚物聚乙炔。
A中残留物![]() 电石
电石![]() 乙炔
乙炔![]() 聚乙炔
聚乙炔
写出反应②~③的化学方程式
(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物有 种。
(3)锥形瓶C中观察到的现象 。经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为 。
(4)写出C中逸出的气体在工业上的两种用途 、 。
四、计算题(本题包括三小题,共17分)
27.(8分)吗啡和海洛因都是严格查禁的毒品。
(1) 吗啡分子含C 71.58%、H 6.67%、N 4.91%,其余为O。已知其相对分子质量不超过300。试求:
① 吗啡的相对分子质量。
② 吗啡的分子式。
(2) 已知海洛因是吗啡的二乙酸酯。试求:
① 海洛因的相对分子质量。
② 海洛因的分子式。
28.(9分)某化学反应2A![]() B+D在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
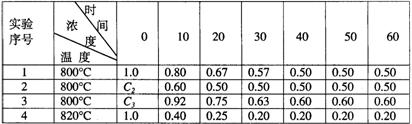
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为______mol/(L·min)。
(2)在实验2,A的初始浓度C2=______mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是 。
(3)设实验3的反应速率为V3,实验1的反应速率为V1,则V3______V1(填>、=、<),且C3______1.0mol/L(填>、=、<)
(4)比较实验4和实验1,可推测该反应是______反应(选填吸热、放热)。理由是
参考答案及评分标准
(满分100分)
一、选择题(本题包括18小题,每题2分,共36分,每题有1~2个选项符合题意。多选错选不得分,有两个答案的只选一个且对者得1分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| D | C | A | A | D | D | B | A | A | D |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| C | A | B | D | A | D | AD | D |
二、问答和填空题:(本题包括6小题,共31分)
19.(1)C20H14O4(2分) (2)BDE(2分)
20..(l)C8N8O16→8CO2+ 4N2(2分) (2) 产物远比反应物稳定;(1分)
分解产物完全是气体,体积膨胀功很大。(l分)
21.(1)不正确.因为是“冷光”而不是明火。(2分)
(2)由于粘度大,反应物不易充分混合,敲打是促进混合,从而促进反应。(2分)
(3)低温使氧化反应变得十分缓慢,恢复常温时反应又加速进行。(2分)
22.(1)啤酒瓶中二氧化碳气体与啤酒中溶解的二氧化碳达到平衡:CO2(气)![]() CO2(溶液),打开啤酒瓶,二氧化碳气体的压力下降,根据勒沙特列原理,平衡向放出二氧化碳气体的方向移动,以减弱气体压力下降对平衡的影响。
CO2(溶液),打开啤酒瓶,二氧化碳气体的压力下降,根据勒沙特列原理,平衡向放出二氧化碳气体的方向移动,以减弱气体压力下降对平衡的影响。
(2)温度是保持平衡的条件,玻璃杯的温度比冰镇啤酒的温度高,根据勒沙特列原理,平衡应向减弱温度升高的方向移动,即应向吸热方向移动,从溶液中放出二氧化碳气体是吸热的,因而,应从溶液中放出二氧化碳气体。
注:压力3分和温度2分,不与勒沙特列原理挂钩不给分。
23.羊油为高级脂肪酸甘油酯,草木灰显碱性,从而发生皂化反应生成可溶于水具有去污作用的物质。
24.(12分)
(1)①③④
(2)碳碳双键,羧基
(3)HO—![]() —CH=CH—
—CH=CH—![]() —OH; CH2=C(COOH)2
—OH; CH2=C(COOH)2
(4)HO—![]() —CH=CH—
—CH=CH—![]() —OH+2CH3OH
—OH+2CH3OH![]()
CH3O—![]() —CH=CH—
—CH=CH—![]() —OCH3+2H2O
—OCH3+2H2O
(5)HO—![]() —CH2—
—CH2—![]()
![]() —OH
—OH
三、实验题:(本题包括2小题,共16分)
25.首先亚甲基蓝被葡萄糖还原,还原后的无色物,又被空气中氧气氧化,又成为亚甲基蓝。反复作用。(答出氧化,还原各得4分)
26.1)CaC2+2H2O→Ca(OH)2+C2H2↑, ![]()
(2)4
(3)棕黄色溶液变无色或褪色; 4.8
(4)合成氨原料,作燃料或有机化工原料(其他合理答案均给分)
四、计算题:(本题包括3小题,共17分)
27.(共8分)
(1) ①285 ②C17H19NO3 (2) ①369 ②C21H23NO5
28.(共9分)
(1)0.013 (2)1.0 催化剂 (3)> > (4)由吸热温度升高时,平衡向右移动。