(新课标)第一学期期末考试高一年级化学试卷(B)
说明:本试卷答题时间为90分钟,试卷满分为100分。
可能用到的相对原子质量:H:1 O:16 C:12 N:14 Na:23 S:32
第一部分选择题(54分)
一、选择题(本题包括10小题,每小题3分,共30分。每小题只有一个选项符合题意。)
1.下列物质是属于非电解质的是………………………………………………………( )
A.NH3 B.(NH4)2SO4 C.Cl2 D.CH3COOH
2.在MgCl2、KCl、K2SO4三种盐的混合溶液中,若K+、Cl-各为1.5mol,Mg2+为0.5mol,则SO42-的物质的量为………………………………………………………………( )
A.0.1mol B.0.5mol C.0.15mol D.0.25mol
3.等质量的钠进行下列实验,其中生成氢气最多的是..……………………………( )
A.将钠投入到足量水中 B.将钠用铝箔包好并刺一些小孔,再放人足量的水中
C.将钠放入足量稀硫酸中 D.将钠放入足量稀盐酸中
4.制印刷电路时常用氯化铁溶液作为“腐蚀液”,发生的反应为2FeCl3+Cu=2FeCl2+CuCl2。向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是烧杯中………………………………………………………………….( )
A.有铁无铜 B.有铜无铁 C.铁、铜都有 D.铁、铜都无
5.自来水常用Cl2消毒,某学生用这种自来水去配制下列物质的溶液,不会产生明显的药品变质问题的是………………………………………………………….……….( )
A.AgNO3 B.FeCl2 C.Na2SO3 D.AlCl3
6.只用一种试剂,可区别Na2SO4、AlCl3、NH4Cl、MgSO4四种溶液,这种试剂是( )
A.HCl B.BaCl2 C.NaOH D.AgNO3
7.某同学在实验报告中有以下实验数据:①用托盘天平称取11.7 g食盐;②用量筒量取5.26 mL盐酸;③用广泛pH试纸测得溶液的pH值是3.5,其中数据合理的是( )
A.① B.②③ C.①③ D.②
8.为了除去FeCl2溶液中混有的少量FeCl3,最好的方法是向此溶液中…………( )
A.通入氯气 B.加入Zn C.加入Fe D.加入Cu
9.除去NaCl中含有的Ca2+、Mg2+、SO42-、HCO3-等离子,通常采用以下四种试剂:①Na2CO3 ②BaCl2 ③NaOH ④HCl。加入试剂合理的操作顺序是………..( )
A.①②③④ B.③①②④ C.④②①③ D.③②①④
10.用98%的浓硫酸(密度为1.84 g/cm3 )配制100 mL l mol/L的稀硫酸。现给出下列仪器(配制过程中可能用到):①100 mL量筒 ②10 mL量筒 ③50 mL烧杯 ④托盘天平 ⑤100 mL容量瓶 ⑥胶头滴管 ⑦玻璃棒,按使用仪器的先后顺序排列正确的是…..( )
A.④③⑦⑤⑥ B.②⑤⑦⑥ C.①③⑤⑥⑦ D.②⑥③⑦⑤⑥
二、选择题(本题共6小题。每题4分,共24分。每小题有1~2个正确选择。若两个选
项只选一个且正确,只给2分;只要错一个零分)
11.把aL含硫酸铵和硝酸铵的混合液分成两等份,一份需用b mol烧碱刚好把氨全部赶出,另一份与氯化钡溶液反应时,消耗c mol氯化钡,由此可知原溶液中N03—的物质的量浓度是(单位:mol·L—1)………………………………………………………( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
12.下列叙述中,正确的是………………………………………………….………( )
A.H2SO4的摩尔质量是98
B.等质量的O2和O3中所含的氧原子数相同
C.等质量的CO与CO2中所含碳原子数之比为11︰7
D.将98g H2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2 mol/L
13.下列叙述中,正确的是……………………………………………..………..( )
A.含金属元素的离子不一定都是阳离子
B.在氧化还原反应中,非金属单质一定是氧化剂
C.某元素从化合态变为游离态时,该元素一定被还原
D.金属阳离子被还原不一定得到金属单质
14.设NA表示阿伏加德罗常数,下列叙述正确的是………………………..……..( )
A.78g Na2O2与足量水充分反应时电子转移数为NA
B.25℃、101.3kPa时,11.2L H2中含有的原子数为NA
C.4℃、101.3kPa时,54mL H2O中含有的分子数为3NA
D.2L 1mol/L Na2SO4溶液中离子总数为3NA
15.在无色强酸性溶液中,下列各组离子能够大量共存的是…………..…...…..( )
A.Cl -、Na+、NO3-、Ca2+ B.NH4+、HCO3-、Cl-、K+
C.K+、Ba2+、Cl-、SO42- D.Cu2+、NH4+、I-、Cl-
16.下列离子方程式的书写正确的是…………..…………………..………….…..( )
A.实验室用大理石和稀盐酸制取CO2:2H+ + CO32- = CO2↑+ H2O
B.铁和稀硝酸反应:Fe + 2H+ = H 2↑+ Fe 2+
C.向AlCl3溶液中加入过量的NaOH溶液:Al3+ + 3OH- = Al(OH)3↓
D.NaHCO3溶液与NaOH溶液反应: OH- + HCO3- = CO32- + H2O
第二部分非选择题(46分)
三、填空题(本题包括2小题,共16分)
17.(8分)(1)0.5 mol H2O的质量为 ,其中含有 个水分子,共有 个原子。
(2)质量都是50 g的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是 _ ,在相同温度和相同压强条件下,体积最大的是 ,体积最小的是 。
(3)在 mL 0.2 mol/L NaOH溶液中含1 g溶质;配制50 mL 0.2 mol/L CuSO4溶液,需要CuSO4·5H2O ____ g。
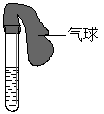 18.(8分)某学生课外活动小组利用右图所示装置分别做如下实验:
18.(8分)某学生课外活动小组利用右图所示装置分别做如下实验:
(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是________________溶液;加热时溶液由红色逐渐变浅的原因是:_________ ____ __ 。
(2)在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是________________溶液;加热时溶液由无色变为红色的原因是 _________ 。
四、推断题(本题包括2小题,共22分)
19.(6分)除去下列物质中所混有的少量杂质,写出有关的反应方程式。
(1)铜粉中混有少量铝粉 ;
(2) FeCl3中混有少量FeCl2 ;
(3)Na2CO3中混有少量NaHCO3 。
20.(16分)已知A.B.C.D分别是AlCl3、BaCl2、FeSO4、NaOH四种化合物中的一种,它们的水溶液之间的一些反应现象如下:
①A+B→白色沉淀,加入稀硝酸,沉淀不溶解。
②B+D→白色沉淀,在空气中放置,沉淀由白色转化为红褐色。
③C+D→白色沉淀,继续加D溶液,白色沉淀逐渐消失。
⑴ 则各是什么物质的化学式为:A 、B 、C 、D 。
⑵现象②中所发生的反应的化学方程式为:
、 。
⑶现象③中所发生反应的离子方程式为:
、 。
五、计算题(本题包括1小题,共8分)
21.向1L AlCl3和FeCl3混合溶液中加入含a mol NaOH的溶液时,产生的沉淀量可达最大值;继续加入NaOH溶液,沉淀开始溶解,当前后加入的NaOH总量达到b mol时,沉淀不再减少,求原溶液中Fe3+的物质的量浓度。
(新课标)第一学期期末考试高一年级化学试卷(A)参考答案
第一部分选择题(48分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 | A | B | B | A | D | C | A | C |
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| 答案 | D | D | D | BC | AD | AC | A | D |
第二部分非选择题(52分)
17.(1) 9g 3.01×1023 9.03×1023 (2) CO2 NH3 CO2
(3) 125 2.5
18..(1)稀氨水+酚酞的混合溶液 加热时氨气逸出,导致溶液的红色变浅;
(2)溶有SO2的品红溶液 加热时SO2气体逸出,品红溶液恢复红色。
19.(1) 2Al + 2NaOH + 2H2O = 2NaAlO2+ 3H2↑
(2) 2FeCl2 + Cl2 =2FeCl3
(3) 2NaHCO3![]() Na2CO3 + CO2↑+ H2O 31.(5分)
Na2CO3 + CO2↑+ H2O 31.(5分)
20.(1) A:BaCl2 B:FeSO4 C:AlCl3 D:NaOH;
(2) FeSO4 + 2NaOH = Fe(OH)2↓+ Na2SO4,
4 Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
(3) Al3+ + 3OH- = Al(OH)3↓,Al(OH)3 + OH- = AlO2- + 2H2O
21.解:因为:Fe3+ +3OH—=Fe(OH)3↓(1分), Al3+ +3OH—=Al(OH)3↓,
Al(OH)3+3OH—=AlO2—+2H2O(1分) 根据物质的量比得:
|
b—a= n(Al3+) ……………………………….
解得:n(Fe3+)]=(4a/3-b)mol/L ……………………………….….
