高二化学下学期选修期末综合试题
(化学反应原理 第三章 实验化学 全) 08.06
一、选择题(本题共20小题,每小题2分,共40分,在每小题给出的四个选项中,只有一项是符合题目要求的。)
1.1体积pH=2.5的盐酸与10体积某一元强碱溶液恰好完全反应,则该碱溶液的pH等于( )
A.9.0
B.9.5
C.10.5
D.11.5
2.下列离子方程式中正确的是( )
A.氢氧化钠溶液吸收过量的二氧化碳OH-+CO2 = HCO3-
B.亚硫酸氢铵溶液与足量氢氧化钠溶液反应 HSO3-+ OH-= SO32-+ H2O
C.氯气通入冷水中Cl2 +H2O = Cl- +ClO- +2H+
D.碳酸镁悬浊液中加醋酸CO32-+2CH3COOH = 2CH3COO-+CO2↑+H2O
3.已知当NH4Cl溶液的浓度小于0.1mol/L时,其pH>5.1。现用0.1mol/L的盐酸滴定10mL0.05mol/L的氨水,用甲基橙作指示剂达到终点时所用盐酸的量应是( )
A.10mL
B.5mL
C.大于5mL
D.小于5mL
4.常温下,0.1 mol/L某一元酸(HA)溶液中 =1×10-8,下列叙述正确的是( )
A.溶液中水电离出的c(H+)=10-10 mol/L
B.溶液中c(H+)+c(A-)=0.1 mol/L
C.溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH-)均增大
D.与0.05mol/L NaOH溶液等体积混合后所得溶液中离子浓度大小关系为c(A-)>c(Na+)>c(OH-)>c(H+)
5.常温下pH=3的二元弱酸H2R溶液与a L pH=11的NaOH溶液混合后,混合液的pH刚好等于7(假设反应前后体积不变),则对反应后混合液的叙述正确的是( )
A.c(R2-)+ c(OH-)=c(Na+)+c(H+)
C.2c(R2-)+ c(HR-)=c(Na+)
B.c(R2-)>c(Na+)>c(H+)=c(OH-)
D.混合后溶液的体积为2a L
6.油墨是有多种色素按一定比例混合而成,某同学欲用纸层析的方法将其主要色素分离开来,可选用做展开剂的物质是( )
A.盐酸
B.酒精
C.NaOH溶液
D.丙酮+盐酸
7.由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是( )
A.②④⑤③①
B.③②④①⑤
C.③④②⑤①
D.②④③⑤①
8.铝分别与足量的稀盐酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的HCl和NaOH物质的量之比为( )
A.1﹕1
B.2﹕1
C.3﹕1
D.1﹕3
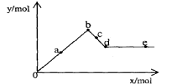 9.已知Ba(AlO2)2可溶于水。右图表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。下列有关叙述正确的是( )
9.已知Ba(AlO2)2可溶于水。右图表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。下列有关叙述正确的是( )
A.a—b时沉淀的物质的量:A1(OH)3比BaSO4多
B.c—d时溶液中离子的物质的量:AlO2-比Ba2+少
C.a—d时沉淀的物质的量:BaSO4可能小于A1(OH)3
D.d—e时溶液中离子的物质的量:Ba2+可能等于OH-
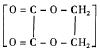 10.以乙醇为原料,用下述6种类型的反应 ① 氧化 ② 消去 ③ 加成 ④ 酯化 ⑤ 水解 ⑥ 加聚,来合成乙二酸乙二酯(结构简式如图所示)的正确顺序是( )
10.以乙醇为原料,用下述6种类型的反应 ① 氧化 ② 消去 ③ 加成 ④ 酯化 ⑤ 水解 ⑥ 加聚,来合成乙二酸乙二酯(结构简式如图所示)的正确顺序是( )
A.①⑤②③④
B.①②③④⑤
C.②③⑤①④
D.②③⑤①⑥
11.对于某些离子的检验及结论一定正确的是( )
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32-
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42-
C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
12.CuS和Cu2S都能溶于硝酸,它们高温灼烧的产物相同,以下鉴别CuS和Cu2S两种黑色粉末的方法合理的是( )
A.将两种样品分别溶于硝酸,区别所产生的气体
B.将两种样品分别溶于硝酸,区别溶液的颜色
C.取两种同质量的样品分别在高温灼烧,区别残留固体的质量
D.取两种同质量的样品分别在高温灼烧,区别残留固体的颜色
13.一定温度下可逆反应:A(s)+2B(g)![]() 2C(g)+D(g);DH<0。现将1
mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
2C(g)+D(g);DH<0。现将1
mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
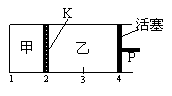

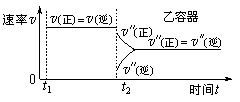
图1 图2 图3
A.保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍
B.保持活塞位置不变,升高温度,达到新的平衡后,甲中B的体积分数增大,乙中B的体积分数减小
C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍
D.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略)
14.钢铁在潮湿的空气中会被腐蚀,发生的原电池反应为:2Fe+2H2O+O2 =2Fe2++4OH-。以下说法正确的是( )
A.负极发生的反应为:Fe-2e- = Fe2+
 B.正极发生的反应为:2H2O+O2+2e-=4OH-
B.正极发生的反应为:2H2O+O2+2e-=4OH-
C.原电池是将电能转变为化学能的装置
D.钢柱在水下部分比在空气与水交界处更容易腐蚀
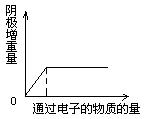
15.用惰性电极电解1L 0.1mol·L-1含Cu2+、X3+的水溶液,阴极增重量与通过电子的物质的量的关系如图所示,则溶液中离子的氧化性有强到弱的顺序是( )
A.Cu2+>X3+>H+
B.X3+ > Cu2+>H+
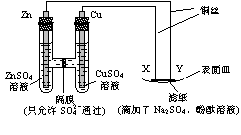 C.Cu2+>H+>X3+
C.Cu2+>H+>X3+
D.H+>Cu2+>X3+
16.如图所示,下列叙述正确的是( )
A.Y为阴极,发生还原反应
B.X为正极,发生氧化反应
C.Y与滤纸接触处有氧气生成
D.X为滤纸接触处变红
17.已知常温常压下饱和CO2溶液的pH值约为3.9,则可以推断盐酸滴定NaHCO3溶液测定其浓度时,适宜选用的指示剂及其终点的颜色变化是( )
A.石蕊,由蓝变红
C.甲基橙,由橙变黄
B.酚酞,红色褪去
D.甲基橙,由黄变橙
18.用惰性电极电解饱和食盐水100mL,经过一段时间后,阴极收集到112 mL氢气(标准状况),此时电解液的pH为(电解液的体积保持不变)( )
A.13
B.12
C.8
D.1
19.今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。
根据上述实验,以下推测正确的是( )
A.K+一定存在
C.Cl-不可能存在
B.100mL溶液中含0.01mol CO32-
D.Ba2+一定不存在,Mg2+可能存在
20.下列分离或提纯物质的方法错误的是( )
A.用渗析的方法精制氢氧化铁胶体
B.用溶解、过滤的方法提纯含有少量硫酸钡的碳酸钡
C.用加热的方法提纯含有少量碳酸氢钠的碳酸钠
D.用盐析的方法分离、提纯蛋白质
二、填空、实验题(本题包括4小题,共48分)
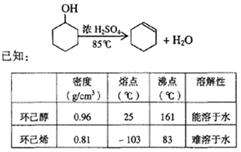
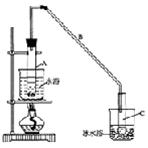
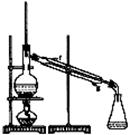
21.(10分)某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是____________,导管B除了导气外还具有的作用是____________。
②试管C置于冰水浴中的目的是____________。
(2)制备精品
 ①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_________层(填上或下),分液后用_________ (填入编号)洗涤。
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_________层(填上或下),分液后用_________ (填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按右图装置蒸馏,冷却水 从_________口进入。蒸馏时要加入生石灰,目的是_____________。
③收集产品时,控制的温度应在_________左右,实验制得的环己烯精品质量低于理论产量,可能的原因是( )
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是_________。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
22.(8分)“碘钟”实验中,3I—+ S2O32- = I3—+SO42-的反应速率可以用I3—与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到数据如下表:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I—)/mol·L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
| c(S2O32-)/mol·L-1 | 0.040 | 0.040 | 0.080 | 0.120 | 0.040 |
| t/s | 88.0 | 44.0 | 22.0 | 44.0 | t1 |
回答下列问题:
(1)该实验的目的是 。
(2)显色时间t1=
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为 (填字母)。
A.<22s B.22—44s C.>44s D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是 。
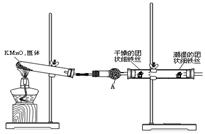 23.(14分)铁生锈是比较常见的现象,某实验小组,为研究铁生锈的条件,设计了以下快速、易行的方法:
23.(14分)铁生锈是比较常见的现象,某实验小组,为研究铁生锈的条件,设计了以下快速、易行的方法:
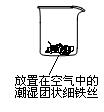
首先检查制氧气装置的气密性,然后按图连接好装置,点燃酒精灯给药品加热,持续3分钟左右,观察到的实验现象为:①直形管中用蒸馏水浸过的光亮铁丝表面颜色变得灰暗,发生锈蚀;②直形管中干燥的铁丝表面依然光亮,没有发生锈蚀;③中潮湿的铁丝依然光亮。
试回答以下问题:
(1)由于与接触的介质不同,金属腐蚀分成不同类型,本实验中铁生锈属于______________。能表示其原理的反应方程式为__________________________________________________。
(2)仪器A的名称为__________,其中装的药品可以是__________,其作用是_________。
(3)由实验可知,该类铁生锈的条件为__________________________________________。
决定铁生锈快慢的一个重要因素是______________________________________________。
24.(16分)实验室用下列方法测定某水样中O2的含量。
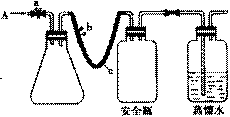 (1)用如右图所示装置,使水中溶解的O2,在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为
(1)用如右图所示装置,使水中溶解的O2,在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为
。
① 打开止水夹a 和b,从A 处向装置内鼓入过量N2,此操作的目的是 。
② 用注射器抽取20.00 mL 某水样从A 处注人锥形瓶。
③ 再分别从A 处注入含m molNaOH的溶液及过量的MnSO4 溶液。
④ 完成上述操作后,下面应进行的操作是 。
c是长橡胶管,使用较长橡胶管的目的是 。
(2)用I— 将生成的MnO(OH)2再还原为Mn2+,反应的离子方程式为:MnO(OH)2+2I—+4H+
==Mn2++I2+3H2O。实验步骤:
⑤ 打开止水夹a、b,分别从A 处注人足量NaI溶液及含n mol H2SO4的硫酸溶液。
⑥ 重复④ 的操作。
(3)用Na2S2O3 标准溶液滴定步骤(2)中生成的I2,反应方程式为:
I2+2Na2S2O3==2NaI+Na2S4O6。
实验步骤:
⑦ 取下锥形瓶,向其中加入2~3滴 作指示剂。
 ⑧ 用0.005 mol · L—1Na2S2O3 滴定至终点。
⑧ 用0.005 mol · L—1Na2S2O3 滴定至终点。
(4)计算。滴定过程中,滴定前后滴定管中的液面读数如右图所示。
⑨ 经计算,此水样中氧(O2)的含量为(单位:mg·L—1) 。
⑩ 本实验中所加NaOH溶液和H2SO4溶液中m和n应有一定量的关系,即应加适量的H2SO4使溶液呈 (填“酸性”、“碱性”或“接近中性”),其原因是 。
三、计算题(本题包括1小题,共12分)
25.氢氧化钡是一种使用广泛的化学试剂。某课外小组通过下列实验测定某试样中Ba(OH)2·nH2O的含量。
(1)称取3.50 g试样溶于蒸馏水配成100 mL溶液,从中取出10.0 mL溶液于锥形瓶中,与0.100 mol / L HCl标准溶液反应,完全反应共消耗标准液20.0 mL(杂质不与酸反应),求试样中氢氧化钡的物质的量。
(2)另取5.25 g试样加热至失去全部结晶水(杂质不分解),称得质量为3.09 g,求Ba(OH)2·nH2O中的n值。
(3)试样中Ba(OH)2·nH2O的质量分数为
2007-2008学年新课标苏教版高中化学选修期末综合试题
参考答案
一.选择题(每小题2分,共40分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | C | A | C | C | C | D | D | C | D | C |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | C | C | D | A | C | A | D | A | A | B |
二.填空、实验题(共48分)
21.(1)(3分)①防暴沸 冷凝 ②防止环己烯挥发
(2)(6分)①上层 c ②g 冷却水与气体形成逆流 ③83oC b
(3)(1分)c
22.(1)(2分)研究反应物I—与S2O32-的浓度对反应速率的影响
(2)(2分)29.3s
(3)(2分)A
(4)(2分)反应速率与反应物起始浓度乘积成正比(或显色时间与反应物起始浓度乘积成反比)
23.(1)(6分)电化学腐蚀 负极:Fe – 2e- = Fe2+,正极:2H2O + O2 + 4e- = 4OH-
(2)(4分)球形干燥管 碱石灰(或无水氯化钙) 干燥O2
(3)(4分)①与O2接触②与水接触 氧气浓度
24.(1)(8分) 2Mn2++O2+4OH—== 2MnO(OH)2
①赶走装置内空气,避免空气中的O2的干扰
④关闭a、b,将锥形瓶中溶液充分振荡;便于实验过程中锥形瓶的振荡
(3)(2分) ⑦淀粉溶液
(4)(6分) ⑨9.4mg·L—1
⑩接近中性;若碱过量,则Mn(OH)2不能全部转变为Mn2+,而酸过量时,滴定过程中Na2S2O3可与酸反应。
三.计算题(12分)
25.(1)0.01 mol(4分)
(2)n=8(4分)
(3)90%(4分)