高二化学会考复习试卷16
(模拟试卷)
(考试时间:90分钟 满分:100分)
命题老师:政和一中 陈童芬
高二 班 姓名 座号 成绩
[相对原子质量:H-1、D-2、C-12 、O-16、Na-23 、Cl-35.5 、 K-39 ]
第I卷 (选择题 46分)
一、选择题:(本题共23小题,每小题2分,共46分,每小题只有一个正确答案)
1. 2000年10月香港特首董建华提出他的第三份施政报告,着重提出要改善香港的环境状况。香港和我国其他许多城市一样,空气质量不佳。其主要原因是机动车尾气排放,为治理污染你认为下列汽油替代品中污染最小的是-------------( )
A. 天然气 B. 酒精 C. 液氢 D. 煤气
2.下列物质中,既含有离子键又含有共价键的是--------------------------( )
A.H2O B.CaCl2 C..Na2 O2 D.C12
3. 以NA表示阿佛加德罗常数,下列说法中正确的是----------------------( )
A. 53g碳酸钠中含NA个CO32—
B. 0.1molOH-含NA个电子
C. 1.8g重水(D2O)中含NA个中子
D. 标准状况下11.2L臭氧中含NA个氧原子
4.在医院中,为酸中毒病人输液不应采用--------------------------------------------( )
A. 0.9%氯化钠溶液 B. 0.9%氯化铵溶液
C. 1.25%碳酸氢钠溶液 D . 5%葡萄糖溶液
5.下列电子式中错误的是
A . Na+ B . ![]() C .
C . ![]() D.
D. ![]()
6、生活中的一些问题常涉及化学知识,下列叙述正确的------------------( )
A. 蚕丝,棉花和人造羊毛的主要成分都是纤维素
B. 纯净的碳酸钡可作为医用“钡餐”
C. 酒厂可用工业酒精(含CH3OH),勾兑白酒
D. 福尔马林是一种良好的杀菌剂,但是不能用来消毒饮
7. 下列互为同位素的是----------------------------------------------( )
A.金刚石和石墨 B.![]() C.乙烷和丙烷 D.T2O和D2O
C.乙烷和丙烷 D.T2O和D2O
8. 在全国上下抗“非典”战斗中,广泛使用过氧乙酸作消毒、杀菌剂。过氧乙酸的
![]()
结构简式为它具有较强的腐蚀性,易挥发,易分解为乙酸和氧气。
下列说法正确的是---------------------------------------------------------( )
A、可直接用过氧乙酸对手,脸等外部位进行消毒
B、喷洒过过氧乙酸的房间,通风后对人体不会产生毒害
C、过氧乙酸含有羧基(─COOH),可发生酯化反应
D、过氧乙酸与乙酸(CH3COOH)互为同分异构体
9. 常温下,将铁片放入下列溶液中,能明显观察到有气体产生的是---------( )
A.浓硫酸 B.稀硫酸 C. ZnSO4溶液 D.CuSO4
10. 在Na2O2与水的反应中,下列叙述正确的是--------------------------( )
A. Na2O2既是氧化剂又是还原剂 B. 水是还原剂
C. 水既是氧化剂又是还原剂 D. 水是氧化剂
11.下列离子方程式书写正确的是--------------------------------------( )
A.醋酸加入氢氧化钠溶液中:H++OH—=H2O
B.铁跟氯化铁溶液起反应;Fe + 2 Fe3+=3 Fe2+
C.氢氧化钡溶液滴入硫酸中:Ba2++SO42—=BaSO4↓
D.碳酸钙与盐酸反应:CO32—+2 H+=H2O+CO2↑
12. 若将乙醛通过下列两步反应转变成溴乙烷:
![]()
这两步反应分别属于有机反应类型中的------------------------------( )
A.加聚反应和水解反应 B.消去反应和加成反应
C.加成反应的取代反应 D.加成反应的消去反应
13. 下列物质中,其分子式为C6H14的可能是----------------------------( )
A.2-甲基丁烷 B.2,3-二甲基戊烷 C.2-甲基己烷 D.2,3-二甲基
14.下列分离或提纯物质所用的方法不正确的是-------------------------( )
A.用加热的方法除去Na2CO3中混有的NaHCO3
B.用分液的方法分离乙醛和水的混合物
C.用萃取的方法提取碘水中的碘
D.用结晶的方法分离氯化钠和硝酸钾的混合物
15. 下列物质露置在空气中,不会发生化学变化的是---------------------( )
A.白磷 B.氢硫酸 C. 烧碱溶液 D. 硝酸钠溶液
16.在强酸溶液中,下列各组离子能够大量共存的是---------------------( )
A. Mg2+、Ca2+、HCO3—、Cl—
B. Na+、AIO2—、CI—、SO42—
C. K+、Fe2+、SO42—、Br—
D. Fe2+、Ca2+、CI—、NO3—
17.进行如下实验时,所选用的试剂错误的是---------------------------( )
A.用稀盐酸清洗做焰色反应的铂丝 B.用浓硫酸吸收二氧化硫中水蒸气
C.用稀硝酸洗去残留在试管壁上的银镜 D.用稀盐酸和二氧化锰制取氯气
18. 能用实验室制取氧气的气体发生的装置来制取的气体是---------------( )
A.Cl2 B.CH4 C.H2 D.HCl
19.
在一定条件下,发生反应:2NO2 ![]() N2O4,该反应达到化学平衡后,降低温度,
N2O4,该反应达到化学平衡后,降低温度,
混合物的颜色变浅,下列有关说法正确的是
A.正反应为放热反应 B.正反应为吸热反应
C.降温后NO2的浓度增大 D.降温后各物质的浓度不变
20. 误食重金属盐会使人中毒,可以解毒急救的措施是-------------------( )
A.服大量的开水 B.喝大量的牛奶或服鸡蛋清
C.服葡萄糖水 D.喝大量白开水
21.下列变化中,不属于化学变化的是----------------------------------( )
A.SO2使品红溶液褪色 B.氯水使有色布条褪色
C.活性炭使红墨水褪色 D.O3使某些染料褪色
22. 等体积的盐酸和氢氧化钠溶液分别与两份足量铝粉反应,在相同条件下产生 相同体积的氢气。则盐酸和氢氧化钠溶液物质的量浓度之比为
A. 1:1 B. 2:1 C. 3:1 D. 2:3
23. A、B、C都是金属,A中混有C时,A先腐蚀;A与B组成原电池时,A为电池的正极。A、B、C三种金属的活动性顺序为
A. A>B>C B. A>C>B C. B>C>A D. B>A>C
第Ⅱ卷 (非选择题 56分)
二.填空题:(本题共7小题,,共34分)
![]()
![]() CH3
CH3
24. (6分) 橡胶是异戊二烯CH2==C—CH=CH2经聚合反应后生成的聚合物,该聚
![]() CH3
CH3![]()
合物-[-CH2—C==CH—CH2-]-n的名称是____________________。明矾[KAl(SO4)2·12H2O]溶于水,生成的胶状氢氧化铝可以吸附水里悬浮的杂质形成沉淀,所以曰常生活中,明矾常用于_______________________。焊接钢轨时所用的铝热剂是__________与氧化铁的混合物。
25. (7分)右图所示为A、B、C三种元素在周期表中的相对位置,已知A、B、C均为短周期元素,且三种元素的原子序数之和为31,最外层电子数之和为17。
![]()
![]() (1)三种元素符号分别是A ;B ;C 。
A B
(1)三种元素符号分别是A ;B ;C 。
A B
![]() (2)A的最高价氧化物对应水化物的分子式是
。 C
(2)A的最高价氧化物对应水化物的分子式是
。 C
(3)B的氢化物的电子式是 。
(4)C的阴离子结构示意图为 。
(5)C的最高价氧化物对应水化物的酸性比高氯酸 (填写“强”或“弱” )。
26.(4分)写出下列反应的化学方程式(并注明反应的条件)。
(1)过氧化钠与二氧化碳反应:
。 。
(2)乙酸与乙醇在浓硫酸存在下共热,发生酯化反反应:
。
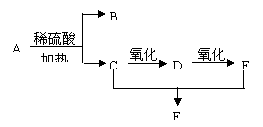 27. 化合物A的分子式为C3H6O2有下列转化关系:
27. 化合物A的分子式为C3H6O2有下列转化关系:
D、E、F都能发生银镜反应。(3分)
(1)A的名称是
(2)B的结构简式是 。
(3)D中含有的官能团是 。
28.(5分)有一包白色固体粉末可能含有CaCO3、Na2CO3 、(NH4)2SO4、NaNO3、CuSO4的中一种或几种。现将固体粉末进行下列实验,产生的现象为:
(1)溶于水得无色澄清溶液; (2)取溶液少许作焰色反应呈黄色;
(3)另取溶液加入足量的氯化钡溶液,得到白色沉淀,向沉淀中加入足量的盐酸,全部溶解。则该白色固体粉末中一定含有 ;一定不含有 ;可能含有 。
29.(3分)丙烯醛的结构简式为:![]() 。现提供下列几种试剂,试推测丙烯醛可能具有的化学性质。请按要求填写下列空格。
。现提供下列几种试剂,试推测丙烯醛可能具有的化学性质。请按要求填写下列空格。
A.溴水 B.新制的Cu(OH) 2 C.Na2CO3溶液 D.KMnO4酸性溶液 E.银氨溶液
(1)在一定条件下丙烯醛能与上述几种试剂中 发生反应(填序号)。
(2)该有机物与足量的氢气在一定条件下完全反应后生成(写名称) 。
30.(6分)简要回答下列问题。
(1)为什么未成熟的水果吃起来不甜,而熟透的水果吃起来才甜?
。
(2)废旧电池集中回收的目的是:
。
(3)四氯化碳可做提取碘水中的碘的萃取剂的理由是:
。
三、实验题:(本题共2小题,共12分)
31.为了证实下列实验 (Ⅰ)项中的结论.请从(Ⅱ)项中选出相应的实验方法、 并(Ⅲ)项中选出所观察到的相应的实验现象,将每题正确答案的标号填写在答案栏Ⅱ、Ⅲ空格里.(6分)
| 答案 | |||||
| (Ⅰ)实验结论 | (Ⅱ)实验方法 | (Ⅲ)实验现象 | Ⅰ | Ⅱ | Ⅲ |
| 1.汽油里含有少量水 | (A)加BaCl2溶液 (B)加水 | a.变蓝 b.黄色 |
1 | ||
| 2.芒硝的成分是硫酸钠 | (C)加稀盐酸 (D)加无水硫酸铜 | C.有白色沉淀生成 d.溶解 |
2 | ||
| 3.长期存放的过氧化钠会变质 | (E)加AgNO3溶液 (F)做焰色反应实验 | e. 沉淀不消失 f.生成使石灰水变浑浊的气体 | 3 | ||
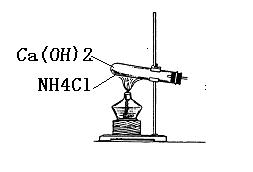 32.(6分) 实验室通常用如右图所示的装置来制
取氨气。回答下列问题:
32.(6分) 实验室通常用如右图所示的装置来制
取氨气。回答下列问题:
(1) 安装仪器时要求试管口略低于试管底的原
因是: 。
。
(2)制取氨气时的化学反应方程式为:
。
(3)收集氨气时必须使用干燥的集气装置的原因是 。
。
(4)加热后将蘸有浓盐酸的玻璃棒靠近导管口,产生的现象是:
。
(5)除氨气外,还可以用该装置制取的常见气体有:
。
四、计算题:(本题共2小题,共8分)
33.(2分) 44.8升(标准状态)的氯化氢气体溶于1060 g水中,所得盐酸(密度为1.03 g/cm3)的物质的量浓度是多少?
34.(6分)实验室可用氯酸钾与浓盐酸反应制取氯气,该反应的化学方程式为:
KClO3+6HCl===KCl+3H2O+3Cl2↑
现将24.5 g KClO3跟150 mL12 mol/L盐酸充分反应,求:
(1)生成的Cl2在标准状态下体积为多少升?
(2)将反应后混合液稀释至500 mL,此时溶液中Cl— 的物质的量浓度为多少?
(KClO3摩尔质量为122.5 g/mol)
高中化学会考复习试卷答案
一、选择题:1 C 2.C 3 B 4 .B 5.C 6.D 7.B 8.B 9.B 10.A .11. B 12.C 13.D 14.B
15.D 16. C 17.D 18.C 19.A.20.B 21. C 22.C.23.D
![]() 二、填空题:24.聚异戊二烯 净水剂 铝
二、填空题:24.聚异戊二烯 净水剂 铝
25.(1)A:N B:O C:S (2)HNO3 (3)
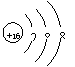
(4)(5)弱
| |
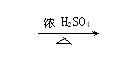
(2) CH3COOH + HO-CH2CH3 CH3COOCH2CH3 + H2O
27. (1)乙酸甲酯 (2)CH3COOH(3)醛基
28.Na2CO3 ; CaCO3、CuSO4、(NH4)2SO4; NaNO3。
29.(1) A.B.D.E;(2)丙醇。
30.(1)因未成熟的水果中含淀粉所以不甜;成熟的水果中含葡萄糖(淀粉在酶的作用下水解变成了葡萄糖)所以吃起来会甜。
(2)因废旧电池中含有镉、铅、锌、锰等重金属会污染环境,所以要集中回收处理。
(3)四氯化碳比水重与水互不相溶,且碘在四氯化碳中的溶解度比在水中大。
31.1.D;a 2.A.F;c.b 3.C;f
32.(1)答:防止加热时产生的水蒸气冷凝流到试管底部而造成试管破裂。
(2)Ca(OH)2 +
2NH4Cl![]() CaCl2
+2NH3↑ +2H2O
CaCl2
+2NH3↑ +2H2O
(3)氨极易溶于水。
(4)有白烟产生。
(5)CH4、O2 .
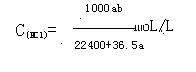
33 .
34.(1)V(cl2)=13.44L
(2)C(Cl_)=1.6mol/L
