高二化学第一次质量检测
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。共150分。考试用时120分钟。
第Ⅰ卷(选择题,共72分)
可能用到的相对原子质量:H—1 C—12 N—14 O—l 6 Na—23 Mg—24 Al—27
S—32 Cl—35.5 Ca—40 Fe—56 Zn—65 Ba—137
一、选择题(本题包括8小题,每小题4分,共32分。每小题只有一个选项符合题意。)
1、在2L密闭容器中,盛有2mol X和2molY物质进行如下反应:
X(s)+3Y(g) Z(g),当反应进行到10s后,测得生成0.5mol Z,这期间的平均反应速率为
A、vX=0.05mol·s-1 B、vX=0.025mol·L-1·s-1
C、vy=0.05mol·L-1·s-1 D、vy=0.075mol·L-1·s-1
2、对于反应A2+3B2 2AB3以下表示的反应速率中,速率最大的是
A、vA2=0.4mol·L-1min-1 B、vB2=0.8mol·L-1min-1
C、v![]() =0.6mol·L-1min-1
D、v
=0.6mol·L-1min-1
D、v![]() =0.01mol·L-1·S-1
=0.01mol·L-1·S-1
3、现有三个体积相等的密闭容器中都进行如下反应:
CO2+H2 CO+H2O(g),反应所处的温度相同,但反应的起始浓度不同,其中
甲: [H2]=[CO2]=amol 乙:[CO2]=amol [H2]=2amol 丙[CO2]=[H2]=[H2O]=amol,达到平衡时,CO的浓度由大到小的顺序排列正确的是
A、丙>甲>乙 B、甲>乙>丙 C、乙>丙>甲 D、乙>甲>丙
4、在一个固定体积的密闭容器中,放入mmol的A和nmol的B,发生如下反应:
mA(g)+nB(g) pC(g),平衡时C的浓度是wmol·L-1,若维持容器的体积不变,起始时放入amolA、bmolB和cmolC,要使平衡时C的浓度仍为wmol·L-1,则a、b、c必须满足的条件是
A、a:b:c=m:n:p
B、a:b=m:n和![]()
C、![]() 和
和![]() D、a=
D、a=![]() , c=
, c=![]() 和c=
和c=![]()
5、对处于化学平衡的体系,以化学平衡与化学反应速率的关系可知:
A、化学反应速率变化时,化学平衡一定发生移动。
B、化学平衡发生移动时、化学反应速率一定变化。
C、正反应进行的程度大、正反应速率一定大。
D、只有催化剂存在下,才会发生化学反应速率变化,而化学平衡不移动的情况。
6、在PCl5(g) PCl3(g)+Cl2(g),达到平衡后,其它条件不变,向平衡体系中加入37Cl2,达到新平衡后,含37Cl的PCl3的物质的量与原平衡相比
A、增大 B、减小 C、不变 D、不能确定
7.某温度下,浓度都是1mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z,达到平衡后c(X2)为0.4mol/L,c(Y2)为0.8mol/L,生成Z为0.4mol/L,则该反应的化学方程式为
A.X2+2Y2![]() 2XY2
2XY2
B.2X2+Y2![]() 2X2Y
2X2Y
C.3X2+Y2![]() 2X3Y
2X3Y
D.X2+3Y2![]() 2XY3
2XY3
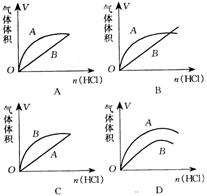
8.进行如下实验,在A锥形瓶中放入10g块状CaCO3,在B锥形瓶中放入5g粉末状CaCO3,分别加入50mL2mol/L盐酸。右图中能正确表示实验结果的是( )
二、选择题(本题包括10小题,每小题4分,共40分,每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给4分,但只要选错一个,该小题就为0分)
9、下列事实不能用勒沙特列原理说明的是
A.由H2、I2(g)、HI组成的平衡体系,加压后颜色加深
B.氨水应密闭保存,放置低温处
C.500℃左右比室温更有利于合成氨的反应
D.实验室常用排饱和食盐水的方法收集氯气
10.已知:4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),若反应速率分别用
4NO(g)+6H2O(g),若反应速率分别用![]() (NH3)、
(NH3)、![]() (O2)、
(O2)、![]() (NO)、
(NO)、![]() (H2O)[mol/(L·min)]表示则下列关系正确的是
(H2O)[mol/(L·min)]表示则下列关系正确的是
A.![]() B.
B.![]()
C.![]() D.
D.![]()
11.在一定温度下,容器中加入CO和H2O(g)各1mol,发生反应:
CO+H2O![]() CO2+H2,达到平衡时生成0.7mol的CO2,若其他条件不变,一开始就加入4mol H2O(g),则达到平衡可能生成的CO2是
CO2+H2,达到平衡时生成0.7mol的CO2,若其他条件不变,一开始就加入4mol H2O(g),则达到平衡可能生成的CO2是
A.0.6mol B.0.95mol C.1mol D.1.5mol
12.反应mA(固)+nB(气) ![]() eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是( )
eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是( )
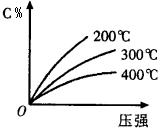
B 到平衡后,加入催化剂则C%增大
B.达到平衡后,若升温,平衡左移
C.化学方程式中n>e+f
D.达到平衡后,增加A的量有利于平衡向右移动
13.把3mol A和2.5mol B混合于2L密闭容器中,发生反应:
3A(g)+B(g)
![]() xC(g)+2D(g)
xC(g)+2D(g)
5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.1mol/(L·min),下列结论错误的是
A.A的平均反应速率为0.1mol/(L·min)
B.平衡时,C的浓度为0.125mol/L
C.平衡时,B的转化率为20%
D.平衡时,容器内压强为原来的0.8倍
14.在一定温度下的固定容积的密闭容器中,当下列物理量不再变化时,表明反应:
A(s)+2B(g)
![]() C(g)+D(g)已达平衡的是
C(g)+D(g)已达平衡的是
A.混合气体的压强 B.混合气体的密度
C.B的物质的量浓度 D.气体的总物质的量
15.在一密闭容器中,aA(g)![]() bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则
bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则
A.平衡向正反应方向移动了
B.物质A的转化率减小了
C.物质B的质量分数增大了
D.a>b
16、在CuCl2水溶液中存在如下平衡:[Cu(H2O)4]2++4Cl- [CuCl4]2-+4H2O不能使黄
(蓝) (绿)
绿色CuCl2溶液向蓝色转化的操作是
A、蒸发浓缩 B、加水稀释 C、加入AgNO3 D、加入食盐晶体
17、反应A(g)+xB(g) yC(g),将A与B按体积比1:x混合反应当A的转化率是50%时,反应前混合气体的密度是反应后混合气体密度的![]() (同温同压),则x、y的值不可能是
(同温同压),则x、y的值不可能是
A、3,4 B、3,2 C、3,3 D、1,1
18.在恒温、恒容的密闭容器中进行反应A(g)==B(g)+C(g),若反应物的浓度由2 mol·L-1降到0.8 m01·L一1需要20s,那么反应物浓度再由0.8 mol·L-1降到0.2 mol·L-1所需要的时间为
(A)lOs (B)大于10s (C)小于10s (D)无法判断
第二部分非选择题 (共78分)
三、(本题包括2小题,共20分)
19.现在一定条件下进行下列可逆反应的实验A(g)+2B(g ) 3C (g); △H <0。平行三组实验的有关条件如表
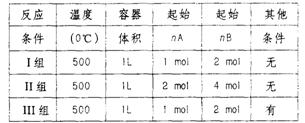
已知I组实验过程中,C气体的体积分数Vc%随时间t的变化曲线如图:
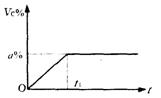
(1)试在右图中画出II组实验过程中C气体体积分数随时间t的变化曲线。
(2)若III组实验过程中.C气体体积分数随时间t的变化曲线与II组相当,则它所具备的“其它条件”可能是
(3)在I组实验中B气体的转化率是 ,若将实验温度变为8000C,则达到平衡所需时间 t1,(小于、大于、等于),平衡时VC% a%(小于、大于、等于)
20. 在一恒容密闭容器中发生某化学反应2A(气) B(气)+C(气)在三种不同条件下进行,其中实验I. II在8000C,实验111在8500C , B, C的起始浓度都为0,反应物A的浓度(mol . L-1)随时间(min)变化如下图,请回答:
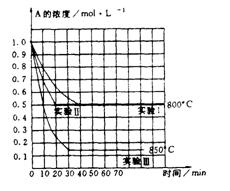
(I)在实验I中,反应在20min至30min内A的平均反应速率为 mol - L-'·min- 1
(2)实验II和实验I比较,可能隐含的反应条件是
(3)根据实验III和实验I比较,可推测该反应升高温度,平衡向 (“正’‘或“逆”)反应移动,该正反应是_ (‘放热”或“吸热”)反应。
(4)与实验I比较若将实验I中A的起始浓度改为1. 2rnol - L-',其他条件不变,则达到平衡时,所用时间_ 实验I(用“>”“=”“<”“无法确定”填写。![]()
四、(本题包括2小题,共22分)
21.(1)发生反应:2SO2+O2![]() 2SO3,当此反应进行到一定程度时,就达到了化学平衡状态。若该容器中维持温度不变,令a、b、c分别代表起始的SO2、O2和SO3的物质的量,如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保持达到平衡时,反应混合物中三种气体的体积分数仍跟上述平衡时完全相同。试填写下列空白:
2SO3,当此反应进行到一定程度时,就达到了化学平衡状态。若该容器中维持温度不变,令a、b、c分别代表起始的SO2、O2和SO3的物质的量,如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保持达到平衡时,反应混合物中三种气体的体积分数仍跟上述平衡时完全相同。试填写下列空白:
(A)若a=0,b=0,则c=______;
(B)若a=0.5mol,则b=________,c=_________;
(C)a、b、c取值必须满足的一般条件是(请用两个不同的式子表示)____________
_______________________________________。
21(2).如图所示为一恒压容器。在恒定温度下,将1molN2和3molH2混合后由A口快
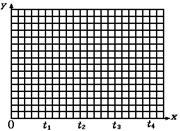
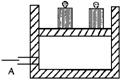
速充入容器,封闭A,反应N2+3H2![]() 2NH3在t1时刻达到平衡,t2时刻再从A口快速充入一定量NH3,封闭A,t3重新达平衡至t4。请在图中画出0→t4时间内混合气中NH3的体积分数(y坐标)随时间(x坐标)变化的曲线。
2NH3在t1时刻达到平衡,t2时刻再从A口快速充入一定量NH3,封闭A,t3重新达平衡至t4。请在图中画出0→t4时间内混合气中NH3的体积分数(y坐标)随时间(x坐标)变化的曲线。
22.在一定条件下,x A+y B![]() z C的反应达到平衡。
z C的反应达到平衡。
(1)已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z之间的关系是__________________;
(2)已知C是气体,且x+y=z,在增大压强时,如果平衡发生移动,则平衡一定向_____________移动;
(3)已知B、C是气体,当其他条件不变,增大A的物质的量时,平衡不发生移动,则A是_____________态物质。
(4)若加热后C的质量分数减少,则正反应是_________(填“放热”或“吸热” )反应。
(5)若A、B、C均为气体,反应在恒温恒压下进行。A、B、C的起始浓度分别为:a mol·L-1、bmol·L-1和cmol·L-1,无论反应是从正反应还是逆反应开始,若要建立相同的平衡状态,a、b、c应满足的条件是 。
五、(本题包括2小题,共16分)
23.在一个盛有催化剂、容积可变的密闭容器中,保持一定温度和压强,进行以下反应:N2+3H2![]() 2NH3。已知加入1mol N2和4 molH2时,达到平衡后生成a mol NH3(见下表“已知”项)。在相同温度、压强下,保持平衡时各组分的体积分数不变。对下列编号①~③的状态,填写表中的空白。
2NH3。已知加入1mol N2和4 molH2时,达到平衡后生成a mol NH3(见下表“已知”项)。在相同温度、压强下,保持平衡时各组分的体积分数不变。对下列编号①~③的状态,填写表中的空白。
| 已知 编号 | 起始状态物质的量n/mol | 平衡时NH3的物质的量n/mol | ||
| N2 | H2 | NH3 | ||
| 1 | 4 | 0 | a | |
| ① | 1.5 | 6 | 0 | |
| ② | 1 | 0.5a | ||
| ③ | m | g(g≥4m) | ||
24(1).在四个同样密闭容器中发生反应:A(g)+3B(g) ![]() 2C(g),在同一时间内测得容器内的反应速率:甲为:
2C(g),在同一时间内测得容器内的反应速率:甲为:![]() (A)=3
mol/(L·min);乙为
(A)=3
mol/(L·min);乙为![]() (B)=4.5
mol/(L·min);丙为
(B)=4.5
mol/(L·min);丙为![]() (C)=4
mol/(L·min);丁为
(C)=4
mol/(L·min);丁为![]() (A)=0.75mol/(L·s)。若其它条件相同,温度不同,则温度由低到高的顺序是___________________。
(A)=0.75mol/(L·s)。若其它条件相同,温度不同,则温度由低到高的顺序是___________________。
24(2)、在一个容积不变的反应容器中,要求通过调节体系的温度使下列反应
A(g)+2B(g) 2C(g)达到平衡时保持容器内气体总物质的量为12mol,。现向反应器中加入6.5molA,X molB,2.0 molC.
(A)若x=5.5时,需要降低体系温度使反应在平衡时达到题设条件,则正反应为_____热反应。
(B)欲使起始反应维持向逆方向移动,则x取值范围是__________
高二化学第一次质量检测
化学答题卡
一.二 选择题
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | | |
| | | | | | | | | | |
| 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| | | | | | | | | | |
三 (本题包括2小题,共20分)
19 (1) (2)它所具备的“其它条件”可能是
(2)它所具备的“其它条件”可能是
(3)B气体的转化率是 到平衡所需时间 t1, 平衡时VC% a%
20
(1)平均反应速率为 mol - L-'·min- 1 (2)隐含的反应条件是
(3) 平衡向 反应移动 正反应是_ 反应
(4)所用时间_ 实验I
四、(本题包括2小题,共22分)
21(1)(A)若a=0,b=0,则c=______;
(B)若a=0.5mol,则b=________,c=_________;
(C)a、b、c取值必须满足的一般条件是(请用两个不同的式子表示)
_______________________________________ 。

21(2)
22(1) x、y、z之间的关系是__________________; (2)平衡一定向_____________移动;
(3)A是_____________态物质。 (4) 正反应是_________反应
(5) a、b、c应满足的条件是 。
五、(本题包括2小题,共16分)
23
| 已知 编号 | 起始状态物质的量n/mol | 平衡时NH3的物质的量n/mol | ||
| N2 | H2 | NH3 | ||
| 1 | 4 | 0 | a | |
| ① | 1.5 | 6 | 0 | |
| ② | 1 | 0.5a | ||
| ③ | m | g(g≥4m) | ||
24(1)温度由低到高的顺序是___________________。
24(2) (A)正反应为_____热反应。(B) x取值范围是__________
