2006�߶���ѧ�ڶ�ѧ����ĩ��������
��ʱ�䣺90���ӡ� ��ֵ��120�֣�
��ע������ ���Ծ���Ϊ��I����ѡ����1��2ҳ���͵ڢ������ѡ����3��8����
�� ����ʱ���ѵ�I����ѡ���⣩�Ĵ�д�ڵ�2ҳѡ����������ڣ��ڢ������ѡ���⣩�Ĵ�ֱ��д��������йؿհ״���
�� �����õ������ݣ�ԭ�ӵ����������H: 1��C: 12��O: 16��
��I�� ��ѡ��������45�֣�
һ��ѡ���⣺������15С�⣬ÿС��3�֣���45�֡������и�����ĸ�ѡ���У�ֻ��һ��ѡ���Ƿ�����ĿҪ��ġ�
1�����и��������л������ࡢ��Ŀ����û�й�ϵ���ǡ�����
A. ÿ��̼ԭ������������ԭ�ӣ���̼ԭ�ӣ��γ��������ۼ�
B. �����ԭ�������ȫ��ͬ�ķ��Ӿ��в�ͬ�Ľṹ
C. ̼ԭ�Ӽ�����γɵ�����˫��������
D. ̼���������ȶ�
2�����й��ڼ������������ȷ���ǡ���������������
A. ������ӵĽṹ��ƽ�������Ρ��������������� B. һ�ȼ���������ͬ���칹��
C. ���������û�в����ͼ���������ܱ��������� D. �����������
3�����������䡱�ǿ�����������һ���ش̡�����ġ���������ָ����
A. ú���������� B. ��ȼ����������C. Һ���������� D. ��ϩ��
4����Һ��������Һ��ʯ�����ĵļ�ƣ�ͨ���ø�ƿʢװ�����ھ��������û��ڳ�����ͨ����ѹʹ�����ΪҺ��������ƿ���棻ʹ��ʱ���ţ�����ѹǿ��С��Һ�����ʻӷ������幩ȼ�ա����ࡰ����������ʹ�á�Һ��������ȼ�ϡ���Һ����������Ҫ�ɷ���
A. ���顡������ B. ���顡������ C. ����Ͷ��顡����D. �Ҵ�
5�������ŵ����Ѿ���ʼʹ�á�������ȡ��ˮú������Ҫ�ɷ�H2��CO����Ϊ�����������������ͨ����������¯��ʹȼ�ա���������ȼ��ˮú���ﵽͬ����Ч�������ڿ����Ľ����ڲ����ǰ���£�����Ҫ�ѡ�ȼ�������Ľ�����
A. ��С�������� B. �������� C. ά�ֲ��䡡������ D. ����ȷ��������
6�����и������ʵĽṹ��ʽ��ȷ����
A. ���� CH3CH3 B. ��ϩCH2CH2�� C. �Ҵ�C2H6O�� D. ��ȩ CHOH����
7�����л�ѧʽֻ�ܱ�ʾһ�����ʵ���
���� A. C2H6O�������� B. C3H6O����������C. C2H6Br������ D. C3H6NO2��������
8����ҵ�ƾ��к����ж����ʣ��Ͻ��ù�ҵ�ƾ�����ʳ�þơ�����������̷�����Ѭ�ģ��ù�ҵ�ƾ��Ƴ�ɢװ�ƣ�ʹ�����������ж���˫Ŀʧ��������������ҵ�ƾ��е��ж��ɷ���
���� A. �״����������� B. �Ҵ���������C. ���ᡡ������ D. ��������
9������ʯ�ͺ�ú�����ƺͼӹ������У������ڻ�ѧ�仯����
A. ���������� B. ��������C. �ѻ��������� D. �ѽ�
10�����л������У����ܷ�����ȥ��Ӧ�����ܷ���ˮ�ⷴӦ����
A. ���ᡡ�� B. �Ҵ����� C. �����顡�� D. ��������
11��������ʵ���У�Ӧ���¶ȼƲ���ˮԡ�е���
A. ��ʵ����������ʯ�͡������������� B. �ɱ�����������������
C. �ɾƾ�����ϩ�������������������� D. ���������Ҵ���Ӧ����������
12�����������У����������𱽷�ˮ��Һ���Ҵ�����������������Һ����������Һ��һ���Լ���
A. ��ˮ���� B. ���Ƶ�������ͭ�� C. ������Һ����D. ������
13��ȼ��0.2 molij�л���õ�0.4mol CO2��0.6molH2O���ɴ˿ɵó��Ľ�����
A. ���л��ﺬ��2��̼ԭ�Ӻ�6����ԭ��
B. ���л�����̼Ԫ�غ���Ԫ�ص�ԭ�Ӹ�����Ϊ1��3
C. ��������2��CO2��3��H2O
D. ���л����һ�������ﺬ��2��̼ԭ�Ӻ�6����ԭ�ӣ������ܺ�����ԭ��
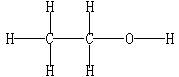
14�������ͼ��ʾ�Ҵ����ӽṹ�����������Ҵ��ڸ��ֻ�ѧ��Ӧ�л�ѧ�����������˵������ȷ���ǡ�����������������������
���� A. ����ᡢŨ���Ṳ��ʱ���ڼ�����
B. ������Ʒ�Ӧʱ���ټ�����
|
|
|
|
D. ��Ag������O2 ��Ӧʱ���� ���� �����ѡ�
![]()
![]() OH
OH
15����«��HO����������CH=CH���������� �㷺������ʳ����绨�������������ѣ��У�
�������������������������������������� OH
�����ܾ��п����ԡ��ܹ���1 mol �û�������Ӧ��Br2��H2 ����������ֱ���
A. 1 mol ��1 mol���� B. 3.5 mol ��7 mol���� C. 3.5 mol ��6 mol����D. 6 mol ��7 mol
��II������ѡ��������75�֣�
ע�����1. ��II����6ҳ, �øֱʻ�Բ���ֱ�Ӵ����Ծ��ϡ�
�������� 2. ���ǰ���ܷ����ڵ���Ŀд���
| �÷� | ������ |
�������������6С�⣬��29��
16(5��). ϩ����ͨʽ��_____________________����д����ϩ�Ľṹʽ_____________________����Ȳ�ĵ���ʽ_________________�����ж���ϩ������(��Ի�Ǽ���)___________���ӣ�������Ϊ________________________________________________________
17(3��). ���CH3��CH2��CH2��CH��CH3 ��������
![]()
![]()
![]()
![]()
![]() ��������CH3
CH2��CH2��������������
______________________________________
��������CH3
CH2��CH2��������������
______________________________________
���� CH3��CH3
18(10��). ���и�������֮����ͬϵ�����_____________����ͬ���칹�����________________
A.�� CH3CH2COOH��CH3COOCH3�������� B. NH2CH2CH2COOH��CH3CH2CH2NO2
C.�� CH2=CHCH3��CH2 =CH��CH=CH2���� D. CH2 =CH��CH=CH2 ��CH3CH2C��CH
![]()
![]()
![]() E.�� ������2�� �����顡�� F. ��������ά�ء� G. ��ϩ�뻷����
E.�� ������2�� �����顡�� F. ��������ά�ء� G. ��ϩ�뻷����
![]() H.����������
�롡��������������
I.������������
��
H.����������
�롡��������������
I.������������
��
19(3��). �ں���ͭ�����ʱ�����Ȱ���ͷ���ڻ�����һ�ᣬ�Գ�ȥ���ı����ᣬ�������ھƾ���պһ�º��ٺ��ӡ�������еĵ����û�ѧ����ʽ��ʾ�ǣ�
_________________________________________________________________________________
20(4��). ��ȡ���������������ַ������� ��������������ȡ����Ӧ �� ��ϩ���Ȼ��ⷢ���ӳɷ�Ӧ�� ��������������ַ������ò�˵��ԭ��
________________________________________________________________________________
________________________________________________________________________________
![]() 21(4��). ��һ�־��������Եĺϳ��Ľṹ��ʽ�ɱ�ʾΪ��CH2CH=CHCH2CH2CH�� �������ָ�
21(4��). ��һ�־��������Եĺϳ��Ľṹ��ʽ�ɱ�ʾΪ��CH2CH=CHCH2CH2CH�� �������ָ�
�������������������������������������������������������������� CN
���ӻ�����ĵĵ���Ľṹ��ʽ��____________________________________________________
| �÷� | ������ |
�����������1С�⣬��8�֡�
22(8��). 1,2����������������Ϳ�������������������ɫҺ�壬�ܶ�2.18g/cm3 ���е�131.4 �� ���۵�9.79 �� ��������ˮ �������ڴ����ѡ���ͪ���л��ܼ�����ʵ�����п�������ͼװ���Ʊ�1,2���������顣���з�Һ©������ƿa��װ���Ҵ���Ũ����Ļ��Һ���Թ�d��װ��Һ�壨���渲������ˮ����
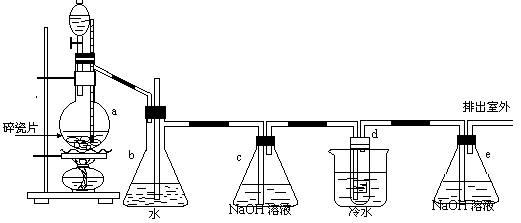 |
��д���пհף�
(1)����д���������Ʊ�1,2�����������������ѧ����ʽ
______________________________________________________________________
______________________________________________________________________
(2)������ȫƿ���Է�ֹ�����������Լ��ʵ�����ʱ�Թ�d�Ƿ�����������д����������ʱƿ
b�����________________________________________________________
(3)�� ����c��NaOH��Һ��������________________________________________
(4)�� ijѧ��������ʵ��ʱ��ʹ��һ������Һ�壬����ȫ����ɫʱ���������Ҵ���Ũ������Һ��������������³������ࡣ���װ�õ�������û�����⣬�Է������ܵ�ԭ��
_______________________________________________________________________
_______________________________________________________________________
| �÷� | ������ |
�ġ��������3С�⣬��24�֡�
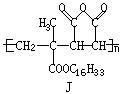
23(6��). A��B�����л���ķ���ʽ��ΪC6H12O2��Aˮ���õ�C��D��C�ܷ���������Ӧ����������Ϊһ�����壬D���ܷ�����ȥ��Ӧ��Bˮ���õ�E��F��F������������E������ͬ���칹�徭������ɵ�E�����жϣ�
(1)�� A�Ľṹ��ʽ_____________________��B�Ľṹ��ʽ__________________________________
(2)�� д��C����������Ӧ�ķ���ʽ_____________________________________________________
24(9��). ������A���緢������ţ���У������������Ǵ�л���м���壬�����������������۵ȷ����Ƶã�A�ĸ���������ϲ���IJ��Ƽ�֮һ��A��ij�ִ����Ĵ����½�������������ﲻ�ܷ���������Ӧ����Ũ��������£�A�ɷ�������ͼʾ�ķ�Ӧ��
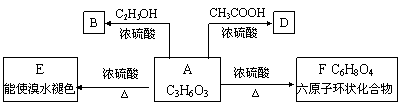 |
��д����(1) ������Ľṹ��ʽ
�������� A____________________ B____________________ D____________________
(2) ���з�Ӧ�Ļ�ѧ����ʽ����ע����Ӧ�Ļ�������
![]() A����
E____________________________________________��Ӧ��������________________
A����
E____________________________________________��Ӧ��������________________
![]() A����
F____________________________________________��Ӧ��������________________
A����
F____________________________________________��Ӧ��������________________
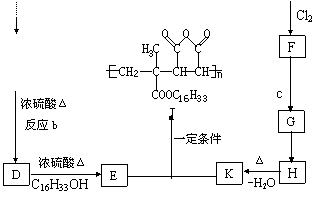
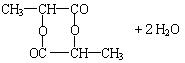
25(9��). Ϊ������������Դ��ʹ��Ч�ʣ���һЩ��Ʒ�м��뽵����J���Խ��������̵㣬����ȼ����Ʒ��ʹ�÷�Χ��J��һ�ָ߷��Ӿۺ�����ĺϳ�·�߿��������ͼ��ʾ������A���������ﲻ����������Ӧ��
| |||||
 | |||||
�����
(1)�� ��Ӧ���ͣ�a________________ b_________________ c________________
(2)�� �ṹ��ʽ��F_________________________ H____________________________
(3)�� ��ѧ����ʽ��
![]() D����E_________________________________________________________________
D����E_________________________________________________________________
![]() E+K����
J______________________________________________________________
E+K����
J______________________________________________________________
| �÷� | ������ |
�����������2С�⣬��14�֡�
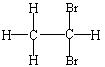
26(7��). Ϊ�ⶨij±���������������е�±ԭ�ӵ���Ŀ�����࣬�ɰ����в������ʵ�飺�� ��ȡ��±����Һ��11.4 mL���� ������������������Һ�������Һ�岻�ֲ㣻�� ��ȴ�����ϡ�����ữ���� ������������Һ��������ȫ���� ���ˣ�ϴ�ӳ���������� ��ȡ�����ij�����������
�ش��������⣺
(1)�� ��������������Һ��Ŀ����
____________________________________________________________________________
(2)�������������������Һ��Ŀ����
_____________________________________________________________________________
(3)�� ��������������Һʱ�����ij���Ϊdz��ɫ�����±�����е�±ԭ����_____________
(4)�� �����Ƹ���ij���������Ϊ37.6g����֪��±����Һ����ܶ���1.65g/cm3���������ܶ�����ͬ״���¼����ܶȵ�11.75�������±������ÿһ�������к�±ԭ�ӵ���ĿΪ______��
��±�������ܵĽṹΪ_____________________________________________
27(7��). A��B��C��������������Ԫ�ص�����������ΪC��40%��H��6.7%��O��53.3%����֪�ڱ�״���£�A�������ܶ�Ϊ1.34g/L����ͬ��ͬѹ�£�B��C�������ܶȶ���A��2������A�ܷ���������Ӧ��B�����ԣ�C�����ԣ�C��������������Һ��Ӧ���ɴ����Ρ�
(1)�� ͨ�����㣬��A��B��C�ķ���ʽ
(2)�� ����A��B��C�����ʣ�ȷ�����ǵĽṹ����д�����ǵĽṹ��ʽ
�ڶ�ѧ����ĩ����
�߶���ѧ����ο��𰸼����ֱ�
һ��ѡ���15С�⣬ÿС��3�֣���45�֡�
| ��� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| �� | D | D | B | C | A | A | C | A | B | C | B | A | D | A | D |
�����������6С�⣬��29��
16. ÿ��1��,��5��
![]() CnH2n����������������������������
�Ǽ��ԡ���ϩ���Ӿ��жԳƵĽṹ
CnH2n����������������������������
�Ǽ��ԡ���ϩ���Ӿ��жԳƵĽṹ
17. 3��
2,4��������3���һ����顡
18. ÿ���1���1�֣���5�֡�ÿ����1�ֿ�1�֣����վ����ø��֡�
E ��I�� A��B��D
|
![]() 4C2H5OH
+ O2����
4CH3CH2O + 2H2O
4C2H5OH
+ O2����
4CH3CH2O + 2H2O
20������2�֣�ԭ��2�֣���4�֡�ֻ�н���û��ԭ��ģ���ԭ����ȫ����ģ����÷֡�
�� ����ϩ���Ȼ��ⷢ���ӳɷ�Ӧ�ķ������á���Ϊ�÷�Ӧ������һ�����ʣ�û�и���Ʒ�����ȸߡ�
21��ÿʽ2�֣���4�֡�
�� CH2=CHCH=CH2�� CH2=CHCN
�����������1С�⣬8��
22��ÿ��2�֣�����ÿ��1�֣���8�֡�
![]()
|
b����ˮ����½����������е�ˮ�������������������
��ȥ��ϩ�д������������壨���ȥCO2��SO2��
��ϩ��������ͨ��Һ�壩���ٶȹ���
ʵ������У��Ҵ���Ũ����Ļ��Һû��Ѹ�ٴﵽ170 �� �����¶ȿ��Ʋ�������
�ġ��������3С�⣬��24��
23��ÿ��2�֣���6�֡�
![]()
![]() ��������������
CH3��������������������
CH3
��������������
CH3��������������������
CH3
![]() ���� (1)��HCOOCCH2CH3���� CH3CH2COOCHCH3��
���� (1)��HCOOCCH2CH3���� CH3CH2COOCHCH3��
�� CH3
![]() ����(2) HCOOH + 2Ag(NH3)2OH������ 2Ag��+ 4NH3 + CO2��+ H2O
����(2) HCOOH + 2Ag(NH3)2OH������ 2Ag��+ 4NH3 + CO2��+ H2O
24���ṹ��ʽÿʽ1�֣�����ʽÿ��2�֣���Ӧ����ÿ��1�֣���9�֡�
![]()
![]()
![]() CH3��CH��COOH����
CH3��CH��COOCH3������ CH3COOCHCOOH
��
CH3��CH��COOH����
CH3��CH��COOCH3������ CH3COOCHCOOH
��
���� OH���������������� OH���������������������� CH3
|
![]()
![]() CH3��CH��COOH��������
CH2=CH��COOH������������
��ȥ��Ӧ
CH3��CH��COOH��������
CH2=CH��COOH������������
��ȥ��Ӧ
|
 ����OH��������������
����OH��������������
![]()
![]() 2 CH3��CH��COOH��������������������������������������
ȡ����Ӧ��������
2 CH3��CH��COOH��������������������������������������
ȡ����Ӧ��������
�� OH��������������
25����Ӧ����ÿ��1�֣��ṹ��ʽÿ��1�֣�����ʽÿ��2�֣���9�֡�
(1) �ӳɡ���ȥ��ȡ������ˮ�⣩
(2) Cl��CH2��CH=CH��CH2��Cl���� HOOC��CH=CH��COOH
|
![]()
![]()
![]() (3)������������
+C16H33OH �������������������������� +
H2O��
(3)������������
+C16H33OH �������������������������� +
H2O��
|
![]()

![]() ������������������������
+����������
������������������������
+����������
�塢�������2С�⣬��14�֡�
26���ṹ��ʽÿʽ1�֣���1��2�֣�����ÿ��1�֣���7�֡�
(1) ʹ±����ˮ�⣬�������ɵ�±���ӣ��Ա����ͼ���±���ӵ��������Ŀ��
(2) ʹ±������ȫת��Ϊ±�����������Ա����ͼ���±���ӵ��������Ŀ��
(3) ��ԭ��
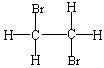 (4) 2
(4) 2
(5)���� ������������������������������������
27��7��
�� �⣺������֪����������C��H��OԪ�ص�ԭ����֮��Ϊ��
|
|
|
���ԣ��������ǵķ���ʽΪ��CH2O��n
������֪��A��Ħ������Ϊ��1.34g/L��22.4L/mol=30.0 g/ mol
�������� B��CĦ��������Ϊ30.0g/ mol��2=60g/ mol
�ɴ˵ã�A�ķ���ʽΪCH2O ��
B��C�ķ���ʽ��ΪC2H4O�������������� ........................................................4��
����A�ķ���������Ӧ����֪A�Ǽ�ȩ���ṹ��ʽΪHCHO����....................................5��
����B�����ԣ���֪BΪ���ᣬ�ṹ��ʽΪ CH3COOH������ .....................................6��
����CΪ���ԣ�����������������Һ��Ӧ���ɴ����Σ�����CΪ����������ṹ��ʽΪ
HCOOCH3�������������������������������������������� ......................................7��