2003-2004学年度上学期
高中学生学科素质训练
高二化学同步测试(5)―化学反应速率
一、选择题 (本题包括10小题,每小题2分,每小题只有一个答案符合题意)
1.决定化学反应速率的主要因素是 ( )
A.反应物的浓度 B.反应温度
C.使用催化剂 D.反应物的性质
2.在2A+B
![]() 3C+4D反应中,表示该反应速率最快的是
( )
3C+4D反应中,表示该反应速率最快的是
( )
A.v(A)=0.5 mol・L-1・s-1 B.v(B)=0.3 mol・L-1・s-1
C.v(C)=0.8 mol・L-1・s-1 D.v(D)=1 mol・L-1・s-1
3.甲、乙两个容器内都在进行A→B的反应,甲中每分钟减少4 mol A,乙中每分钟减
少2 mol A,则两容器中的反应速率 ( )
A.甲快 B.乙快 C.相等 D.无法确定
4.20℃时,将0.1 mol・L-1Na2S2O3溶液10 mL和0.01 mol・L-1 H2SO4溶液10 mL混合,2 min后溶液中明显出现浑浊,已知温度每升高10℃,化学反应速率增大到原来的2倍,那么50℃时,同样的反应要看到同样的浑浊,需要的时间是 ( )
A.40 s B.15 s C.48 s D.20 s
5.某温度下,浓度都是1 mol・L-1的两种气体X2和Y2,在密闭容器中反应生成气体
Z,经过t min后,测得物质的浓度分别为:
c(X2)=0.4 mol・L-1,c(Y2)=0.8 mol・L-1,c(Z)=0.4 mol・L-1,
则该反应的反应式可表示为: ( )
A.X2+2Y2 ![]() 2XY2 B.2X2+Y2
2XY2 B.2X2+Y2 ![]() X2Y
X2Y
C.3X2+Y2 ![]() 2X3Y D.X2+3Y2
2X3Y D.X2+3Y2 ![]() 2XY3
2XY3
阅读下题,回答6―7题
把0.6 mol X气体和0.4 mol Y气体混合于2 L容器中,发生反应:
3X(g)+Y(g) ![]() nZ(g)+2W(g),5 min末已生成0.2
mol W,若测
nZ(g)+2W(g),5 min末已生成0.2
mol W,若测
知以Z浓度变化来表示的平均速率为0.01 mol・L-1・min-1
6.上述反应中Z气体的计量系数n的值是 ( )
A.1 B.2 C.3 D.4
7.上述反应在5 min末时,已用去的Y占原来总物质的量分数为 ( )
A.20% B.25% C.33% D.50%
8.用3克块状大理石与30毫升3摩/升盐酸反应制取CO2气体,若要增大反应速率,可
采取的措施是①再加入30毫升3摩/升盐酸 ②改用30毫升6摩/升盐酸
③改用3克粉末状大理石 ④适当升高温度 ( )
A.①②④ B.②③④ C.①③④ D. ①②③
9.在一个容积为6 L的密闭容器中,放入3 L X(g)和2 L Y(g),在一定条件下发生反
应: 4X(g)+nY(g) ![]() 2Q(g)+6R(g)
2Q(g)+6R(g)
反应达到平衡后,容器内温度不变,混合气体的压强比原来增加了5%,X的浓度减
小1/3,则该反应中的n值为 ( )
A.3 B.4 C.5 D.6
10.反应4NH3(气)+5O3(气)![]() 4NO(气)+6H3O(气)在10L密闭容器中进
4NO(气)+6H3O(气)在10L密闭容器中进
行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率V (X)(反应物
的消耗速率或产物的生成速率)可表示为 ( )
A.V(NH3)=0.0101mol.L-1.s-1 B.V(O2)=0.0010mol.L-1.S-1
C.V(NO)=0.0010mol.L-1.s-1 D.V(H2O)=0.045mol.L-1.s-1
二、选择题(本题包括11小题,每小题3分,共33分。每题有1-2个选项符合题,少选
扣2分,多选、错选均不给分)
11.反应4NH3(气)+5O2(气) ![]() 4NO(气)+6H2O(气)在2升的密闭容器中进行,1 分钟
4NO(气)+6H2O(气)在2升的密闭容器中进行,1 分钟
后,NH3减少了0.12摩尔,则平均每秒钟浓度变化正确的是 ( )
A.NO:0.001摩/升 B.H2O:0.002摩/升
C.NH3:0.002摩/升 D.O2:0.00125摩/升
12.目前普遍认为,质子和中子都是由被称为u夸克和d夸克的两类夸克组成。u夸克
带电量为![]() e,d夸克带电量
e,d夸克带电量![]() e,e为基元电荷。下列论断可能正确的是 ( )
e,e为基元电荷。下列论断可能正确的是 ( )
A.质子由1个u夸克和1个d夸克组成,中子由1个u夸克和2个d夸克组成
B.质子由2个u夸克和1个d夸克组成,中子由1个u夸克和2个d夸克组成
C.质子由1个u夸克和2个d夸克组成,中子由2个u夸克和1个d夸克组成
D.质子由2个u夸克和1个d夸克组成,中子由1个u夸克和1个d夸克组成
13.在一定条件下,反应N2+3H2![]() 2NH3,在2L密闭容器中进行,5min内氨的质量增
2NH3,在2L密闭容器中进行,5min内氨的质量增
加了1.7g,则反应速率为 ( )
A.V(H2)=0.03mol/L・min B.V(N2)=0.02mol/L・min
C.V(NH3)=0.17mol/L・min D.V(NH3)=0.01mol/L・min
14.在一个容积为2L的密闭容器中,发生如下反应:3A+B=2C (A.B.C均为气体)若最初加
入的A.B都是4mol,A的平均反应速率为0.12mol/L・s,则10s后容器中的B是 ( )
A.2.8mol B.1.6mol C.3.2mol D.3.6mol
15.下列关于催化剂的说法,正确的是 ( )
A.催化剂能使不起反应的物质发生反应
B.催化剂在化学反应前后,化学性质和质量都不变
C.催化剂能改变化学反应速率
D.任何化学反应,都需要催化剂
E:电解水时,往水中加少量NaOH,可使电解速率明显加快,所以NaOH是这个反
应的催化剂
16.在一定条件下,将A2和B2两种气体通入1L密闭容器中,反应按下式进行:
xA2+yB2
![]() 2C(气),两秒种后反应速率如下V(A2)=0.4mol/(L・s)
2C(气),两秒种后反应速率如下V(A2)=0.4mol/(L・s)
V(B2)=1.2 mol/(L・s) VC= 0.8mol/(L・s) 则该x和y的值分别为 ( )
A.2和3 B.3和2 C.3和1 D.1和3
17.在N2+3H2![]() 2NH3的反应中,经过一段时间后,NH3的浓度增加0.6mol/L,
2NH3的反应中,经过一段时间后,NH3的浓度增加0.6mol/L,
在此时间内用H2表示的平均反应速率为0.45 mol/L・s,则所经历的时间是 ( )
A.0.44s B.1s C.1.33s D.1.2s
18.把下列4种X的溶液分别加入4个盛有10mL 2mol/L盐酸的烧杯中,均加水稀到
50mL,此时X和盐酸和缓地进行反应。其中反应速率最大的是 ( )
A.20mL 3mol/L X 的溶液 B.20mL 2mol/L X 的溶液
C.10ml 4mol/L X 的溶液 D.10mL 2mol/L X 的溶液
19.一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,
可向盐酸中加入适量的 ( )
A..NaOH固体 B.H2O
C.NH4Cl固体 D.CH3COONa固体
20.下列四个数据都表示合成氨的反应速率,其中速率代表同一反应中的是 ( )
①V(N2)=0.3mol/L・min ②V(NH3)=0.9mol/L・min
③V(H2)=0.6mol/L・min ④V(H2)=0.0225mol/L・s
A.①② B.①③ C.③④ D.②④
21.将纯净的N2和H2按体积比2∶3混合后,缓缓通人一个正在加热的装有足量催化剂
的硬质管,在硬质管的另一端收集到的气体是 ( )
A.NH3和N2 B.NH3和H2
C.纯净的NH3 D. NH3、H2和N2的混合气体
三、填空题(本题包括7小题,共36分)
22.(5分)对于反应:2SO2+O2 ![]() 2SO3,当其他条件不变时,只改变一个反应条
2SO3,当其他条件不变时,只改变一个反应条
件,将生成SO3的反应速率的变化填入空格里(填写“增大”“减小”“不变”)
| 编 号 | 改变的条件 | 生成SO3的速率 |
| ① | 升高温度 | |
| ② | 降低温度 | |
| ③ | 增大O2的浓度 | |
| ④ | 使用V2O5作催化剂 | |
| ⑤ | 压缩体积 |
 23.(4分)某温度时,在2 L容器中,X、Y、Z三种物质的物质的
23.(4分)某温度时,在2 L容器中,X、Y、Z三种物质的物质的
量随时间变化曲线图2―3所示。由图中数据分析,该反应的
化学方程式为:
_________________________________________________。
反应开始至2 min,Z的平均反应速率为__________。
24.(6分)取a mol A和b mol B置于V L容器中,发生可逆反应:
aA(g)+bB(g) ![]() cC(g)+dD(g),1 min后,
cC(g)+dD(g),1 min后,
测得容器内A的浓度为x mol・L-1,这时B的浓度为:
_____ ;C的浓度为:________。在这段时间内反应速率若以物质A的浓度变化来表示,应为__________。
 25.(6分)将镁带投入盛放在敞口容器的盐酸里,产生H2的速
25.(6分)将镁带投入盛放在敞口容器的盐酸里,产生H2的速
率与时间的关系可由图2―20表示。
在下列因素中①盐酸的浓度 ②镁带的表面积
③溶液的浓度 ④氢气的压强 ⑤Cl-的浓度
(1)影响反应速率的因素__________;
(2)解释图中AB段形成的原因__________;
(3)解释图中t1时刻后速率变小的原因__________。
26.(6分)将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应
3A(g)+B(g)![]() xC(g)+2D(g),经过4min时,测得D的浓度为0.5 mol/L
xC(g)+2D(g),经过4min时,测得D的浓度为0.5 mol/L
c(A)∶c(B)=3∶5,C的反应速率是0.1 mol・L-1・min-1,A在4 min末的
浓度是 _______ ,B的平均反应速率是 ________ ,x的值是 。
27.(5分)在密闭容器里,通入x mol H2和y mol I2(g),改变下列条件,反应速率将
如何改变?(填“增大”“减小”或“不变”)
(1)升高温度 ; (2)加入催化剂 ;
(3)充入更多的H2 ; (4)扩大容器的体积 ;
(5)容器容积不变,通入氖气 。
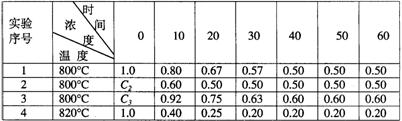
28.(5分) 某化学反应2A![]() B+D在四种不同条件下进行,B、D起始浓度为及反应
B+D在四种不同条件下进行,B、D起始浓度为及反应
A的浓度(mol/L)随反应时间(min)的变化情况如下表:
|
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为 mol/(L・min)。
(2)在实验2,A的初始浓度C2= mol/L,反应经20分钟就达到平衡,可推
测实验2中还隐含的条件是 。
(3)设实验3的反应速率为V3,实验1的反应速率为V1,则V3 V1(填>、=、
<=,且C3 1.0mol/L(填>、=、<=)
四、计算题(共10分)
29.一定温度下,在密闭容器中,发生反应:2NO2 ![]() 2NO+O2,经过一定时间后,
2NO+O2,经过一定时间后,
测得混合气中NO2浓度为0.06 mol・L-1,O2的浓度为0.12 mol・L-1,且各物质的
浓度不再发生变化,
求:(1)NO2的起始浓度?
(2)此时NO2的分解率?
30.A、B两种气体在一定条件下发生反应:mA(g) + nB(g) = pC(g) + qD(g)。取a mol A
和b mol B置于容积为V L的容器内,1 min后,测得容器内A的浓度为x mol/L
求:此时B的浓度和C的
参考答案
一、选择题 (本题包括10小题,每小题2分,每小题只有一个答案符合题意)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| D | B | D | B | C | A | B | B | D | C |
二、选择题(本题包括11小题,每小题3分,共33分。每题有1-2个选项符合题,少选
扣2分,多选、错选均不给分)
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| AD | B | D | C | BC | D | D | A | BD | D |
| 21 | |||||||||
| D |
三、填空题
22、①增大②减小③增大④增大⑤增大
23、3X + Y![]() 2Z;0.05 mol/L・min
2Z;0.05 mol/L・min
24、![]() ;
;![]() ;
;![]() mol/L・min
mol/L・min
25、⑴①②③;⑵镁条与盐酸反应放热,温度升高,反应速度加快;
⑶反应进行,盐酸浓度减小,反应物浓度减小,反应速度减慢
26、0.75 mol/L;0.0625 mol/L・min;2
27、⑴增大⑵增大⑶增大⑷减小⑸不变
28、⑴0.013 ⑵1.0;催化剂 ⑶ >;>
29、⑴0.3 mol/L ⑵80%
30、CB = 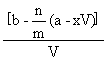 mol/L
mol/L
CC = ![]() mol/L
mol/L