武汉市高三年级理科综合一月调考试题
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分150分。考试时间120分钟。
第Ⅰ卷(选择题 共20题 每题6分 共120分)
在下列各题的四个选项中,只有一个选项是最符合题目要求的。
以下数据可供解题时参考:
相对原子质量:H―1 C―12 N―14 O―16 Na―23 Al―27
1.下列物质和结构中不含糖成分的是 ( )
A.生长素 B.核糖体 C.ATP D.DNA
2.下列物质转变过程属于光反应的是 ( )
NADP+ ATP CO2 叶绿素a
①↑↓② ③↑↓④ ⑤↑↓⑥ ⑦↑↓⑧
NADPH ADP C6H12O6 失去电子的叶绿素a
A.①③⑤⑦ B.①②④⑧ C.②③⑦⑧ D.①④⑦⑧
|
A.Ⅰ+Ⅱ是有性生殖过程
B.Ⅲ过程是在细胞分裂和细胞分化基础上进行的
C.有性生殖实现了基因重组,增强了生物变异性
D.由于有性生殖方式的出现,加快了生物进化的进程
4.下列可以确定为遗传病的是 ( )
A.艾滋病母亲生下艾滋病婴儿
B.母亲是色盲基因的携带者(XBXb),其子是色盲
C.母亲是Rh阴性血型(Rh―Rh―),其子也是Rh阴性血型
D.母亲患癌症,其子也患癌症
5.甲是一种能生活在多种土壤中的小型昆虫,常常被昆虫乙大量捕食。现用两种杀虫剂分
别处理田块,Ⅱ号杀虫剂对甲、乙昆虫的毒性相同,Ⅰ号杀虫剂对乙昆虫的毒性比对甲
昆虫的毒性更强。下列哪两个图能分别代表Ⅰ、Ⅱ号杀虫剂单独作用对害虫数量的影响
|
A.①③ B.②④ C.①④ D.②③
6.如欲利用细菌大量生产人胰岛素,则下列叙述不正确的是 ( )
A.需有适当运载体将人胰岛素基因置入细菌
B.需有适当的酶对运载体与人胰岛素基因进行切割与黏合
C.重组后的运载体DNA,须在细菌体内转录、翻译成人胰岛素
D.生产人胰岛素的细胞工程技术也可生产疫苗
7.下列变化过程中,无化学键断裂或生成的是 ( )
A.石墨转化为金刚石 B.NaCl晶体溶于水
C.干冰升华 D.HCl溶于水
8.下列说法正确的是(NA为阿伏加德罗常数) ( )
A.在标准状况下,1mol三氧化硫的体积约为22.4L
B.在1L、1mol/L的FeCl3溶液中,Fe3+的个数为NA
C.在1mol的Na2O2中,有2NA个阴离子
D.在1mol甲基(―CH3)中,原子核外存在9NA个电子
9.下列保存试剂的方法正确的是 ( )
A.氨水一般盛装在玻璃容器、橡皮袋、陶瓷坛或内涂沥青的铁桶里
B.少量的锂、钠、钾均可保存在煤油中
C.浓硝酸应保存在带橡皮塞的棕色细口瓶中
D.用排水法收集满一瓶氢气,用玻璃片盖住瓶口,瓶口朝上放置
10.具有相同质子数的两种不同粒子 ( )
A.一定是同位素 B.一定是一种分子和一种离子
C.一定是两种不同的离子 D.无法判断
11.常温下,在10mL、0.2mol/L氨水中,滴入0.2mol/L的稀盐酸,使溶液pH=7。则下列说法正确的是 ( )
A.加入盐酸的体积大于10mL B.c(NH4+)=c(Cl-)
C.加入盐酸的体积等于10mL D.c(NH4+)<c(Cl-)
12.吗丁啉是一种常见的胃药,其有效成分的结构简式可用下图表示。关于该物质的下列说法不正确的是 ( )
|
A.该物质的分子式为C22H24ClN5O2 B.该物质具有碱性,能与酸反应
C.该物质不能发生水解反应 D.该物质能发生取代反应和加成反应
13.一定温度下,mg下列物质在足量的氧气中充分燃烧后,产物与足量的过氧化钠充分反应,过氧化钠增加了ng,且n>m,符合此要求的物质是 ( )
①H2 ②CO ③CO和H2的混合物 ④HCOOCH3 ⑤CH3CHO
A.⑤ B.①② C.①②③④ D.①②③④⑤
14.关于波动,下列说法正确的是 ( )
A.多普勒效应是声波特有的现象
B.光的偏振现象说明光是一种纵波
C.电子束通过铝箔时可能产生衍射图样
D.相同频率的声波与无线电波相遇,一定产生干涉现象
15.下列说法正确的是 ( )
A.在显微镜下观察到的布朗运动就是分子的运动
B.分子间的距离越小,分子引力越小,斥力越大
C.不可能使热量由低温物体传递到高温物体
D.一定质量的理想气体若体积不变,吸收热量,则压强变大
16.神州五号载人飞船返回舱以超高速进入大气层时,返回舱表面附近形成一个温度高达几千摄氏度的高温区。高温区内的气体和返回舱表面材料的分子被分解和电离,这时返回舱与外界的联系中断,这种现象就称为黑障。其原因是 ( )
A.飞船受到万有引力消失
B.飞船为了安全而暂时关闭通讯系统
C.在飞船周围高温气体被电离成等离子体,从而对飞船起屏蔽作用
D.飞船表面温度太高,如同火球,使得航天员看不见外面,外面也看不见飞船里面
17.下列说法正确的是 ( )
A.光导纤维丝的内芯材料的折射率比外套材料的折射率小
B.氢原子由低能级向高能级跃迁时,原子系统总能量增加
C.轻核结合成较重质量的原子核时,总质量一定增加,吸收能量
D.某金属在单色光照射下发射出光电子的最大动能随照射光波长的增大而增大
18.有一个电子器件,当其两端的电压高于100V时则导通,等于或低于100V时则不导通。若把这个电子器件接到100V、50Hz的正弦交变电源上,这个电子器件将 ( )
A.不导通 B.每次导通的时间为0.01s
C.每秒导通50次 D.每秒导通100次
19.加速上千的升降机顶部悬有一轻质弹簧,弹簧下端挂有一小球,若升降机突然停止,以升降机底板为参照物,小球在继续上升的过程中 ( )
A.动能逐渐减小 B.动能先增大后减小
C.加速度逐渐增大 D.加速度逐渐减小
20.点电荷Q1、Q2产生的静电场的等势面如图中实线所示,标在等势面上的数值分别表示该等势面的电势,a、b、c…表示等势面上的点,下列说法正确的是 ( )
A.点电荷在d点受电场力的方向指向Q1
B.b点的场强与d点的场强大小相等
C.把+1C的点电荷从c点移到d点过程中电场力所做的功等于-3kJ
D.把+1C的点电荷从a点移到c点过程中电势能减少1kJ
|
第Ⅱ卷(非选择题 共180分)
21.(20分)某同学准备用100![]() A的电流表改装成一块量程为2.0V的电压表。他为了能够
A的电流表改装成一块量程为2.0V的电压表。他为了能够
|
数如下:
A.电流表G1(量程1.0mA,内电阻约100![]() )
)
B.电流表G2(量程500![]() A,内电阻约200
A,内电阻约200![]() )
)
C.电池组E(电动势为3.0V,内电阻未知)
D.滑线变阻器R(0~25![]() )
)
E.四旋纽电阻箱R1(总阻值9999![]() )
)
F.保护电阻R2(阻值约100![]() ) G.开关S1,单刀双掷开关S2
) G.开关S1,单刀双掷开关S2
(1)实验中该同学先合上开关S1,再将开关S2与![]() 相连,调节滑线变阻器R,当电流表G2
相连,调节滑线变阻器R,当电流表G2
有某一合理的示数时,记下电流表G1的示数I;然后将开关S2与![]() 相连,保持
相连,保持
不变,调节
,使电流表G1的示数仍为I时,读取电阻箱的读数![]() 。
。
(2)由上述测量过程可知,电流表G2内电阻的测量值![]() 。
。
(3)若该同学通过测量得到电流表G2的内电阻值为190![]() ,他必须将一个
,他必须将一个
|
(4)该同学把改装的电压表与标准电压表V0进行了核对,
发现当改装的电压表的指什刚好指向满刻度时,
标准电压表V0的指针恰好如图2所示.由此可知,
该改电压表的百分误差为 %。
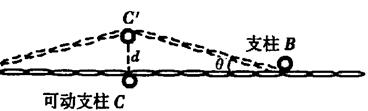
22.(18分)电梯修理员或牵引专家常常需要监测金属绳中的张力,但不能到绳的自由端去
直接测量.某公司制造出一种能测量绳中张力的仪器,工作原理如图所示,将相距为L的
两根固定支柱A、B(图中小圆框表示支柱的横截面)垂直于金属绳水平放置,在AB
的中点用一可动支柱C向上推动金属绳,使绳在垂直于AB的方向竖直向上发生一个偏
移量![]() ,这时仪器测得绳对支柱C竖直向下的作用力为F.
,这时仪器测得绳对支柱C竖直向下的作用力为F.
(1)试用L、![]() 、F表示这时绳中的张力T.
、F表示这时绳中的张力T.
|
|
23.(18分)长为L、质量为M的铁板放在水平地面上,铁板与地面间的动摩擦因数为![]() ,
,
一质量为![]() 的人,从铁板的一端匀加速地跑向另一端,到达另一端时骤然停在铁板上,
的人,从铁板的一端匀加速地跑向另一端,到达另一端时骤然停在铁板上,
人在跑动过程中铁板刚好不滑动(铁板受到的最大静摩擦力等于滑动摩擦力)。求:
(1)人在铁板上跑动的加速度多大?
(2)人跑至铁板另一端骤然停止前时的速度多大?

 (3)人相对铁板骤然停止后,人和铁板一起向前运动,铁板在水平地面上移动的最大距离
(3)人相对铁板骤然停止后,人和铁板一起向前运动,铁板在水平地面上移动的最大距离
是多少。
24.(14分)以下是某同学关于酶特性的实验操作步骤,请根据要求回答:
| 步 骤 1 | 操作方法 | 试 管 | |
| Ⅰ | Ⅱ | ||
| 1 | 注入可溶性淀粉溶液 | 2mL | ― |
| 2 | 注入蔗糖溶液 | ― | 2mL |
| 3 | 注入斐林试剂 | 2mL | 2mL |
| 4 | 注入新鲜的某种酶溶液 | 2mL | 2mL |
| 5 | 酒精灯隔水加热 | 煮沸1min | |
| 6 | 观察现象 | A | B |
(1)若该实验的目的是验证酶作用的专一性,则步骤4可以选用 或
两种不同类别的酶。
(2)如果按上述步骤进行操作,分析A、B可能出现的现象及原因:
现象:
原因:
(3)该实验步骤中存在明显的缺陷,请写出正确的操作步骤(注:可直接用上表步骤中的
数字表示,需增加的步骤用文字表述):
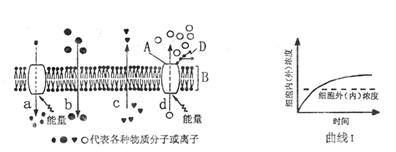
|
(1)图中A代表 。在a~d过程中,可以代表甘油由肠腔进入小肠上
皮细胞的过程是图中编号 ,与曲线I相符的过程是图中编号 。
(2)当温度升高时,B的厚度变小,这说明细胞膜具有 的特点;下列现象
中与该特点不直接相关的是 (A.受精作用 B.细胞融合
C.吞噬细胞吞噬抗原 D.神经纤维上兴奋的传导。)
(3)与正常细胞的细胞膜相比,衰老细胞的细胞膜的 功能改变,使物质运输功
能下降;癌细胞易扩散、易转移是由于图中物质 的减少,进一步引起细胞
之间的黏着性下降而造成的。
26.(6分)下列反庆分别表示物质代谢中的何过程:
|
|
①
②
27.(12分)2003年10月16日“神舟五号”飞船成功发射,实现了中华民族的飞天梦想。
运送飞船的火箭燃料除液态双氧水外,还有另一种液态氮氢化合物。已知该化合物中氢
元素的质量分数为12.5%,相对分子质量为32,结构分析发现该分子结构中只有单键。
(1)该氮氢化合物的电子式为 。
(2)若64g该物质与液态双氧水恰好完全反应,产生两种无毒又不污染环境的气态物质,
还放出3000kJ的热量。写出该反应的热化学方程式 。
(3)NH3分子中的N原子有一对孤对电子,能发生反应:NH3+HCl=NH4Cl。试写出上述氮
氢化合物通入足量盐酸时,发生反应的化学方程式 。
28.(12分)已知:下图中的物质均为中学化学中常见物质;常温下,A、C、F、H、J、K
为固体,D、G为气体;A为常见金属单质;B为重要的工业原料,可用于制备炸药,
其浓溶液通常呈黄色;E的溶液呈黄色;C、D均为由两种短周期元素组成的化合物;G
 为动植物生命活动中不可缺少的物质;方框中字母代表反应物或生成物(部分生成物已
为动植物生命活动中不可缺少的物质;方框中字母代表反应物或生成物(部分生成物已
略去)。
试填空:
(1)B的名称 ;A在周期表中的位置 。
|
![]() 离子反应方程式:E+F H+I+D:
。
离子反应方程式:E+F H+I+D:
。
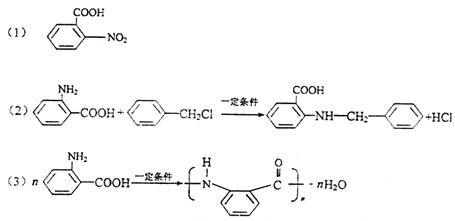
29.(12分)据《中国制药》报道,化合物F是用于制备“非典”药品(盐酸祛炎痛)的中
间产物,其合成路线为:
 |
|
![]() (Ⅰ)RNH2+
(Ⅰ)RNH2+![]() CH2Cl
RNHCH2
CH2Cl
RNHCH2![]() +HCl(R和
+HCl(R和![]() 代表烃基)
代表烃基)
(Ⅱ)苯的同系物能被酸性高锰酸钾溶液氧化,如:
 |
(Ⅲ) (苯胺,弱碱性,易氧化)
|
(Ⅳ) 与浓硫酸、浓硝酸混合在不同温度下会得到不同产物。
回答下列问题:
(1)C的结构简式是 。
(2)D+E→F的化学方程式:
。
(3)E在一定条件下,可聚合成热固性很好的功能高分子,写出合成此高聚物的化学方程
。
(4)反应①~⑤中,属于取代反应的是(填反应序号) 。
30.(14分)在一容积为2.0L且容积不变的密闭容器中加入适量碳粉和0.20mol H2O。
在800℃条件下,经20s后达到如下化学平衡(第一平衡):
|
已知平衡时,CO为0.12mol。试填空:
(1)若用![]() (H2O)表示该反应前20s内平均速率,则
(H2O)表示该反应前20s内平均速率,则![]() (H2O)=
。
(H2O)=
。
(2)若在上述平衡混合物中加入少量Na2O固体,并在此温度下再次达到新的平衡(第二平
衡),则平衡时H2的物质的量 (填“增大”“减小”或“不变”)。理由是
。
(3)若向上述第一平衡的混合物中再充入amolH2(a<0.12)在相同条件下达到新的平衡(第
三平衡)此时,CO的物质的量n的联欢会范围是 。
|
备反应原理为:Al2O3+N2+3C 2AlN+3CO。制备过程中,原料配比不当或反应不完
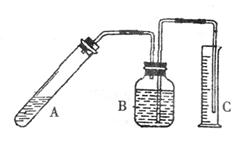
全等因素都会造成产品中含有碳或Al2O3等杂质。为测定产品中AlN的质量分数,某同
学按下图装置进行相关实验。可选用的化学试剂为:
![]() 氮化铝片状固体、NaOH饱和溶液、水、煤油、医用酒精。
氮化铝片状固体、NaOH饱和溶液、水、煤油、医用酒精。
|
(1)简述检查该套装置气密性的方法
。
(2)右图B中试剂最好选用(填序号):
。
①水 ②煤油 ③医用酒精
已知A 中有NaAlO2生成,并放出有刺激性气
味气体,写出A中发生反应的化学方程式
。
(3)读取C(量筒)中液体体积时,应注意 。(填序号)
a.C中液面不再上升时立即读数 b.上下移动C,使之液面与B中液面相平
c.A中不再有气泡逸出 d.视线与凹液面最低处相平
(4)mg氮化铝与足量NaOH饱和溶液反应,实验结束后,C中收集到液体的体积为VL(已
折算成标准状况),则AlN样品的纯度为 (写计算表达式)。
(5)上述实验方案,可能因气体体积测量不准,导致误差较大。有人建议改用下列A、B两
个装置中的一种(在通风橱内进行),只需进行简单而又必要的数据测写,用差量法就
|
32.(22分)质量为![]() 、带电荷量为+
、带电荷量为+![]() 的绝缘小珠,穿在半径为
的绝缘小珠,穿在半径为![]() 的光滑圆形轨道上,轨道
的光滑圆形轨道上,轨道
平面水平,空间有分布均匀且随时间变化的磁场,磁场方向竖直向上,如图1所示. 磁
感应强度B(![]() )的变化规律如图2所示.
)的变化规律如图2所示.
(1)若圆环由金属材料制成,求圆环上感应电动势![]() 的大小,
的大小,
(2)若圆环由绝缘材料制成,已知在![]() 内,圆环处的感应电场的场强方向是沿顺时针并
内,圆环处的感应电场的场强方向是沿顺时针并
指向圆环的切线方向、大小为E=![]() ,
,![]() 时刻小珠静止.求
时刻小珠静止.求![]() 时,轨道对小珠
时,轨道对小珠
的作用力F 的大小(小珠重力不计).
| |||
| |||
理科综合答案及评分参考
|
21.(20分)
(1)电阻R;电阻箱R1…………8分
(2)r ……4分 (3)3.81 ……4分
(4)5.26 ……4分
22.(18分)(1)设c′点受两边绳的张力为T1和T2,![]() 的夹角为θ,如图所示。依对称性有 T1=T2=T
由力的合成有 F=2Tsinθ ① ……4分
的夹角为θ,如图所示。依对称性有 T1=T2=T
由力的合成有 F=2Tsinθ ① ……4分
根据几何关系有 sinθ= ② ……4分
② ……4分
联立①②解得 T=![]() ③ ……4分
③ ……4分
因d<<L,故 ![]() ④ ……2分
④ ……2分
说明:根据①②式,运用近似运算sinθ≈tanθ,得出④,第(1)问得14分。
(2)将d=10mm,F=400N,L=250mm代入③或④,解得 T=2.5×103N ⑤ ……4分
即绳中的张力为2.5×103N
23.(18分)(1)铁板刚好不动时,以人为研究对象,设人受铁板的静摩擦力为f,人跑动的
加速度为a,根据牛顿第二定律有 f=ma ① ……2分
设人对铁板的静摩擦力为f′,根据牛顿第三定律有 f′= f ② ……1分
以铁板为研究对象,根据力的平衡有 ![]() ③ ……2分
③ ……2分
联立①②③解得人的加速度 ![]() ……3分
……3分
(2)设人跑到另一端骤然停止前时的速度大小为v,根据匀加速运动速度一位移关系,有 ![]() ④ ……2分 解得
④ ……2分 解得![]() ……2分
……2分
(3)人骤然停止跑动时,人和铁板系统动量守恒,设人和铁板的共同速度为![]() ,有
,有
![]() ⑤ …… 2分
⑤ …… 2分
设铁板向前滑动的最大距离为s,由动能定理
![]() ⑥ ……2分 解得
⑥ ……2分 解得 ![]() ……2分
……2分
以下为评分参考,阅卷时可依题意,选择其它合理答案:
24.(14分)(1)蔗糖酶 淀粉酶(或答唾液淀粉酶 α-淀粉酶)(4分)
(2)现象:可能A、B都不能形成砖红色沉淀 (2分)
原因:①先加斐林试剂再加酶,斐林试剂可能对酶活性有影响 (2分)
②加入酶溶液后,直接加热煮沸,既可能使酶不能充分催化反应,又可能使酶失去活性而无催化作用…………………………(2分)
(3)1→2→4→适应温度条件下,保温5min→3→5→6 (4分)
25.(14分)(1)载体蛋白 (2分) b (2分) a、d(2分)
(2)一定的流动性 (2分) D(2分) (3)通透性(2分) D(2分)
26.(6分)①氨基转换作用(3分) ②脱氨基作用(3分)
![]() H H
H H
27.(1)H:N:N:H (2)N2H4(l)+2H2O2(l)=N2(g)+4H2O(g);△H=-1500kJ・mol-1
(3)N2H4+2HCl=N2H6Cl2(若写成N2H5Cl,不得分)(每空4分,共12分)
28.(1)硝酸 第四周期,Ⅷ族 (2)2Na2O2+2CO2=2Na2CO3+O2
2Fe3++2CO32―+3H2O=2Fe(OH)3↓+3CO2↑(每空4分,共12分)
|
(4)①、②、⑤ (每空3分,共12分)
30.(1)0.0030mol・L―1・s―1 (2)减小。Na2O与H2O反应,使水蒸气浓度降低,平衡向左移动。
(3)(0.12-a)<n<0.12 (第2空2分,其余每空4分,共14分)
31.(1)将C中导管浸入水中,微热试管A,C中导管出口有气泡逸出。冷却后,C中导管仍有高出液面的水柱不下降。(或先在B中加入煤油,然后将试管A放入冰水中,B中导管有气泡进入B,将试管A恢复室温,B中导管有高出液面的油柱不下降。)(其它合理答案均可给分)
(2)② AlN+NaOH+H2O=NaAlO2+NH3↑
(3)b,c,d (4)![]() (5)A (每空3分,共18分)
(5)A (每空3分,共18分)
32.(22分)(1)由图2可知,当t<T时,磁感应强度B随时间t均匀增强,根据法拉第电磁感应定律有 ![]() ……2分
……2分
又 ![]() ……6分
……6分 ![]() ……2分
……2分
得 ![]() ……2分
……2分
在t≥T时,磁场稳定不变,通过圆环所围面积内的磁通量不再改变,则
![]() ……2分 因而感应电动势ε=0
……2分 因而感应电动势ε=0
(2)在t<T时,根据电磁场理论,空间产生感应电场,在圆环上感应电场的方向指向圆环的切线方向(顺时针),故小珠在圆环上做变加速圆周运动。在求解小珠的线速度时,可将小珠在圆环切线方向上的运动等效为匀加速直线运动。
则t时刻小珠的速度 ![]() …………1分
…………1分
电荷沿圆环切线方向的加速度![]() ……1分
……1分
由场强定义知 F电=qE …………1分 依题意 ![]() …………1分
…………1分
解得![]() …………1分 当t=T时,
…………1分 当t=T时,![]() …………1分
…………1分
当t>T时,ε2=0,则E2=0,此后由轨道对小珠的
作用力F和小珠受到的洛仑兹f共同提供小珠做匀
速圆周运动的向心力,线速度为v2…………1分
|
由洛仑兹力公式有 ![]() ……1分
……1分
F的大小为 ![]() ……1分
……1分
F的方向时刻背离圆环的中心。
以上为评分参考,阅卷时可依题意,选择其它合理答案。