普通高校统一考试理科综合能力测试(江西卷)
第I卷(选择题共:126分)
以下数据可供解题时参考:
相对原子质量(原子量): C 12 O 16 Na 23
一、选择题( 本题包括 13 小题。每小题只有一个选项符合题意 )
1、人体神经细胞与肝细胞的形态结构和功能不同,其根本原因是这两种细胞的
A. DNA 碱基排列顺序不同 B.核糖体不同
C. 转运 RNA 不同 D.信使 RNA 不同
2、在光照下,供给玉米离体叶片少量的14CO2,随着光合作用时间的延续.在光合作用固定CO2形成的C3化合物和C4化合物中, 14C含量变化示意图正确的是
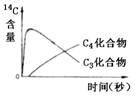
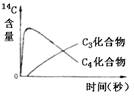
A B
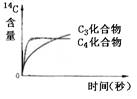
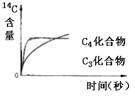
C D
3、镰刀型细胞贫血症的病因是血红蛋白基因的碱基序列发生了改变。检测这种碱基碱基序列改变必须使用的酶是
A.解旋酶 B. DNA 连接酶 C.限制性内切酶 D.RNA 聚合酶
4、将小麦种子分别置于 20 ℃ 和 30℃ 培养箱中培养 4 天,依次取等量的萌发种子分别制成提取液 I 和提取液Ⅱ。取三支试管甲、乙、丙,分别加入等量的淀粉液,然后按下图加入等量的提取液和蒸馏水,45℃水浴保温分钟.立即在 3 支试管中加人等量斐林试剂并煮沸2分钟.摇匀观察试管中的颜色。结果是
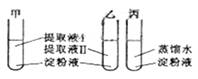 A.甲呈蓝色,乙呈砖红色,丙呈无色
A.甲呈蓝色,乙呈砖红色,丙呈无色
B.甲呈无色,乙呈砖红色,丙呈蓝色
C.甲、乙皆呈蓝色,丙呈砖红色
D.甲呈没砖红色,乙呈砖红色,丙呈蓝色
5、为了保护鱼类资源不受破坏.并能持续地获得最大捕鱼量。根据种群
增长的S型曲线,应使被捕鱼群的种群数量保持在K/2水平,这是因为在这个水平上
A.种群数量相对稳定 B.种群增长量最大
C.种群数量最大 D.环境条件所允许的种群数量最大
6、下列分子中所有原子都满足最外层为 8电子结构的是
A.BF3 B.H2O C.SiCl4 D.PCl5
7、等物质的量的主族金属A、B、C 分别与足量的稀盐酸反应,所得氢气的体积依次为VA、VB、VC,已知VB =2 VC,且VA= VB + VC,则在C的生成物中,该金属元素的化合价为
A.+1 B.+2 C.+3 D.+4
8、已知 Q 与 R 的摩尔质量之比为 9:22 .在反应 X + 2Y = 2Q + R 中,当 1.6g X与 Y 完全反应后,生成 4.4gR , 则参与反应的 Y 和生成物 Q 的质量之比为
A.46:9 B.32:9 C.23:9 D.16:9
9、下列说法中正确的是
A.非金属元素呈现的最高化合价不超过该元素原子的最外层电子数
B.非金脚元素呈现的最低化合价,共绝对值等于该元素原子的最外层电子数
C.最外层有 2 个电子的原子都是金属原子
D.最外层有5个电子的原子都是非金属原子
10、在 pH= 1的溶液中,可以大量共存的离子是
A.K+、Na+、SO42-、S2O32- B.NH4+、Mg2+、SO42-、 Cl-
C.Na+、K+、HCO3-、Cl- D.K+、Na+、AlO2-、NO3-
11、关于电解 NaCl水溶液,下列叙述正确的是
A.电解时在阳极得到氯气,在阴极得到金属钠
B.若在阳极附近的溶液中滴入KI溶液,溶液呈棕色
C.若在阴极附近的溶液巾滴入酚酞试液,溶液呈无色
 D.电解一段时间后,将全部电解液转移列烧杯中,充分搅拌后溶液呈中性
D.电解一段时间后,将全部电解液转移列烧杯中,充分搅拌后溶液呈中性
12、右图是温度和压强对 X +Y![]() 2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中 Z 的体积分数。下列叙述正确的是
2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中 Z 的体积分数。下列叙述正确的是
A.上述可逆反应的正反应为放热反应
B.X、Y 、Z均为气态
C.X 和Y中只有一种为气态, Z 为气态
D.上述反应的逆反应的△H> 0
13、已知充分燃烧ag 乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量 bKJ,则乙炔燃烧的热化学方程式正确的是
A.2C2H2(g)+5O2(g)====4CO2(g)+2H2O(l);△H=-4bKJ/mol
B.C2H2(g)+ O2(g)====2CO2(g)+H2O(l);△H=2bKJ/mol
C.2C2H2(g)+5O2(g)====4CO2(g)+2H2O(l);△H=-2bKJ/mol
D.2C2H2(g)+5O2(g)====4CO2(g)+2H2O(l);△H=bKJ/mol
二、选择题(本题包括 8 小题。每小题给出的四个选项中,有的只有一个选项正确.有的有多个选项正确.全部选对的得6分,选对但不全的得3 分,有选错的得0分)
14、一质量为m的人站在电梯中,电梯加速上升,加速度大小为g,g为重力加速度。
人对电梯底部的压力为
![]()
![]() 15、已知介子和π-介子都是由一个夸克(夸克u或夸克d)和一个反夸克(反夸克 或反夸克 )组成的,它们的带电量如下表所示,表中e为元电荷。
15、已知介子和π-介子都是由一个夸克(夸克u或夸克d)和一个反夸克(反夸克 或反夸克 )组成的,它们的带电量如下表所示,表中e为元电荷。
| π+ | π- | u | d |
|
| |
| 带电量 | +e | - e | +e | -e | -e | +e |
![]()
![]() 下列说法正确的是
下列说法正确的是
![]()
![]() A.π+由u和
组成 B.π+由d和
组成
A.π+由u和
组成 B.π+由d和
组成
C.π-由u和 组成 D.π-由d和 组成
16、把火星和地球绕太阳送行的轨道视为圆周。由火星和地球绕太阳运动的周期之比可求得
A.火星和地球的质量之比 B.火星和太阳的质量之比
C.火星和地球到太阳的距离之比 D.火星和地球绕太阳运行速度大小之比
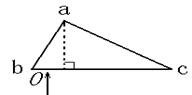 17、图示为一直角棱镜的横截面,∠bac=60°,∠abc=90°。一平行细光束从O点沿垂直于bc面的方向射入棱镜。已知梭镜材料的折射率n=,若不考虑原入射光在bc面上的反射光,则有光线
17、图示为一直角棱镜的横截面,∠bac=60°,∠abc=90°。一平行细光束从O点沿垂直于bc面的方向射入棱镜。已知梭镜材料的折射率n=,若不考虑原入射光在bc面上的反射光,则有光线
A.从 ab面射出
B.从 ac 面射出
C.从bc面射出,且与bc面斜交
D.从bc面射出,且与bc面垂直
 18、一列沿 x 轴正方向传播的简谐横波,周期为0.50s。某一时刻,离开平衡位置的位移都相等的各质元依次为P1,P2,P3,……。已知P1和P2之间的距离为20cm,P2和P3之间的距离为80cm。则P1的振动传到P2所需的时间为
18、一列沿 x 轴正方向传播的简谐横波,周期为0.50s。某一时刻,离开平衡位置的位移都相等的各质元依次为P1,P2,P3,……。已知P1和P2之间的距离为20cm,P2和P3之间的距离为80cm。则P1的振动传到P2所需的时间为
A.0.50s B.0.13s C.0.10s D.0.20s
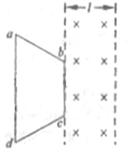
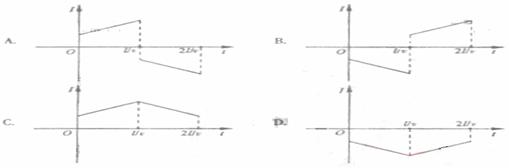 19、图中两条平行虚线之向存在匀强磁场,虚线间的距离为l,磁场方向垂直纸面向里。abcd是位于纸面内的梯形线圈,ad与bc间的距离也为l。t=0时刻,bc边与磁场区域边界重合(如图)。现令线圈以恒定的速度υ沿垂直于磁场区域边界的方向穿过磁场区城。取沿a→b→c→d→a的感应电流为正.则在线圈穿越磁场区域的过程中,感应电流I随时t变化的图线可能是
19、图中两条平行虚线之向存在匀强磁场,虚线间的距离为l,磁场方向垂直纸面向里。abcd是位于纸面内的梯形线圈,ad与bc间的距离也为l。t=0时刻,bc边与磁场区域边界重合(如图)。现令线圈以恒定的速度υ沿垂直于磁场区域边界的方向穿过磁场区城。取沿a→b→c→d→a的感应电流为正.则在线圈穿越磁场区域的过程中,感应电流I随时t变化的图线可能是
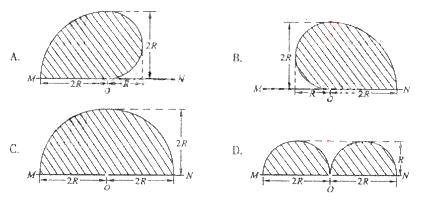
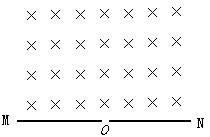 20、如图,在一水平放置的平板MN的上方有匀强磁场,磁感应强度的大小为B,磁场方向垂直纸面向里。许多质量为m带电量为+q的粒子,以相同的速率v沿位于纸面内的各个方向,由小孔O射人磁场区域,不计重力,不计粒子间的相互影响。下列图中阴影部分表示带电粒子可能经过的区城,其中R=。哪个图是正确的?
20、如图,在一水平放置的平板MN的上方有匀强磁场,磁感应强度的大小为B,磁场方向垂直纸面向里。许多质量为m带电量为+q的粒子,以相同的速率v沿位于纸面内的各个方向,由小孔O射人磁场区域,不计重力,不计粒子间的相互影响。下列图中阴影部分表示带电粒子可能经过的区城,其中R=。哪个图是正确的?
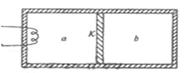
21、如图所示.绝热隔板 K 把绝热的气缸分隔成体积相等的两部分,K与气缸璧的接触是光滑的。两部分中分别盛有相同质量、相同温度的同种气休a和 b 。气体分子之间相互作用势能可忽略。现通过电热丝对气体a加热一段时间后a、b各自达到新的平衡,
 A.a的体积增大了,压强变小了
A.a的体积增大了,压强变小了
B.b 的温度升高了
C.加热后a的分子热运动比 b的分子热运动更激烈
D.a增加的内能大于b增加的内能
第 Ⅱ卷(非选择题 共174分)
22 、 ( 17 分)
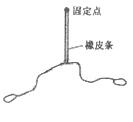 (l)在“验证力的平行四边形定则”实验中.需要将橡皮条的一端固定在水平木板上,另一端系上两根细,细绳的另一端都有绳套(如图)。 实验中需用两个弹簧秤勾住绳套,并互成角度地拉橡皮条。某同学认为在此过程中必须注意以下几项:
(l)在“验证力的平行四边形定则”实验中.需要将橡皮条的一端固定在水平木板上,另一端系上两根细,细绳的另一端都有绳套(如图)。 实验中需用两个弹簧秤勾住绳套,并互成角度地拉橡皮条。某同学认为在此过程中必须注意以下几项:
A.两根细绳必须等长。
B.橡皮条应与两绳夹角的平分线在同一直线上。
C.在使用弹簧秤时要注意使弹簧秤与木板平面平行。其中正确的是________。(填入相应的字母)
(2)测量电源B的电动势E及内阻r(E约为4.5V,r约为1.5Ω)。器材:量程3V的理想电压表V,量程0.5A的电流表A(具有一定内阻),固定电阻R=4Ω,滑线变阻器R’,电键 K ,导线若干。
 ① 画出实验电路原理图。图中各元件需用题目中给出的符号或字母标出。
① 画出实验电路原理图。图中各元件需用题目中给出的符号或字母标出。
② 实验中,当电流表读数为I1时 ,电压表读数为U1;当电流表读数为I2时 ,电压表读数为U2。则可以求出E=___________,r=_______________。用(I1、I2、U1、U2及R表示)
…
23、(16 分)
原地起跳时,先屈腿下蹲,然后突然蹬地。从开始蹬地到离地是加速过程(视为匀加速),加速过程中重心上升的距离称为“加速距离”。离地后重心继续上升,在此过程中重心上升的最大距离称为“竖直高度”。
现有下列数据:人原地上跳的‘加速距离”d1=0.50m., h1=1.0m ;跳骚原地上跳的“加速距离”d2=0.00080m.,“竖直高度”h2=0.10m 。假想人具有与跳骚相等的起跳加速度,而“加速距离”仍为0.50m,则人上跳的“竖直高度”是多少?
 24、(19
分)
24、(19
分)
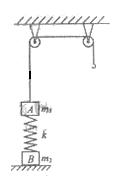
如图.质量为m1的物体 A 经一轻质弹簧与下方地面上的质量为m2的物体B相连,弹簧的劲度系数为k, A 、B都处于静止状态。一条不伸长的轻绳绕过轻滑轮,一端连物体A,另一端连一轻挂钩。开始时各段绳都处于伸直状态。A上方的一段绳沿竖直方向。现在挂钩上挂一质量为m3的物体C并从静止状态释放,已知它恰好能使B离开地面但不继续上升。若将C换成另-个质量为(m1+m3)的物体 D,仍从上述初始位置由静止状态释放,则这次B 离地时D的速度大小是多少?已知重力加速度为g。
25 、(20 分)
图1中B为电源,电动势E=27V,内阻不计。固定电阻R1=500Ω,R2为光敏电阻。C为平行板电容器,虚线到两极板距离相等,极板长,两极板的间距d=1.0×10-2m。S为屏,与极板垂直,到极板的距离l2=0.16m。 P 为一圆盘,由形状相同、透光率不同的三个扇形a、b和c构成,它可绕从AA’轴转动。当细光束通过扇形a、b、c照射光敏电阻R2时,R2的阻值分别为1000Ω、2000Ω、4500Ω。有一细电子束沿图中虚线以速度V0=8.0 ×106m/s连续不断地射人C。已知电子电量e=1.6×10-19C,电子质量m=9×10-31Kg。忽略细光束的宽度、电容器的充电放电时间及电子所受的重力。假设照在R2上的光强发生变化时R2的阻值立即有相应的改变。
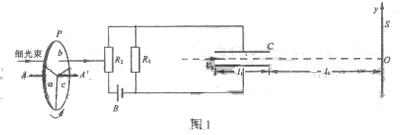
 (1)设圆盘不转动,细光束通过b照射到R2上,求电子到达屏S上时,它离O点的距离y。(计算保留两位有效数字)
(1)设圆盘不转动,细光束通过b照射到R2上,求电子到达屏S上时,它离O点的距离y。(计算保留两位有效数字)
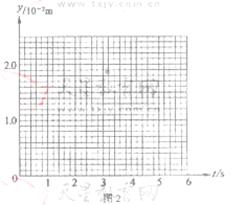
(2)设转盘按图1中箭头方向匀速转动.每3 秒转一圈。取光束照在a、b分界处时t=0,试在图2给出的坐标纸上,画出电子到达屏S上时,它离O点的距离 y 随时间t的变化图线(0~6 s间)。要求在y轴上标出图线最高点与最低点的值。(不要求写出计算过程,只按画出的图线评分。)
26、(15分)
已知A 、B 、C 、D 为气休, E、F为固体,G是氯化钙,它们之间转换关系如下图所示:
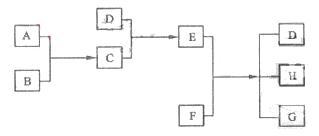
(1)D的化学式(分子式)是___________,E的化学式(分子式)是_____________。
(2)A 和B反应生成C的化学方程式是__________________________
(3)E 和F反应生成D、H、G的化学方程式是__________________________________
27、(15分)
甲、乙、丙、丁为前三周期元素形成的微粒,它们的电子总数相等。已知甲、乙、丙为双原子分子或负二价双原子阴离子,丁为原子。
(1)丙与钙离子组成的离子化合物跟水反应产生一种可燃性气体,反应的化学方程式是_______________________________。
(2)乙在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途:____________________________________
(3)在一定条件下,甲与O2反应的化学方程式是___________________________
(4)丁的元素符号是________,它的原子结构示意图为_____________
(5)丁的氧化物的晶体结构与_______________的晶体结构相似。
28、(15 分)
己知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。
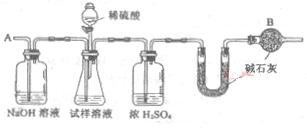
主要实验步骤如下:
① 按图组装仪器,并检查装置的气密性
② 将 ag 试样放人锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③ 称量盛有碱石灰的U型管的质量,得到bg
④ 从分液漏斗滴人6mol/L的硫酸.直到不再产生气体时为止
⑤ 从导管A处缓缓鼓人一定量的空气
⑥ 再次称量盛有碱石灰的U型管的质量,得到cg
⑦ 重复步骤⑤ 和 ⑥ 的操作,直到U型管的质量基本不变,为dg
请填空和回答问题:
(l)在用托盘天平称量样品时,如果天平的指针向左偏转,说明________________
(2)装置中干燥管B的作用是________________________________
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果_____(填偏高、偏低或不变)
(4)步骤⑤的目的是____________(5)步骤⑦的目的是____________
(6)该试样中纯碱的质量分数的计算式为__________________________
(7)还可以用其它方法测定试样中纯碱的质量分数。请简述一种不同的实验方法。
29 、(15 分)
苏丹红一号(sudan I )是一种偶氮染料,不能作为食品添加剂使用的。它是由苯胺和 2 –萘酚为主要原料制备的,它们的结构简式如下所示:
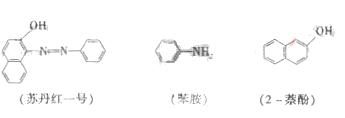
(1)苏丹红一号的化学式(分子式)为__________________
(2)在下面化合物(A)~(D)中,与2 –萘酚互为同分异构体的有(填字母代号)_________
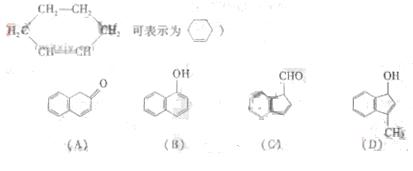
(3)上述化合物(C)含有的官能团是________________________________
(4)在适当的条件下,2 –萘酚经反应可得到芳香化合物E(C8H6O4), 1molE 与适量的碳酸氢钠溶液反应可放出二氧化碳44.8L(标准状况),E与溴在有催化剂存在时反应只能生成两种一溴取代物,两种一溴取代物的结构简式分别是___________________________,E与碳酸氢钠反应的化学方程式是________________________________________________
(5)若将E与足量乙醇在浓硫酸作用下加热,可以生成一个化学式(分子式)为C12H14O4的新化合物,该反应的化学方程式是__________________________反应类型是_____。
30 、 ( 21 分)
为了验证胰岛素具有降低血糖的作用,以小鼠活动状况为观察指标设计实脸。某同学的实验方案如下:
①将正常小鼠随机分成A、B两组,现察并记录其活动状况。
②A组小鼠注射适量胰岛素溶液,B组注射等量生理盐水。一段时间后,A组小鼠会出现四肢无力,活动减少,甚至昏迷等低血糖症状,B组活动状况无变化。
③A组小鼠出现低血糖症状后.分别给A、B 两组小鼠注射等量葡萄糖溶液。一段时间后, A组小鼠低血糖症状缓解,B组活动状况无变化。
该实验方案可以说明胰岛素具有降低血糖的作用。
请回答:
(1)该实验原理是:___________________________________
(2)分析小鼠注射胰岛素溶液后出现低血糖症状的原因:____________________________
(3)胰岛素在血糖平衡调节中的作用是:________________________________________
31、(21分)
已知牛的有角和无角为一对相对性状,由常染色体上的等位基因A与a控制。在自由放养多年的一群牛中(无角的基因频率与有角的基因频率相等),随机选出 1 头无角公牛和6头有角母牛,分别交配,每头母牛只产了 l 头小牛。在 6 头小牛中,3 头有角,3 头无角。
(1)根据上述结果能否确定这对相对性状中的显性性状?请简要说明推断过程。
(2)为了确定有角和无角这对相对性状的显隐性关系,用上述自由放养的牛群(假设无突变发生)为实验材料,再进行新的杂交实验,应该怎样进行?(简要写出杂交组合、预期结果并得出结论)
