天津市十二所重点中学理科综合联合测试
试卷
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,满分300分,考试时间150分钟。
第Ⅰ卷(选择题共22题,每题6分,共132分)
原子量:H 1 C 12 N 14 O 16 Na 23 Fe 56
一、选择题
1、对下列有关实例形成原理的解释,正确的是
A、克隆羊的获得利用了杂交育种的原理
B、培养青霉菌高产菌株利用的是基因突变的原理
C、利用高浓度盐水腌制咸肉能存放很长时间利用了高浓度盐水影响酶活性的原理
D、结扎女性输卵管可以避孕的原理是抑制了女子排卵和雌性激素的分泌
2、光照下的正常生长的某绿色植物,其它条件不变,突然停止光照。请判断短时间内叶绿体中C3合成速率(横坐标为时间,纵坐标为速率)
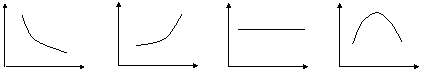 |
A B C D
3、随着转基因技术的发展,“基因污染”应运而生,关于基因污染的下列说法不正确的是
A、转基因作物可通过花粉扩散到它的近亲作物上,从而污染生物基因库。
B、杂草、害虫从它的近亲获得抗性基因,可能破坏生态系统的稳定性。
C、基因污染是一种不可以增殖的污染。
D、基因污染难以清除。
4、两只杂合黑豚鼠交配,后代出现白豚鼠的原因最可能是什么?杂合黑豚鼠一胎生出4只豚鼠,则出现3黑1白的可能性为
A、受精作用时,非等位基因的自由组合,27/64
B、减数分裂时,等位基因的分离,27/64
C、受精作用时,非等位基因的自由组合,27/256
D、减数分裂时,等位基因的分离,27/256
5、某生物兴趣小组的同学用小鼠作材料进行实验,切除了某器官后,小鼠表现为饮水量增加,且喜欢饮淡盐水。注射某种物质后,恢复到正常状态。切除的器官和注射的物质分别是
A、甲状腺 甲状腺激素 B、垂体 抗利尿激素
C、下丘脑 抗利尿激素 D、肾上腺 醛固酮
6、下表列出了生态群落①、②、③、④含有的物种及每个物种的种群密度(个体数/m2)
| 群落 | 种1 | 种2 | 种3 | 种4 | 种5 | 种6 | 种7 | 种8 |
| ① | 92 | 4 | 0 | 0 | 1 | 1 | 1 | 1 |
| ② | 0 | 25 | 20 | 20 | 20 | 5 | 0 | 0 |
| ③ | 0 | 2 | 3 | 5 | 40 | 50 | 0 | 0 |
| ④ | 0 | 65 | 20 | 10 | 3 | 2 | 0 | 0 |
当受到大规模虫害袭击,并且危害程度逐步增加时,这些群落中受影响最小的是 ;最大的是 。
A.①、② B.③、④ C.③、① D.②、①
7、某同学用青菜的幼苗进行了四项实验,如下图所示。下列说法不正确的是:
 | |||||||||
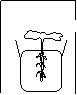 | |||||||||
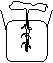 | |||||||||
 | |||||||||
![]()
(1) (2) (3) (4)
A、实验②、③对照可以证明植物生长具有向光性
B、实验③进行一段时间后,青菜叶片发黄的原因是无光条件叶绿素不能合成。
C、实验④的生长结果只能证明根具有向地性
D、实验①的目的是起对照作用
8、图中横坐标A、B、C、D表示某种哺乳动物(2n)在有性生殖过程中某些时期的细胞。图中a、b、c表示各种结构或物质在不同时期的连续数量变化,请问:四分体时期可能发生在
 |
a b a b c a b c a b
A B C D
9、据最新消息,我国今年将实现“神州号”宇宙飞船载人飞行。发射飞船的运载火箭,其推进剂引燃后发生剧烈反应,产生大量高温气体从火箭尾部喷出。引燃后的高温气体主要是CO2、H2O、N2、NO,这些气体均为无色,但在卫星发射现场看到火箭喷射出大量红烟,产生红烟的原因是
A、高温下N2遇空气生成NO2 B、NO遇空气生成NO2
C、CO2与NO反应生成NO2 D、NO与H2O反应生成NO2
10、下图表示一个化学反应过程,图中的黑球表示两个相同的单糖或其单元。则图中的a、b、c分别表示
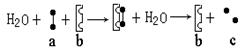
A、麦芽糖 麦芽糖酶 葡萄糖 B、蔗糖 蔗糖酶 果糖
C、乳糖 乳糖酶 葡萄糖 D、淀粉 淀粉酶 葡萄糖
11、有两种短周期元素X和Y,可组成化合物XY3 ,若X原子序数为a,Y原子序数为b,则a + b不可能的是
A、 a + b=16 B、 a + b=30
C、 a + b=24 D、 a + b=43
12、下列离子方程式书写正确的是
A、等物质的量浓度的FeI2溶液与溴水等体积混合
2Fe2+ + 2I- + 2Br2=2Fe3+ + I2 + 4Br-
B、用氨水吸收少量的SO2 2NH3·H2O +
SO2=2NH4+ + SO![]() + H2O
+ H2O
C、铜与浓硝酸反应 Cu + 2H+ + 2NO![]() =Cu2+ + 2NO2↑+ H2O
=Cu2+ + 2NO2↑+ H2O
D、NaHSO4溶液与过量的Ba(OH)2反应 H+ + OH-=H2O
13、据报道,摩托罗拉公司开发的一种以甲醇为原料、以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月。关于该电池的叙述正确的是
A、放电时,正极反应为:O2 + 4e- + 4H+ = 2H2O
B、放电时,负极反应为:CH3OH-6e-+8OH- = CO32-+6H2O
C、充电时,原电池的负极与电源的正极连接
D、充电时,阴极反应为:4OH- - 4e- = 2H2O + O2↑
14、在一固定容积的密闭容器中,加入2 L X(g)和3 L Y(g),发生如下反应:nX(g)+3Y(g) D 2R(g);△H= -QKJ/mol,平衡后,测得X和Y的转化率分别为a%和b%,已知a<b,则n值为
A、1 B、2 C、3 D、4
15、下列操作方法和所得结论都正确的是
A、向待测溶液中加入硝酸酸化的BaCl2溶液生成白色沉淀,则待测液中一定含有SO42-离子
B、向淀粉溶液中加入稀硫酸,加热几分钟,再用NaOH溶液中和至碱性,滴加碘水溶液不变蓝,则说明淀粉全部水解了
C、向某待测液中滴加BaCl2溶液生成白色沉淀,加盐酸沉淀溶解并产生无色无味气体则待测液中一定含有CO32-离子
D、向某卤代烃中加入NaOH溶液,小火加热几分钟后用盐酸中和至酸性,滴加AgNO3溶液生成白色沉淀,则该卤代烃中含有氯原子
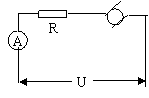 16、 如图所示,电路电阻为R,当电压为U时,安培表读数为I,此时电动机不转动,若电压增大为U’,安培表读数为I’,此时电动机正常工作,安培表为理想表,则
16、 如图所示,电路电阻为R,当电压为U时,安培表读数为I,此时电动机不转动,若电压增大为U’,安培表读数为I’,此时电动机正常工作,安培表为理想表,则
①电动机的内电阻为U’/ I’-R
②电动机的输出功率为(I’-I)(U’-I’R)
③电动机的输出功率为I’(U’-I’U/I)
④以上说法都不对
A.①② B.③ C.①③ D. ④
17、地球的大气中,基本不变的成分为氧、氮、氩等,占大气总量的99.9%.可变气体成分主要有二氧化碳(CO2)、水气和臭氧等,这些气体的含量很少,但对大气物理状况影响却很大.据研究:人类大量燃烧矿物燃料放出大量CO2,使大气中的CO2浓度不断增大,是导致“温室效应”的主要原因.即:大气的平均温度上升,从而导致一系列生态环境问题.由此可判断:CO2比大气中的氧、氮、氩等基本不变的气体成分
A、对可见光的吸收作用强 B、对无线电波的吸收作用强
C、对紫外线的吸收作用强 D、 对红外线的吸收作用强
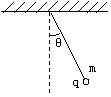 18、如图所示在匀强电场中,用一绝缘丝线系一带电小球
18、如图所示在匀强电场中,用一绝缘丝线系一带电小球
(质量为m,电量为q), 为保证丝线与竖直方向夹角
θ=600,则匀强电场的电场强度大小可能为
①mgtan600/q ②mgcos600/q
③mgsin600/q ④mg/q
A、①② B、③④
C、①③ D、①③④
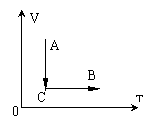 19、一定质量的理想气体自状态A经状态C变化到状态B。这一过程在V-T图上表示如图所示,则
19、一定质量的理想气体自状态A经状态C变化到状态B。这一过程在V-T图上表示如图所示,则
①在过程AC中,外界对气体做功
②在过程CB中,外界对气体做功
③在过程AC中,气体压强不断变大
④在过程CB中,气体压强不断变大
A.①③ B.②④ C.①④ D.①③④
20、地球同步卫星离地心的距离为r,运行速度为v1,加速度为a1,地球赤道上的物体随地球自转的向心加速度为a2,第一宇宙速度为v2,地球半径为R,则下列比例关系正确的是
A、 a1 /a2=r/R , v1/ v2=r/R B、 a1 /a2= r/R , v1/ v2=(R/r)1/2
C、 a1 /a2=(R/r) 2 , v1/ v2=r/R D、 a1 /a2=(R/r) 2 , v1/ v2=(R/r)1/2

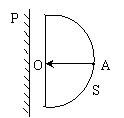 21、如图所示,将半圆形玻璃砖放在竖直面内,它左方有
21、如图所示,将半圆形玻璃砖放在竖直面内,它左方有
较大的光屏P,线光源S可沿玻璃砖圆弧移动,它发出
的光束总是射向圆心O,若S从图中A向B处移动,
在P上先看到七色光带,以后各色光陆续消失,则此七
色光带从下到上的排列顺序以及最早消失的光是
A、 光→紫光,红光
B、紫光→红光,红光
C、红光→紫光,紫光
D、紫光→红光,紫光
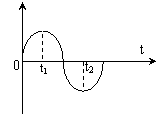
|
①电容器的带电量为零
②线圈中的磁场能达到最小
③线圈中的电场能达到最小
④线圈两端的电压为零
A、 ② B、①③ C、①③④ D、①②④
2003年天津市十二区县市重点中学联合测试
理科综合试卷
第II卷(非选择题 共10题 共168分)
| 题 号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 得 分 |
| 答 案 | |||||||||
| 题 号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 得 分 | |
| 答 案 | |||||||||
| 题 号 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 得 分 | |
| 答 案 |
| 题号 | Ⅰ卷 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 | 31 | 32 | II卷 | 总分 | ||
| 得分 | 生物 |
| |||||||||||||
| 化学 |
| ||||||||||||||
| 物理 |
| ||||||||||||||
以下数据可供解题时参考:原子量:H 1 C 12 N 14 O 16 Na 23 Fe 56
二、简答题
23、(共13分)将一段黑藻放在水中,给予人工光照,在不断改变灯与烧杯的距离下进行测定。记录藻枝放出的气泡数,结果如下表。
| 灯与烧杯之间的距离(cm) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 气泡数(个/分钟) | 16 | 13 | 8 | 6 | 5 | 4 | 3 | 2 | 1 | 0 |
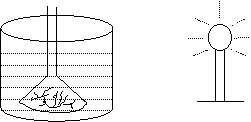
(1)划坐标图表示实验结果。
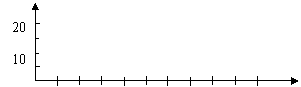 气泡数
气泡数
距离
10 20 30 40 50 60 70 80 90 100
(2)从图表中你能得出什么结论?
_____________________________________________________________。
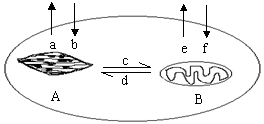
(3)上图是某植物细胞的示意图,请据图分析该植物的代谢类型属于
。
用示踪法以C18O2作原料进行光合作用。在较强光照下,测得含18O的呼吸
作用产物的主要去向是图中的 ______ 途径(用小写字母表示)。
(4)新的观点认为“清晨不宜在树林中进行早锻炼”,请据图说明其中的科
学道理 ___________________________________ _________
_____________ _______________________________________。
24、(12分)材料一:美国自“9•11”恐怖事件后,在华盛顿、新泽西和佛罗里达等地相继发生“炭疽事件”,使有些人感染了炭疽杆菌并患炭疽热病。
材料二:一位科学家在显微镜下观察到,载玻片上每单位面积平均有50个炭疽杆菌,把此载玻片放在液体培养液中培养4小时后将其稀释10倍,再放到相同条件的显微镜下观察,发现每单位面积平均有80个炭疽杆菌。
材料三:大多数种类的炭疽热杆菌对青霉素非常敏感,但若长期使用青霉素治疗,效果会越来越差。因此,医生建议:在预防和治疗炭疽热时应在使用青霉素的同时,配合使用环丙沙星和强力霉素等抗生素。
请阅读上述材料,回答下列问题:
(1)炭疽杆菌与酵母菌相比,在细胞结构上的最主要特点是
_______________ _________。
(2)炭疽杆菌增殖的方式为__________________,炭疽杆菌每分裂一次的平均
时间为_____________。
(3)在治疗炭疽热病的过程中,使用青霉素的同时,还要配合强力霉素和环丙
沙星等多种抗生素的使用,其主要原因是
____________________________________________。
25、(6分)现用体重等方面大体相同的三组兔子进行实验。将含有放射性碘的注射液注射到A、B、C三组兔子的体内,然后,定时测定兔子甲状腺的放射量,实验结果如图所示。4d后,向A组兔子注射无放射性的甲状腺激素,向B组兔子注射无放射性的促甲状腺激素,向C组兔子注射生理盐水。请据图回答:
(1)
![]()
![]()
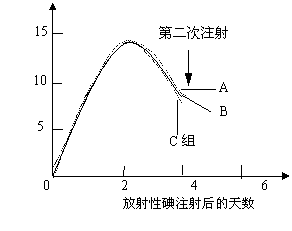 开始的4天内,三组兔子体内甲状腺放射量升降的原因是
开始的4天内,三组兔子体内甲状腺放射量升降的原因是
_____________________________________________________________________________________________________________________________________________。
(2)第二次注射后,三组兔子甲状腺放射量下降的速率从快到慢依次为____________ _________。
26、(共16分)
Ⅰ(8分):下面所示装置(酒精灯、铁架台等未画出)制取三氯化磷,在仪器d(瓶塞用金属簿包裹)放入足量白磷,将氯气迅速而又不间断地通入仪器d中,氯气与白磷就会发生反应,产生火焰。三氯化磷和五氯化磷的物理常数如下表所示:
| 熔点 | 沸点 | |
| 三氯化磷 | -112℃ | 76℃ |
| 五氯化磷 | 148℃ | 200℃(分解) |
| 熔点 | 沸点 | |
| 三氯化磷 | -112℃ | 76℃ |
| 五氯化磷 | 148℃ | 200℃(分解) |
⑴有浓盐酸、浓硫酸、白磷、二氧化锰、氢氧化钠等物质供选用,a、b中应
该装入的试剂分别是a_____________、b______________。
 |
⑵需要加热的仪器有___________ (填字母)。
⑶生成的三氯化磷在蒸馏烧瓶e中收集,为保证三氯化磷蒸汽冷凝,应在水
槽g中加入________________。
⑷三氯化磷遇水蒸气强烈反应,甚至爆炸。所以d、e仪器以及装入的物质都
不能含有水分。为除去氯气中的水分,C可以装入下列物质中的___________(填字母)。
A、碱石灰 B、浓硫酸 C、无水氯化钙
⑸氯气和白磷反应放出大量的热,为使仪器d不致因局部过热而炸裂,实验开始前应在曲颈瓶的底部放少量________________。
⑹实验室的白磷保存在水中,取出白磷后用滤纸吸干表面的水分,浸入无水酒精中片刻再浸入乙醚中片刻即可完全除去水分。已知水与酒精互溶,酒精与乙醚互溶。用上述方法完全除去水分的原理是_________________。
⑺为防止氯气污染空气,装置末端导出的气体最好用(填字母)________进行净化处理。
A、NaOH溶液 B、Ca(OH)2溶液 C、饱和食盐水
![]()
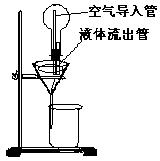
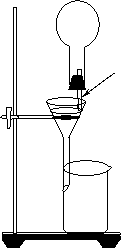 Ⅱ(8分):某学生为了使过滤操作能自动添加
Ⅱ(8分):某学生为了使过滤操作能自动添加
液体,设计了“自动加液过滤器”,如右图所示。
倒置的烧瓶中盛放待过滤的液体,液体从“液
体流出管”流入漏斗。为使液体顺利流下,需
插入“空气导入管”与大气相通。
(1)“空气导入管”下口应在______
A、滤纸边沿下方 B 、滤纸边沿上方
C、以上情况均可。
(2)在图中画出“空气导入管”的简单示意。
(3)试简要说明自动加液过滤的原因是
_______________________________________________________________
_______________________________________________________________。
27、(共30分。第Ⅰ题14分,第Ⅱ题10分,第Ⅲ题6分)
Ⅰ、(14分)下图中A~L分别表示反应中的一种常见物质,E、F在通常状况下是气体单质,其中E为刺激性气味的气体,X、Y是常见的固态单质,参加反应的水及生成的水在图中已略去。 B溶液的焰色反应为紫色。填写下列空白:
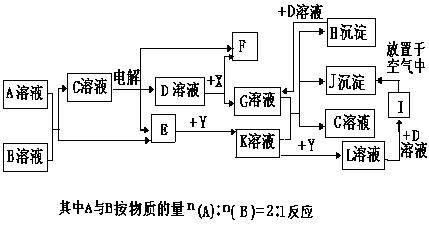
(1)E是(填名称,下同)___________J是 _____________
(2)写出下列反应的离子方程式:
K+Y"L ______________________________
A+B " C +E ______________________________
H+D"G _______________________________
C "F+D+E ______________________________
Ⅱ、(10分)2001年诺贝尔化学奖被美国的诺尔斯、沙普雷斯和日本的野依良治获得,以表彰他们发现某些被称为手性的分子可以用来加速并控制化学反应的创造性工作。在有机物分子中,若某碳原子连接四个不同的原子或基团,则这种碳原子称为“手性碳原子”。例如:
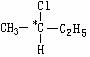
中*C就是手性碳原子。含“手性碳原子”的物质通常
具有不同的光学特征(称为光学活性)。
![]()
(1)据报道最新合成的有机物A为:
具有光学活性,若要使A失去光学活性,可将A与浓硫酸共热,使
![]()
![]() 变为 :
变为 :
列出可采用的其他方法(最少列举三种方法)
①_________________________________________;
②_____________________________________________;
③_______________________________________________;
④________________________________________________;
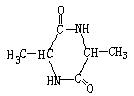
(2)某有机物B的化学式为C3H7NO2, 已知二分子B在一定条件下生成环
B既能与强酸溶液反应,又能与强碱溶 状化合物C,则C的结构简式为
液反应。且B具有光学活性。则B的
结构简式为
__________________________________
_____________________________
若B能在一定条件下生成高分子化合物D,写出B形成D的化学方程式:
_________________________________________。
Ⅲ(6分)淀粉是人类的主要能源物质,淀粉在人体内水解成葡萄糖。葡萄糖释放能量有两种形式,即有氧呼吸和无氧呼吸。
⑴淀粉水解成葡萄糖的化学方程式为:
⑵在有氧呼吸时,每克固态葡萄糖氧化成CO2气体和液态水释放15.56 kJ的热量。请写出葡萄糖氧化的热化学方程式:
28、(8分)现有Na2O2和NaHCO3的混合物两等份,第一份混合物放入密闭容器中加热,使其充分反应;第二份混合物中加入足量的稀H2SO4。两种情况下得到同样的气体,但气体体积不同。前者产生气体的体积为a L,后者产生的气体体积为b L(气体体积都是在通常状况下测得,该条件下,气体的摩尔体积为VL/mol)。
⑴ 第一份混合物加热充分反应后的固体残留物是 ,
其物质的量为 。
⑵ 每份样品中Na2O2的物质的量为 ,
NaHCO3的物质的量为
。
29、(20分)如下列中左图所示,一个子弹水平射入一个原来静止的单摆并留在里
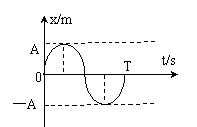
 面,且射入时间甚短,结果单摆的振动图线如下列中右图所示。已知摆球的质量为子弹的5倍,摆球上摆角度小于50,试求子弹射入摆球前的速度是多少?
面,且射入时间甚短,结果单摆的振动图线如下列中右图所示。已知摆球的质量为子弹的5倍,摆球上摆角度小于50,试求子弹射入摆球前的速度是多少?
30、(22分)利用风力发电是一种经济而又清洁的能源利用方式.我国甘肃省某地,四季的平均风速为![]() .已知空气的密度为
.已知空气的密度为![]() ,该地新建的小型风力发电机的风车有三个长度均12米长的叶片,转动时可形成半径为12米的一个圆面.
,该地新建的小型风力发电机的风车有三个长度均12米长的叶片,转动时可形成半径为12米的一个圆面.
(1)若这个风车能将通过此圆面内的10%的气流的动能转化为电能,那么该风车带动的发电机功率为多大?(保留两位有效数字)
(2)为了减少风车转动轴的磨损,根据最新设计,在转动轴与轴承的接触部分,镀了一层纳米陶瓷.一般陶瓷每立方厘米含有![]() 晶粒,而这种纳米陶瓷每立方厘米含有
晶粒,而这种纳米陶瓷每立方厘米含有![]() 个晶粒.若把每个晶粒看做球形,并假设这些晶粒是一个挨着一个紧密排列的,那么每个晶粒的直径大约是多少纳米?
个晶粒.若把每个晶粒看做球形,并假设这些晶粒是一个挨着一个紧密排列的,那么每个晶粒的直径大约是多少纳米?
(3)干旱多风的气候特点,使生态环境破坏严重,大片土地沙漠化,对此现象应采取
的措施是____________________________________________________
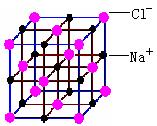 (4)纳米材料的表面微粒占总微粒比例极大,
(4)纳米材料的表面微粒占总微粒比例极大,
这是它有许多特性的原因。假设某氯化钠纳
米颗粒的大小和形状如图。
这种纳米颗粒中所含Cl-___ ___个,
Na+____ ____个,表面微粒数与总微粒数之
比为_____ ___。
31、(20分)如图所示,两根光滑的平行金属导轨与水平面成θ角放置。导轨间距为L,导轨上端接有阻值为R的电阻,导轨的电阻不计。整个导轨处在方向竖直向上、磁感应强度为B的匀强磁场中,把一根质量为m,电阻也为R的金属圆杆垂直于两根导轨放在导轨上,从静止开始释放。求:
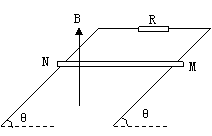 (1)金属圆杆MN运动的最大速度VM的大小。
(1)金属圆杆MN运动的最大速度VM的大小。
(2)金属圆杆MN达到最大速度的1/3时的加速度a的大小。
 32、(21分)1998年6月2日,我国科学家研制的阿尔法磁谱仪由“发现号”航天飞机搭载升空,用于探测宇宙中是否有反物质和暗物质存在,反物质的原子(反原子)是由带负电的反原子核和核外正电子组成,反原子核由反质子和反中子组成.与
32、(21分)1998年6月2日,我国科学家研制的阿尔法磁谱仪由“发现号”航天飞机搭载升空,用于探测宇宙中是否有反物质和暗物质存在,反物质的原子(反原子)是由带负电的反原子核和核外正电子组成,反原子核由反质子和反中子组成.与 ![]() 、
、![]() 、
、![]() 等物质粒子相对应的
等物质粒子相对应的![]() 、
、![]() 、
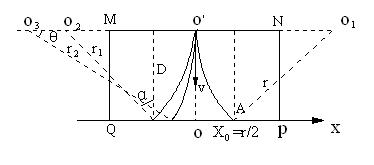
、![]() 等称为反粒子.由于反粒子具有和相应粒子完全相同的质量及相反对应的电荷,故可用下述方法探测,如图所示:设图中各粒子或反粒子均由
等称为反粒子.由于反粒子具有和相应粒子完全相同的质量及相反对应的电荷,故可用下述方法探测,如图所示:设图中各粒子或反粒子均由![]() 处沿垂直于匀强磁场B的方向(
处沿垂直于匀强磁场B的方向(![]() )进入截面为MNPQ的磁谱仪时速度相同(可以认为该速度即为飞船的速度),且已知氢原子核(
)进入截面为MNPQ的磁谱仪时速度相同(可以认为该速度即为飞船的速度),且已知氢原子核(![]() )在磁场中做圆弧运动,在
)在磁场中做圆弧运动,在![]() 轴上的偏转位移
轴上的偏转位移![]() 恰为其轨迹半径r的一半,打在A点.试论证:反氢核(
恰为其轨迹半径r的一半,打在A点.试论证:反氢核(![]() )和反氦核(
)和反氦核(![]() )的轨迹如何?及其在
)的轨迹如何?及其在![]() 轴上的偏转位移
轴上的偏转位移![]() 和
和![]() 各多大?(如果预言正确,那么当人们观察到这样的轨迹,就证明已经探测到了反氢和反氦的核)
各多大?(如果预言正确,那么当人们观察到这样的轨迹,就证明已经探测到了反氢和反氦的核)
命题人:高仰山(杨村一中)刘媛媛(杨柳青一中) 李金秋(宝坻一中) 刘 倩(塘沽一中)
国卫国(汉沽一中)刘桂敏(杨村一中) 齐占波(汉沽一中) 运启喜(宝坻一中) 周连海(蓟县一中)窦云胜(塘沽一中) 肖跃强(静海一中) 赵晶岩(四十七中) 李庆忠(大港一中)
天津市十二所重点中学理科综合联合测试
理科综合 答案及评分标准
一、选择题:每题6分,8小题共132分。
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| B | A | C | D | D | D | C | B | B | A | D |
| 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 |
| B | B | A | C | B | C | D | D | B | C | C |
二、非选择题(共168分):
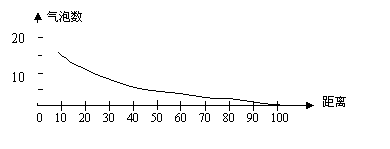 23、(1)(3分)
23、(1)(3分)
(2)(3分)光合作用强度与光照强度有关
(3)(2分)自养需氧型;(2分)d
(4)(3分)夜间植物细胞A处不能进行光合作用,只有B处进行呼吸作用,因此清晨时树林中CO2多O2少,对人体呼吸不利。
24、每空3分,共12分
(1)没有核膜包被的典型细胞核 (2)分裂生殖;1小时
(3)长期使用青霉素,使炭疽杆菌产生抗药性。交替使用不同的抗生素,可大大降低其抗药性。
 25、(1)开始甲状腺能利用碘合成甲状腺激素,所以甲状腺的放射性增高。以后,甲状腺分泌的甲状腺激素逐渐进入血液,所以甲状腺的放射量降低。(3分)
25、(1)开始甲状腺能利用碘合成甲状腺激素,所以甲状腺的放射性增高。以后,甲状腺分泌的甲状腺激素逐渐进入血液,所以甲状腺的放射量降低。(3分)
(2)B > C > A(3分)
26、Ⅰ(每空1分,共8分)
(1)浓盐酸,二氧化锰 ⑵b ⑶冰水
⑷C ⑸细沙 ⑹相似相溶原理 ⑺A
Ⅱ (共8分)(1)A (2分) (2)见图(2分)
(3)过滤的液体沿“液体流出管”流入漏斗,当
漏斗里的液面封住 “空气导入管”的管口时,空气停止进入烧瓶,液体停止流入漏斗;随着过滤的进行,漏斗里液面下降,当降到“空气导入管”的下管口以下时,空气又进入烧瓶,液体又流入漏斗,这样循环往复,便完成了自动加液过滤操作。(4分)
27、Ⅰ(14分)(1)Cl2 Fe(OH)3 (各1分)
(2)2 Fe3++Fe==3Fe3+ ClO-+Cl-+2H+==Cl2 +H2O
![]() Al(OH)3+OH-==AlO-+2H2O
Al(OH)3+OH-==AlO-+2H2O
2Cl-+2H2O H2↑+2OH-+Cl2↑(各3分)
Ⅱ(共10 分)
(1)(只要写对3种方法既给3分)
①将A 与H2加成,使—CHO变为—CH2OH
②将A氧化,使—CH2OH变为—CHO
![]()
③将A与CH3COOH酯化,使 —CH2OH变为
![]()
④将A水解,使 变为HO—CH2—
(2)
![]()
(每空2分)
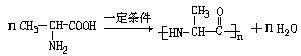
(3分)
Ⅲ.(每空3分,共6分)
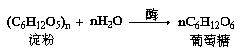
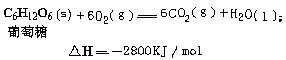
![]()
![]()
28、(1) Na2CO3 ; mol (2) mol ;
![]() mol
mol
(每空2分,共8分)
29.碰撞中满足动量守恒定律:mV0=(m+M)V ——4分
由于单摆运动的上摆角度а小于50,故sinа=A/L ——4分
![]() 由单摆周期公式:T=2π√L/g
——4分
由单摆周期公式:T=2π√L/g
——4分
上摆过程中,机械能守恒,有
(m+M)L(1-cosа)=(m+M)V2/2 ——4分
由题意知:M=4m
![]()
联立方程组得:V0=6√2 g(L-√L2-A2) ——4分
(1) 植树造林、退耕还林还草、控制载畜量、划区轮牧等(答对即可)(2分)
(4)Cl-
14 ;Na+ 13;![]() (每空2分,共6分)
(每空2分,共6分)
30. ⑴P=ηmv2/2 ——3分
而每秒通过该圆面的空气质量为m=ρπr2v ——3分
所以P=ηρπr2v3/2=2.9×104w ——2分
⑵设每个晶粒的直径为d,则V=1019πd3/6=10-6 ——4分
得: d=6×10-9m=6nm ——2分
31. ⑴平衡时,mgsinθ=ILBcosθ ——3分
ε=BLVMcosθ ——3分
I=ε/2 R=BLVMcosθ/2 R ——3分
故:VM=2mgRsinθ/B2L2cos2θ ——2分
⑵ mgsinθ-ILBcosθ=ma ——3分
I=BL(VM/3)cosθ/2 R ——4分
故:a=2gsinθ/3 ——2分
32. 因反氢核和反氦核带负电,故均向左偏,其半径分别为r1和r2,轨迹
如题图所示。 ——4分
设氢核的质量为m,电量为q,由qvB=mv2/r ,则半径r=mv/qB ——3分
由于反氢核的质量也为m,电量也为-q,故轨道半径r1=r ——2分
但偏转方向相反,即x1= -x0 =-r/2 ——2分
由于反氦核的质量为4m,电量为-2q,故轨道半径r2 = 4mv/2 qB = 2r——2分
对图中角α,有sinα=(r-r/2)/r=1/2,则α=π/6 ——2分
磁场宽度D=rcosα=![]() · r/2
——2分
· r/2
——2分
设反氦核偏转角度为θ,则sinθ= D/2r = ![]() /4
/4
故![]() = —(2 r – 2 r cosθ)= —(2 --
= —(2 r – 2 r cosθ)= —(2 --![]() )r ————4分
)r ————4分
命题人:高仰山(杨村一中)
刘媛媛(杨柳青一中) 李金秋(宝坻一中) 刘 倩(塘沽一中) 国卫国(汉沽一中)
刘桂敏(杨村一中) 齐占波(汉沽一中) 运启喜(宝坻一中) 周连海(蓟县一中)
窦云胜(塘沽一中) 肖跃强(静海一中) 赵晶岩(四十七中) 李庆忠(大港一中)
2003年天津市十二所重点中学联合测试
理科综合(生物) 答案及评分标准
二、选择题:每题6分,8小题共48分。
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| B | A | C | D | D | D | C | B |
二、非选择题:
 23、(1)(3分)
23、(1)(3分)
(2)(3分)光合作用强度与光照强度有关
(3)(2分)自养需氧型;(2分)d
(4)(3分)夜间植物细胞A处不能进行光合作用,只有B处进行呼吸作用,因此清晨时树林中CO2多O2少,对人体呼吸不利。
24、每空3分,共12分
(1)没有核膜包被的典型细胞核 (2)分裂生殖;1小时
(3)长期使用青霉素,使炭疽杆菌产生抗药性。交替使用不同的抗生素,可大大降低其抗药性。
25、(1)开始甲状腺能利用碘合成甲状腺激素,所以甲状腺的放射性增高。以后,甲状腺分泌的甲状腺激素逐渐进入血液,所以甲状腺的放射量降低。(3分)
(2)B > C > A(3分)
30.(3)植树造林、退耕还林还草、控制载畜量、划区轮牧等(答对即可)
(2分)
组题人:刘媛媛(杨柳青一中) 李金秋(宝坻一中) 刘 倩(塘沽一中) 国卫国(汉沽一中)
2003年天津市十二所重点中学联合测试
理科综合(化学) 答案及评分标准
一、择题:每题6分,7小题共42分。
| 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| B | A | D | B | B | A | C |
 二、非选择题:(共60分)
二、非选择题:(共60分)
26、(16分)Ⅰ(每空1分,共8分)
(1)浓盐酸,二氧化锰 ⑵b ⑶冰水
⑷C ⑸细沙 ⑹相似相溶原理 ⑺A
Ⅱ (共8分)(1)A (2分) (2)见图(2分)
(3)过滤的液体沿“液体流出管”流入漏斗,当漏斗里的液面封住 “空气导入管”的管口时,空气停止进入烧瓶,液体停止流入漏斗;随着过滤的进行,漏斗里液面下降,当降到“空气导入管”的下管口以下时,空气又进入烧瓶,液体又流入漏斗,这样循环往复,便完成了自动加液过滤操作。(4分)
27、Ⅰ(14分)(1)Cl2 Fe(OH)3 (各1分)
(2)2 Fe3++Fe==3Fe3+ ClO-+Cl-+2H+==Cl2 +H2O
![]() Al(OH)3+OH-==AlO-+2H2O
Al(OH)3+OH-==AlO-+2H2O
2Cl-+2H2O H2↑+2OH-+Cl2↑(各3分)
Ⅱ(共10 分)
(1)(只要写对3种方法既给3分)
①将A 与H2加成,使—CHO变为—CH2OH
②将A氧化,使—CH2OH变为—CHO
![]()
③将A与CH3COOH酯化,使—CH2OH变为
![]()
④将A水解,使 变为HO—CH2—
 (2)
(2)
![]()
(每空2分)
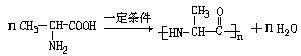
(3分)
Ⅲ.(空3分,共6分)
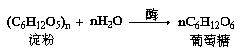
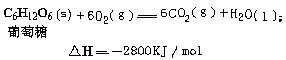
![]()
![]() 28、(1) Na2CO3
;
mol (2) mol ;
28、(1) Na2CO3
;
mol (2) mol ;
![]() mol
mol
(每空2分,共8分)
30. (4)Cl- 14 ; Na+ 13; ![]() (每空2分,共6分)
(每空2分,共6分)
组题人:刘桂敏(杨村一中) 齐占波(汉沽一中) 运启喜(宝坻一中) 周连海(蓟县一中)
2003年天津市十二所重点中学联合测试 理科综合(物理) 答案及评分标准
一、选择题:每题6分,7小题共42分。
| 16 | 17 | 18 | 19 | 20 | 21 | 22 |
| B | C | D | D | B | C | C |
二、非选择题:(共75分)
29.碰撞中满足动量守恒定律:mV0=(m+M)V ——4分
由于单摆运动的上摆角度а小于50,故sinа=A/L ——4分
![]()
由单摆周期公式:T=2π√L/g ——4分
上摆过程中,机械能守恒,有
(m+M)L(1-cosа)=(m+M)V2/2 ——4分
由题意知:M=4m
![]()
联立方程组得:V0=6√2 g(L-√L2-A2) ——4分
30. ⑴P=ηmv2/2 ——3分
而每秒通过该圆面的空气质量为m=ρπr2v ——3分
所以P=ηρπr2v3/2=2.9×104w ——2分
⑵设每个晶粒的直径为d,则V=1019πd3/6=10-6 ——4分
得: d=6×10-9m=6nm ——2分
31.⑴平衡时,mgsinθ=ILBcosθ ——3分
ε=BLVMcosθ ——3分
I=ε/2 R=BLVMcosθ/2 R ——3分
故:VM=2mgRsinθ/B2L2cos2θ ——2分
⑵ mgsinθ-ILBcosθ=ma ——3分
I=BL(VM/3)cosθ/2 R ——4分
故:a=2gsinθ/3 ——2分
32. 因反氢核和反氦核带负电,故均向左偏,其半径分别为r1和r2,轨迹
如题图所示。 ——4分
设氢核的质量为m,电量为q,由qvB=mv2/r ,则半径r=mv/qB ——3分
由于反氢核的质量也为m,电量也为-q,故轨道半径r1=r ——2分
但偏转方向相反,即x1= -x0 =-r/2 ——2分
由于反氦核的质量为4m,电量为-2q,故轨道半径r2 = 4mv/2 qB = 2r——2分
对图中角α,有sinα=(r-r/2)/r=1/2,则α=π/6 ——2分
磁场宽度D=rcosα=![]() /2· r/2
——2分
/2· r/2
——2分
设反氦核偏转角度为θ,则sinθ= D/2r = ![]() /4
/4
故![]() = —(2 r – 2 r cosθ)= —(2 --
= —(2 r – 2 r cosθ)= —(2 --![]() /2)r ————4分
/2)r ————4分
组题人: 窦云胜(塘沽一中) 肖跃强(静海一中) 赵晶岩(四十七中) 李庆忠(大港一中)