高三理科综合第七次月考试卷
理 科 综 合 能 力 测 试
考生须知:
1.全卷分试卷Ⅰ、Ⅱ,试卷共11页,有31小题,满分为300分,考试时间150分钟。
2.本试卷答案做在答卷的相应位置上,不能答在试题卷上。
3.请用钢笔或蓝、黑圆珠笔将班级、姓名、学号、试场号、座位号填写在答卷密封线以内的相应位置上。考试结束后只需上交答卷,考试时不能使用计算器。
4.本试卷可能用到的相对原子质量:H—1,C—12, O—16,Mg—24,S—32,Cl—35.5,Ca—40,Ba—137
第I卷(选择题,共126分)
一、选择题(本题包括13小题.每小题只有一个选项符合题意.每小题6分,共78分)
1.下列关于细胞的说法正确的一组是
① 含细胞壁结构的细胞必定为植物细胞 ② 含中心体的细胞必定为动物细胞 ③ 同一动物体不同组织细胞中线粒体含量不同 ④ 植物细胞必定含叶绿体 ⑤ 能进行光能自养的生物不一定是绿色植物
A.①③ B.①④ C.③⑤ D.②⑤
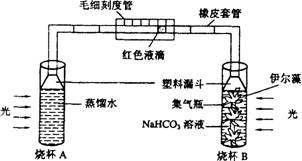 2.下图表示研究NaHCO3溶液浓度影响光合作用速率的实验,下列说法错误的是
2.下图表示研究NaHCO3溶液浓度影响光合作用速率的实验,下列说法错误的是
A.将整个装置放在光下,毛细管内的红色液滴会向左移动
B.将整个装置置于暗室,一段时间后检查红色液滴是否移动,可以证明光是光合作用的必要条件
C.当NaHCO3溶液浓度不变时,在B内加入少量蠕虫,对红色液滴移动不产生影响
D.为使对照更具说服力,应将伊尔藻置于蒸馏水中(不含NaHCO3)的烧杯中
3.桃的果实成熟时,果肉与果皮粘连的称为粘皮,不粘连的称为离皮;果肉与果核粘连的称为粘核,不粘连的称为离核。已知离皮(A)对粘皮(a)为显性,离核(B)对粘核(b)为显性。现将粘皮、离核的桃(甲)与离皮、粘核的桃(乙)杂交,所产生的子代出现4种表现型。由此推断,甲、乙两株桃的基因型分别是
A.AABB、aabb B.aaBB、Aabb C.aaBB、Aabb D.aaBb、Aabb
4.下列有关于多倍体与单倍体的说法有误的是:
A.多倍体植株一般表现为茎杆粗壮,叶片、果实和种子较大,所以四倍体葡萄比二倍体葡萄果实大。
B.多倍体在植物中远比在动物中普遍,是因为植物不能躲避环境条件剧烈变化的影响
C.海拔高的地方多倍体植物比例较高,这不但说明这样的环境易产生多倍体,而且也表明多倍体适应不良环境的能力强
D.利用秋水仙素处理单倍体幼苗,可得到二倍体或多倍体
5.将盆栽幼苗横放地上一周后,测得幼苗根尖的背地端与向地端生长素浓度之比为1∶2,请分析下图,幼苗根尖的背地端的生长素浓度范围是:
![]()
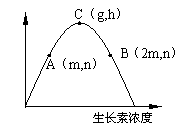

A.小于m B.大于m,小于2m C.大于2m D.无法确定
6.下列有关晶体的说法正确的是
A.分子晶体中分子间作用力越大,分子越稳定
B.原子晶体中共价键越强,晶体熔点越高
C.冰熔化时水分子中共价键发生断裂
D.氯化钠溶于水时离子键未被破坏
7.下列关于元素周期表和元素周期律的叙述正确的是
A.元素的性质随着相对原子质量的递增,呈周期性的变化
B.元素周期表中,元素所在族的序数都等于该族元素原子的最外层电子数
C.第三周期,随着核电荷数的递增,元素的离子半径依次减小
D.随着核电荷数的递增,VII A族元素的单质熔沸点升高,碱金属元素单质熔沸点降低
8.阿伏加德常数为NA,则下列说法正确的是
A.常温下,2.7g铝与足量的浓硫酸反应,失去的电子数为0.3NA
B.64g的铜发生氧化还原反应,一定失去2NA个电子
C.标准状况下,0.3 mol 双氧水中含有电子数为5.4NA
D.常温常压下,1mol氦气含有的核外电子数为4NA
9.三氯化氮分子中每个原子其最外层均达到8电子稳定结构,且氮与氯的共用电子对偏向于氮原子。则下列关于三氯化氮的叙述正确的是
A.N元素的非金属性比Cl元素弱
B.在NCl3分子中N为+3价,跟水发生水解反应的产物是HNO2和HCl
C.在NCl3分子中N为—3价,NCl3跟水发生水解反应的产物是NH3和HClO
D.NCl3跟水反应生成NH4Cl、O2和Cl2
10.某溶液中含有HCO3-、CO32-、SO32-、Na+、NO3- 五种离子。若向其中加入Na2O2充分反应后(溶液体积变化忽略不计),溶液中离子浓度保持不变的是
A.NO3- B.CO32-、NO3- C.SO32-、NO3- D.CO32-、NO3-、Na+
11.镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越来越成为人们研制绿色原电池的关注焦点。其中一种镁原电池的反应为:
|
A.负极反应为xMg-2xe-= xMg2+ B.正极反应为Mo3S4+2xe-= Mo3S42x-
|
12.等物质的量的下列物质:① ② Ca(H2PO4)2 ③ Si ④ Al2(SO4)3
⑤ NaHSO4,分别与足量的NaOH溶液反应,耗碱最由多到少的顺序正确的是
A.②①④③⑤ B.④②①③⑤ C.④②③①⑤ D.④①②③⑤
13.今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:(1)第一份加入AgNO3溶液有沉淀产生;(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol;(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。
根据上述实验,以下推测正确的是
A.K+一定存在,Cl-可能存在 B.100mL溶液中含0.01mol CO32-
C.K+可能存在,Cl-一定存在 D.Ba2+一定不存在,Mg2+可能存在
二、选择题(本题包括8小题.每小题给出的四个选项中,有的只有一个选项正确,有的有
多个选项正确,全部选对的得6分,选对但不全的得3分,有选错的得0分,共48分)
14.图中A是一个具有弹性的位置固定的线圈,当磁铁迅速向左接近时,则线圈A在
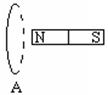 A.N极接近时扩大,S极接近时缩小
A.N极接近时扩大,S极接近时缩小
B.N极接近时缩小,S极接近时扩大
C.N极、S极接近时都缩小
 D.N极、S极接近时都扩大
D.N极、S极接近时都扩大
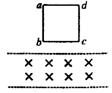
15.如图所示,让闭合矩形线圈abcd从高处自由下落一段距离后进人匀强磁场,从bc边开始进入磁场到ad边刚进入磁场的这一段时间里,如图所示的四个v—t图象中,可能表示线圈运动情况的是:
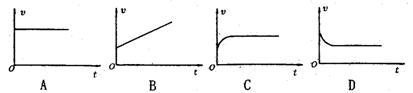
16.一长直导线MN中通以如图所示的交流电,在导线附近的正下方放置一闭合线圈,线圈平面与导线在同一平面内如图,则下列说法中止确的是:
 A.在t1时刻,线圈内有感应电流
A.在t1时刻,线圈内有感应电流
B.在t2时刻,线圈内没有感应电流
C.t>O的任意时刻,线圈内都有感应电流
D.以上说法都不对
17.如图电路中,A1和A2是完全相同的灯泡,线圈L的电阻可以忽略.说法中正确的是:
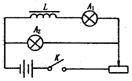 A.合上开关K接通电路时,A2先亮,A1后亮,最后一样亮
A.合上开关K接通电路时,A2先亮,A1后亮,最后一样亮
B.合上开关K接通电路时,A1和A2始终一样亮
C.断开开关K切断电路时,A2立即熄灭,A1过一会才熄灭
D.断开开关K切断电路时,A1和A2都要过一会儿才熄灭
18.如图所示,光滑导轨倾斜放置,其下端连接一个灯泡,匀强磁场垂直于导线所在平面,当ab棒下滑到稳定状态时,小灯泡获得的功率为P0,除灯泡外,其它电阻不计,要使灯泡的功率变为2P0,下列措施正确的是
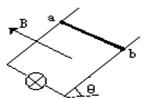 A.换一个电阻为原来2倍的灯泡
A.换一个电阻为原来2倍的灯泡
B.换一根质量为原来的![]() 倍的金属棒
倍的金属棒
C.把磁感强度B增为原来的2倍
 D.把导轨间的距离增大为原来的
D.把导轨间的距离增大为原来的![]() 倍
倍
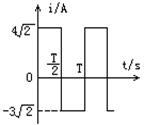
19.如图表示一交流电电流随时间而变化,此交流电的有效值是:
![]()
20.在交流电电路中,如果电源电动势的最大值不变,频率可以改变,
在如图电路的a、b两点间逐次将图中的电路元件甲、乙、丙单独接入,当使交流电频率增加时,可以观察到下列哪种情况
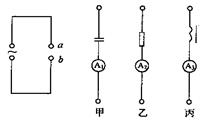 A.A1读数不变,A2增大,A3减小
A.A1读数不变,A2增大,A3减小
B.A1读数减小,A2不变,A3增大
C.A1读数增大,A2不变,A3减小
D.A1,A2 ,A3读数均不变
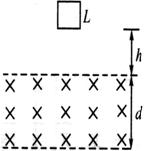
21.如图所示,两条水平虚线之间有垂直于纸面向里、宽度为d、磁感应强度为B的匀强磁场.质量为m、电阻为R的正方形线圈边长为L(L<d),线圈下边缘到磁场上边界的距离为h.将线圈由静止释放,其下边缘刚进入磁场和刚穿出磁场时刻的速度都是v0,则在线圈下边缘进入磁场到下边缘穿出磁场过程中,下列说法中正确的是
 A.线圈先减速后加速
A.线圈先减速后加速
B.线圈先加速后减速
C.线圈的最小速度一定是mgR/B2 L2
D.线圈的最小速度一定是![]()
第II卷(非选择题,共174分)
注意事项:
答第Ⅱ卷前,考生务必将自己的姓名、准考证号用钢笔或圆珠笔(蓝、黑色)写在答题卷密封线内相应的位置。答案写在答题卷上,不能答在试题卷上。
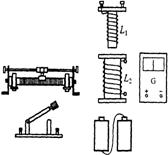 22.(16分)(1)如图可用来研究电磁感应现象及确定感应电流方向。
22.(16分)(1)如图可用来研究电磁感应现象及确定感应电流方向。
①在实物图中,用实线作为导线将实验仪器连成实验电路。
②将线圈L1插入L2中,合上开关稳定后。能使感应电流与原电流的绕行方向相同的实验操作是
A.插入软铁棒 B.拔出线圈L1
C.使变阻器接入电路的阻值变大 D.断开开关
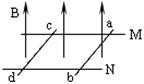 (2)如图所示,两光滑的金属导轨M、N水平放置处在竖直向上的匀强磁场中,搁在导轨上的两金属杆ab和cd垂直于轨,当ab杆沿导轨向右运动时,通过cd杆的电流方向是 ▲ ,cd杆
(2)如图所示,两光滑的金属导轨M、N水平放置处在竖直向上的匀强磁场中,搁在导轨上的两金属杆ab和cd垂直于轨,当ab杆沿导轨向右运动时,通过cd杆的电流方向是 ▲ ,cd杆
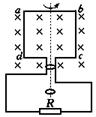 将向 ▲ 运动。
将向 ▲ 运动。
(3)一矩形线圈,面积是0.05m2,共100匝,线圈电阻为2Ω,外接电阻为R=8Ω,线圈在磁感应强度为B=T/Л的匀强磁场中以300r/min的转速绕垂直于磁感线的轴匀速转动,如图所示,若从中性面开始计时,则线圈中感应电动势的瞬时值表达式 ▲ V,线圈从开始计时经1/30s时,线圈中电流的瞬时值 ▲ A。
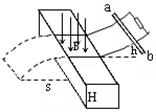
 23.(20分)如图所示,由导线制成的正方形框边长为L,每条边的电阻均为R,其中ab边材料较粗且电阻率较大,其质量为m,其余各边的质量均可忽略不计.线框可绕与cd边重合的水平轴oo’自由转动,不计空气阻力及摩擦.若线框从水平位置由静止释放,历时t到达竖直位置,此时ab边的速度为v.若线框始终处在方向竖直向下、磁感应强度为B的匀强磁场中,重力加速度为g.求:
23.(20分)如图所示,由导线制成的正方形框边长为L,每条边的电阻均为R,其中ab边材料较粗且电阻率较大,其质量为m,其余各边的质量均可忽略不计.线框可绕与cd边重合的水平轴oo’自由转动,不计空气阻力及摩擦.若线框从水平位置由静止释放,历时t到达竖直位置,此时ab边的速度为v.若线框始终处在方向竖直向下、磁感应强度为B的匀强磁场中,重力加速度为g.求:
(1)线框在竖直位置时,ab边两端的电压及所受的安培力大小.
(2)在这一过程中,通过线框横截面的电量.(3)这一过程中感应电动势的有效值.
 24.(20分)如图所示,把两根平行光滑金属导轨放在水平桌面上,桌子高H=0.8m,导轨距为L=0.2m,在导轨水平部分有磁感应强度B=0.1T、方向竖直向下的匀强磁场,弧形金属导轨的一端接有电阻R=1Ω,质量m=0.2kg金属杆
24.(20分)如图所示,把两根平行光滑金属导轨放在水平桌面上,桌子高H=0.8m,导轨距为L=0.2m,在导轨水平部分有磁感应强度B=0.1T、方向竖直向下的匀强磁场,弧形金属导轨的一端接有电阻R=1Ω,质量m=0.2kg金属杆![]() 由静止开始距桌面h=0.2m高处开始下滑,最后落到距桌面水平距离
由静止开始距桌面h=0.2m高处开始下滑,最后落到距桌面水平距离![]() =0.4m处,
=0.4m处,
金属杆及导轨电阻不计(g=10m/s2)。试求:
(1)金属杆进入导轨水平部分瞬间产生的磁感应电流的大小和方向;
(2)金属杆滑出导轨瞬间感应电动势的大小;
(3)整个过程中电阻R放出的热量。
25.(16分)人们利用发电机把天然存在的各种形式的能量转化为电能,为了合理地利用这些能源,发电站要修建在靠近这些天然资源的地方.但用电的地方却分布很广,因此需要把电能输送到很远的地方.某电站输送电压U=5000V,输送功率P=500kW,安装在输电线路的起点和终点的电度表一昼夜读数相差4800kW·h.试求:
(1)该电路的输电效率和输电线的电阻.
(2)如果发电机输出电压为250V,用户需要电压为220V.要使输电损耗为5%,分别求升压和降压变压器的原、副线圈匝数之比.(计算时取![]() )
)
26.(13分)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验 编号 | HA物质的量 浓度(mol/L) | NaOH物质的量 浓度(mol/L) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | c1 | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
请回答:
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸 ▲ ;
(2)不考虑其它组的实验结果,单从乙组情况分析,c1 ▲ (填“一定”或“不一定”)等于0.2mol/L,混合溶液中离子浓度c(A-)与c(Na+)的大小关系是
▲ ;
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是 ▲ 酸(填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是 ▲ ;
(4)丁组实验所得混合溶液中由水电离出的c(OH—)= ▲ mol/L,写出该混合溶液中下列算式的精确结果(不能做近似计算): c(Na+)-c(A—)= ▲ mol/L。
27.(15分)下列图1中B是一种常见的无色无味的液体。C是一种有磁性的化合物,E是一种无色无味的有毒气体。根据下列图1、图2,回答下列问题:
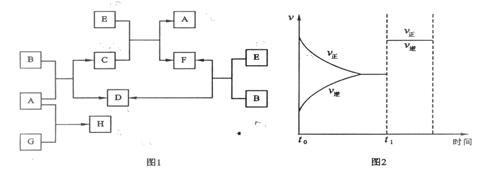
(1)写出C的化学式 ▲ ;
(2)E和N2是等电子体,请写出可能E的电子式 ▲ ;
(3)在101kPa和150℃时,可逆反应E(g)+ B(g)![]() F(g) + D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母)
F(g) + D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母)
▲ ;
A.升高温度 B.增大压强 C.加入催化剂
(4)若G是一种淡黄色固体单质,16 g G和足量的A反应放出的热量为Q kJ(Q > 0),写出这个反应的热化学方程式 ▲ 。若G是一种气态单质,H的水溶液可以和有机物I反应使溶液呈紫色,请写出I的结构简式
▲ ;H的水溶液呈酸性,请用离子方程式表示呈酸性的原因
▲ 。
28.(18分)有一包含有氧化镁的碳酸钙粉末,某课外活动小组通过实验,用测定氧化镁质量的方法测定混合粉末中碳酸钙的质量分数。请你根据他们设计的下列操作步骤进行补充,并回答有关问题。
(1)称取3.3g样品放入锥形瓶中,缓慢滴入60mL3.0mol/L的盐酸。滴加盐酸过程中,锥形瓶内可观察到的现象是 ▲ ;
(2)加入 ▲ ;
(3)称量一张滤纸(其质量为W1g)安装过滤器,过滤。过滤时,某同学操作不慎,使漏斗里的液体的液面高于滤纸的边缘,该同学发现后,应采取的措施是 ▲ ;
(4) ▲ ,目的是 ▲ ;
(5)取滤渣连同滤纸放在坩埚内进行干燥与灼烧至恒重W3g(已知坩埚的质量为W2g),滤渣经灼烧后,固体物的成分(不考虑滤纸灰)是(填化学式) ▲ ;
(6)取另一张质量与过滤时所使用的相同的滤纸放在另一坩埚(质量为W4g)内干燥与灼烧至恒重W5g。则该样品中碳酸钙的质量分数为 ▲ 。某同学在进行(1)操作称量样品时,是把样品放在托盘天平的右盘里,左盘里共放了3g砝码,天平摆动到达平衡时,游码处于0.3g的刻度上。这位同学的称量操作对最后结果造成的影响是(填无、偏高、偏低) ▲ 。
29.(14分)“C1化学”是指以分子中只含一个碳原子的物质为原料进行物质合成的化学。下图是以天然气的主要成分为原料的合成路线流程图,其中“混合气体”的成分与水煤气相同;B的水溶液有杀菌防腐性能;D是C的钠盐,2mol D分子间脱去1mol H2分子可缩合生成E;H是F与A按物质的量之比为1∶2反应的产物。
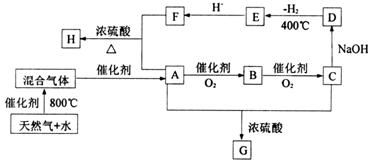
填写下列空白:
(1)天然气主要成分的电子式是 ▲ ,E的化学式是 ▲ ;
(2)D、G的结构简式:D ▲ 、G ▲ 。
(3)写出下列反应式的化学方程:A→B ▲ ,A+F→H ▲ 。
30.(21分)某育种科学家在农田中发现一株大穗不抗病的小麦,自花授粉后获得160颗种子。这些种子发育成的小麦中有30株为大穗抗病,有X(X≠0)株为小穗抗病,其余都染病。假定控制小麦穗大小的基因分别用D、d表示,控制不抗病与抗病的基因分别用T、t表示。请分析回答下列问题:
(1)题中的30株大穗抗病的小麦的基因型为 ▲ 。其中能够稳定遗传的约为 ▲ 株;
(2)若将这30株大穗抗病的小麦作为亲本自交,在F1中选择大穗抗病的再进行自交,F2中能稳定遗传的大穗抗病小麦占F2中所有大穗抗病小麦的比例约为 ▲ ;
(3)将选出的大穗抗病小麦种子晒干后放在容器内,采用什么措施可延长储存期?(不少于3种措施) ▲ ;
(4)上述育种方法是 ▲ 。选育能稳定遗传的大穗抗病小麦还可以采用的育种方法是 ▲ 。
31.(21分)在研究细胞周期时,可用BrdU进行标记。将细胞置于含有BrdU的某种培养基中培养,当细胞DNA复制时,BrdU可替代胸腺嘧啶脱氧核苷酸掺入到DNA的子链中。将处于不同细胞周期的中期细胞进行常规制片,经特殊染色后,显微镜下观察每条染色体的姐妹染色单体的着色情况。由于掺入BrdU的情况不同,着色的深浅也不同;在染色单体中,若DNA只有一条单链掺有BrdU,则着色深;若DNA的两条单链都掺有BrdU,使DNA双链螺旋程度降低,从而着色浅。请分析回答:
(1)若观察到的置于含有BrdU的某种培养基中的细胞中所有染色体上的两条姐妹染色单体着色深,则该细胞正处于 ▲ 个细胞周期的中期;
(2)若细胞中的所有染色体上的两条姐妹染色单体一条着色深、一条着色浅,则该细胞正处于第 ▲ 个细胞周期的中期。 判断的理由是 ▲ 。
现有一真核细胞,以下则是与该细胞中的遗传信息及其表达相关的问题:
(3)将同位素标记的尿核苷(尿嘧啶和核糖的结合物)加入细胞培养液中,不久在细胞核中发现被标记的是 ▲ ;
(4)将从A细胞中提取的核酸,通过基因工程的方法,转移到另一种细胞B中,当转入 ▲ 时,其遗传信息在B细胞中得到表达并能够复制传给下一代,当转入 ▲ 时,在B细胞中虽能合成相应的蛋白质,但性状不会遗传。
