2003年MAM高考理综仿真试题(六)答案
一、1.C 2.B 3.A 4.D 5.B 6.D 7.D 8.D 9.C 10.C 11.A 12.B 13.C 14.D 15.C 16.D 17.B 18.C 19.C 20.B 21.A 22.A
二、23.(1)离子 交换吸附 主动运输(各2分)
(2)N元素等矿质元素大量增加,引起藻类大量繁殖(3分)
藻类等水生生物大量死亡,水体中有机物大量增加(3分)
(3)4 6 (各2分)
藻类大量减少,供鱼类捕食的食物缺乏,而引起鱼类大量减少(2分)
24.(1)A B (2)甲状腺激素能促进蝌蚪的发育 (3)对照 B 碘是甲状腺激素合成的必需成分(每空3分)
25.(1)D(2分) (2)CO2、H2O、C2H5OH 上升
呼吸作用释放能量,使瓶内温度升高(3分)
(3)防止空气中CO2进入锥形瓶,影响实验效果
防止溶液表面形成BaCO3,影响对CO2的吸收(2分)
(4)![]() (2分)
(2分)
26.(1)4.25×[M(![]() )]-1=
)]-1=![]() =0.0188(3分)
=0.0188(3分)
(2)由中子个数守恒有:N=[(226-88)-(4-2)]=136(3分)
(3)在不含重氢的苯中加入HCl后再加入足量的NaOH溶液检查混合物中有无放射性,
若有放射性则说明 分子中H原子与HCl分子中H原子存在着氢交换。(5分)
(4)因为光合作用中生成O2全部来自于水中的氧元素,所以生成氧气摩尔质量为 36 g·mol-1 (3分)
27.(1)浓HCl 加热(2分)
(2)冷水,将PCl3蒸气冷却到76℃以下,使其变为液体而在烧瓶中收集。(2分)
(3)CaCl2(4分)
(4)白磷上残留的水溶解在酒精中,残留的酒精又溶解在乙醚中,可完全除去白磷上的水分(2分)
(5)NaOH溶液(2分)
28.(1)方法一:
①2Na2O2+2CO2=2Na2CO3+O2↑
②2Na2O2+2H2O=4NaOH+O2↑ 补充适量的水蒸气
方法二:
(1) 2H2O+O2+4e=4OH-;
CO2+2OH-=CO![]() +H2O;
+H2O;
2H2+4OH--4e=4H2O;
CO32-+H2O=2OH-+CO2↑(4分)
(2)阴;4OH--4e=2H2O+O2↑(2分)
(3)生成的甲烷可做飞船的气体燃料,体现了物质的循环使用和充分利用(2分)
29.(1)2 atm(或2.02×105 Pa)(4分)
(因为:s、P、t下,![]() =
=![]() ×22.4=0.672 L
×22.4=0.672 L
在546 K时 ![]() =
=![]() =2 atm)
=2 atm)
(2)0.96 (4分)
(因为:P0=4-![]() =2
atm)
=2
atm)
设O2在标况下体积为V
![]()
V=0.672 L
(混合气体中![]() =
=![]() ×32=0.96 g)
×32=0.96 g)
(3)当放出相同热量时,燃烧无烟煤放出的CO2是CH4的222% (4分)
(CH4+2O2![]() CO2+2H2O+890 kJ C+O2
CO2+2H2O+890 kJ C+O2![]() CO2+403.2 kJ,燃烧无烟煤放出相同的890
kJ热量,则放出CO2为
CO2+403.2 kJ,燃烧无烟煤放出相同的890
kJ热量,则放出CO2为![]() =2.2 mol,可见,放出相同热量时,燃烧无烟煤放出的CO2是CH4的222%。)
=2.2 mol,可见,放出相同热量时,燃烧无烟煤放出的CO2是CH4的222%。)
结论:根据上述比较,这将加剧温室效应,使全球升温造成人类环境的恶化。因此,改变燃料的种类减少CO2排放是保护环境的重要内容。(4分)
30.(1)原核(2分)
(2)C17H18N3O3F 羰基 羧基(6分)
(3)5 1(4分)
(4)应注意18O不在水中

(4分)
(5)多种只写一种即可

(4分)
31.(1)参考电路:(4分)
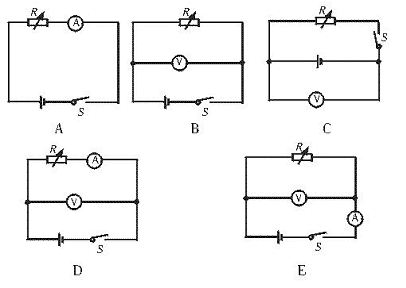
(2)简单的实验操作方案:
(ⅰ)采用电路A(或B)时:①闭合开关S,电阻箱取值R1时,记下电流表(或电压表)指针偏转格数N1,②电阻箱取值R2时,记下电流表(或电压表)指针偏转格数N2。(2分)
(ⅱ)采用电路C时,①断开S,记下电压表指针偏转格数N1。②电阻箱取值R,闭合S,记下电压表指针偏转格数N2。(2分)
(ⅲ)采用电路D(或E)时:①闭合S,电阻箱取值R1时,记下电流表,电压表指针偏转格数分别为n1和N1,②电阻箱取值为R2时,记下电流表,电压表指针偏转格数分别为n2和N2。(2分)
(3)推导r的表达式:设电流表每小格刻度值为I0,电压表每小格刻度值为U0
采用电路A:![]()
得r=![]()
采用电路B: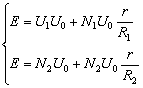
得r=![]()
采用电路C: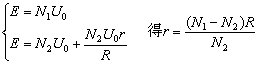
采用电路D、E时:![]()
而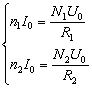
得r=![]() 或 r=
或 r=![]() (6分)
(6分)
(4)采用电路A、E时,由于产生误差的原因是r测=RA+r真,因此要求电流表内阻RA<<r,且选择电阻箱取值时,在电流表不超出量程的条件下,应尽量使R1、R2的值不要比r大得太多。
采用电路B、C、D时,由于产生误差的原因是电压表的分流,r测是r真与RV的并联值,因此要求电压表内阻RV>>r,且考虑到误差产生的原因,在选择电阻箱取值时,R的值要比RV小得多。(4分)
32.太阳上的聚变反应发生一次需消耗4个![]() 核,故1 kg的
核,故1 kg的![]() 核可发生该反应的次数为
核可发生该反应的次数为
N=![]() ①(2分)
①(2分)
由质能公式可知,该反应每发生一次释放出来的能量为
ΔE=(4mP-mα-2me)C2 ②(2分)
因此1 kg的![]() 核全部发生该反应时所释放出来的能量共为
核全部发生该反应时所释放出来的能量共为
E=N·ΔE ③(2分)
氢气燃烧与氧气化合生成水的化学反应式为
2H2+O2→2H2O (3分)
每形成1个水分子H2O释放出的能量ε=6.2 eV,若采用国际单位,则ε=6.2×1.6× 10-19 J=9.92×10-19 J。 (2分)
由化学反应式可知,每合成一个H2O分子,需燃烧掉一个H2分子。而每个H2分子含两个质子和两个电子。故要产生相当于1 kg的![]() 核聚变成α粒子时所释放的能量,需燃烧掉的氢气质量为 M=2(mP+me)
核聚变成α粒子时所释放的能量,需燃烧掉的氢气质量为 M=2(mP+me)![]() ④(2分)
④(2分)
33.【解析】(1)磁铁与螺线管在相互作用的过程中,竖直方向各自的重力与向上的弹力都是相平衡的,水平方向由于螺线管中磁通量发生变化,而产生感应电流,感应电流的磁场阻碍磁铁运动,使磁铁向右减速运动而穿出螺线管,螺线管所受的安培力使其向右做加速运动。(5分)
(2)以磁铁和螺线管为系统,系统所受合外力为零,所以系统动量守恒,则:
Mv0=M·(![]() v0)+(
v0)+(![]() M)v ①
M)v ①
解得,磁铁穿出螺线管后,螺线管的速度v=![]() v0(3分)
v0(3分)
系统相互作用的过程中,系统减少的动能转化为电能,再转化为内能,由能的转化和守恒定律有:
Q=![]() Mv02-
Mv02-![]() M(
M(![]() v0)2-
v0)2-![]() ·(
·(![]() M)v2 ②
M)v2 ②
将v=![]() v0代入求得Q=
v0代入求得Q=![]() Mv02(3分)
Mv02(3分)
34.【解析】
(1)跳绳时每次跳跃时间△t=0.5 s,腾空时间为△t空=0.2 s,最大升高H=g(△t空/2)2/2= 0.05 m。(2分)
(2)克服重力做功W=mgH=25 J,平均功率为:
P=W/△t=50 W(3分)
(3)心脏每次泵血做功W′=FL=P△v=3 J,平均功率P′=W′/t′=7 W,是平常的4.7倍。(2分)
(4)由C6H12O6![]() 2C3H6O3+能量(2分)
2C3H6O3+能量(2分)
本题正确选项为B。
【答案】见解析。