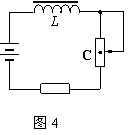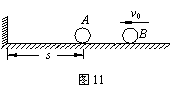2006��߿�ģ������
�����ۺ���������
���Ծ��ֵڢ����ѡ���⣩�͵ڢ������ѡ���⣩�����֣��ڢ��1��5ҳ���ڢ��6��14ҳ�����Խ�������������ʹ��һ�����ء�
�ڢ����ѡ���21��ÿ��6�ֹ�126�֣�
ע�����
����1����ڢ��ǰ��������ؽ��Լ�����������֤�š����Կ�ĿͿд�ڴ���ϡ�
����2��ÿС��ѡ���𰸺���Ǧ�ʰѴ���϶�Ӧ��Ŀ�Ĵ𰸱��Ϳ�ڣ�����Ķ�������Ƥ���ɾ�����ѡͿ�����𰸱�ţ����ܴ���������ϡ�
�������ݿɹ�����ʱ�ο���
���ԭ��������ԭ��������
H 1�� O��16�� Ne��20 Na��23�� S��32 Fe��56�� Cu��64
���
һ��ѡ�������������13С�⡣ÿС��ֻ��һ��ѡ��������⣩
1�����й������µ��ڵ������У���ȷ���ǡ������������������������� ������
����A���������Ǹо����±仯����Ҫ���࣬���γ�������Ⱦ��IJ�λ
����B������������ֲ���Ƥ�����¾��������ֲ�����������
C�����价���г��֡���ս����ս����������ë�������Ľ��
����D�������Ȼ����д����ź���δ����������ֻ�к�Һ������ʹ����ɢʧ
2.���й��ڹ������ǿ�ȵ���������ȷ���ǡ����������������������� ������
A����һöҶƬ�����ϵ��������������У���������ǿ���Dz���ı��
B����ֲ��Ⱥ��Ĵ�ֱ�����ϣ�ռ�ݲ�ͬ�ռ��ֲ��ҶƬ�Ĺ������ǿ���в���
C��ֲ��Ĺ������ǿ��ֻ�ܵ��������ص�Ӱ�죬���������
D��������ǿ����ͬ��������ֲ��Ĺ������ǿ�ȸ�������ֲ��
3.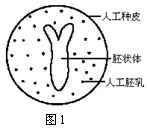 ͼ1ʾһ�˹����ӡ��������˹����ӵ��������������йص�����������ȷ���ǡ���������������
�� ��
ͼ1ʾһ�˹����ӡ��������˹����ӵ��������������йص�����������ȷ���ǡ���������������
�� ��
A.�˹�����һ���������ֲ��ϸ��ͨ����֯�����������
B.��״������������֯�ֻ����ɣ�����ϸ��ֻ���γ�������֯���ܱ��ֳ�ȫ����
C.ͬһ���ε��˹����ӿ��Ա�֤������ͬ�Ļ�����
D.��״������δ�ֻ��ġ����з���������ϸ������
4.�������������ȷ���ǡ��������������������������������������� �� ��
A.�ӹ���������һ�ֶ���ֲ����ij����������������Ϊ�õ�����������
B.���ũ��Ĺ���ǿ�ȣ�����������ҹ�²������������������Ҫ��ʩ
C.2,4-D��������ʹ�ã���Ч�ؽ����ijЩ���������ʵ�ķ�������������
D.�����㴹�����ȡ��ɴ�ʹ�������ѣ���Ϊ���庬�д����ټ��ء���
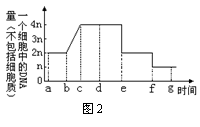 5��ͼ2��ʾ������ij���ᆱ�����γɾ��ӵĹ����У�һ��ϸ���ڣ�������ϸ���ʣ�DNA���������ı仯�����и����жԱ�ͼ�Ľ�����ȫ��ȷ���� ��
��
5��ͼ2��ʾ������ij���ᆱ�����γɾ��ӵĹ����У�һ��ϸ���ڣ�������ϸ���ʣ�DNA���������ı仯�����и����жԱ�ͼ�Ľ�����ȫ��ȷ���� ��
��
A��a��d��ʾ��ԭϸ����f���ʾ�������ѽ���
B��e���ʾ������һ�η��ѽ�����g���ʾ�����ڶ��η��ѽ���
C��a��e��ʾ������ĸϸ����f��g��ʾ����ϸ�������γɾ���
D��d��e�����У�ͬԴȾɫ����룬e��f�����У���ͬԴȾɫ���������
6��2005��11��13�գ���ʯ�ͼ���ʯ����˾˫����������ը�������ɻ������ģ����Ⱦ����֪��Ҫ��Ⱦ��Ϊ����������C6H5NH2�����������ȣ������йر�����������������˵���в���ȷ���ǣ�������
A����ȼ��ʱ���������Ĵ���Ũ�̵Ļ���
��B��������������ȼ��ʱ�����ػ�ɫ��Ũ��
��C�����������������������ڷ�����
����D����������һ�ִ��п�����ζ����״Һ�壬�ܶȴ���ˮ����ˮ�о��м��ߵ��ȶ��ԣ���ɵ�ˮ����Ⱦ������൱����ʱ��
7������˵����ȷ���ǣ��� ��
����A.10 g��������ԭ����Ϊ6.02��1023
����B.25��ʱ��pH=6��ˮ��Һ��c(H+)>c(OH-)
����C.ʵ����������ʱ��������CuSO4�ɼӿ췴Ӧ�����������������ˮ��
����D.��16.0 g��ˮ����ͭ��ĩ����������������ͭ��Һ�л�����25.0 g����
8�������¹ʴ�����������ȷ���ǣ�������
����A.���ϵ���Ũ���������ô���ˮ��ϴ
B.Ƥ����մ�˱���������Ũ����������Һϴ��
����C.�������Ż�Ѹ����ɳ�����
����D.ˮ���¶ȼƲ������ƣ�Ѹ�ٽ�ˮ���ռ�ˮ�⣬�ռ�������������۸���
9���ø���ĸ�����ؿ����Ƶü����������������KMnO4��MnO2+K2O+O2(240��)������˵������ȷ���ǣ�������
����A.ÿ����11.2 L����ת����2 mol����
����B.��ͬ������KMnO4�ֽ⣬����MnO2�ķ�Ӧ������K2MnO4�ķ�Ӧ�ų���������
C.O2���������MnO2�ǻ�ԭ����
D.�ڴ������£�KMnO4��������ǿ��O2
10��������������Һ���ܴ������棬����Һ����þ��������������ǣ��� ��
�� A.Ba2+��Na+��NO3-��I-������������������ B.H+��Ag+��NO3-��HCO3-
�� C.Fe3+��Na+��S2-��Cl-������������������ D.Al3+��K+��Br-��SO42-
11����ijһ�ݻ�Ϊ2 L���ܱ������ڣ�����0.2 mol��CO��0.2 mol��H2O���ڴ������ڵ������¸��¼��ȣ��������·�Ӧ��
CO(g) +H2O (g)
![]() CO2(g) + H2(g)����H=a kJ/mol����Ӧ�ﵽƽ����c(CO):c(CO2)= 3:2������˵����ȷ���ǣ�������
CO2(g) + H2(g)����H=a kJ/mol����Ӧ�ﵽƽ����c(CO):c(CO2)= 3:2������˵����ȷ���ǣ�������
A���жϸ÷�Ӧ�ﵽƽ���������CO��H2O��CO2��H2��Ũ�ȶ����
��B����Ӧ�ų�������Ϊ0.04 a kJ
��C��ƽ��ʱH2O ��ת����Ϊ40%
D���������������ѹ��Ϊ1 L�������ڸ÷�Ӧƽ�������ƶ�
12���������Ϊ1 L��pH������2������ʹ�����Һ�У��ֱ�Ͷ��0.23 gNa����ͼ3�бȽϷ��Ϸ�Ӧ��ʵ�������ǣ�������
 | |||
 | |||
13�����������У����������ᷴӦ������������������Һ��Ӧ���ǣ�����
�� ��![]() ����NaHCO3����������Al����������
����NaHCO3����������Al����������![]() ������������ ��Al2��SO4��3
������������ ��Al2��SO4��3
| ����A���٢� | B���ۢ� | C���٢ڢ� | D���٢ۢ� |
����ѡ���⣨�������8С�⡣ÿС��������ĸ�ѡ���У��е�ֻ��һ��ѡ����ȷ���е��ж��ѡ����ȷ��ȫ��ѡ�Եĵ�6�֣�ѡ�Ե���ȫ�ĵ�3�֣���ѡ���ĵ�0�֣�
14������˵������ȷ���� ������ ��
A������ķ������˶����ܵ��ܺ;������������
B������ͬһ�����壬�¶�Խ�ߣ�����ƽ������һ��Խ��
C��Ҫʹ����ķ���ƽ���������������������崫��
D��һ�����������壬�¶�����ʱ�����Ӽ��ƽ������һ������
15������˵����ȷ���ǣ����� ��
����A��̫�������������Ҫ����̫���ڲ����ѱ䷴Ӧ
����B������¬ɪ���Ħ�����ɢ��ʵ����Թ���ԭ�Ӻ˵Ĵ�С
����C���������������ݦ�����ɢ��ʵ������ó���
����D����ԭ�Ӻ�����ӴӰ뾶��С�Ĺ��ԾǨ���뾶�ϴ�Ĺ��ʱ�����ӵĶ��ܼ�С����������������������
16���ס�����ֻ����ɴ���ͬһ��Բ�ι�����Ƶ������У�����ǰ�����ں����ҷɴ��ϼɴ�ʵ�ֶԽӵĹ��̣�����˵������ȷ���� ����������
����A���ҷɴ�������������������������ʹ�ҷɴ����٣����ʵ�����ɴ��Խ�
B���ɴ������������������ǰ������ʹ�ɴ����٣����ʵ�����ɴ��Խ�
����C���ס��ҷɴ�ͬʱ����������������ҷɴ����ٶ��ɴ����٣����ʵ�����ɴ��Խ�
����D���������ַ��������ܴﵽ�ɴ��Խӵ�Ŀ��
|
|
17����ͼ4��ʾ��·��L���Ը�ϵ���ϴ����Ȧ���ڻ����������Ļ���ƬP��A��Ѹ�ٻ���B�˵Ĺ����У�����AB�е�Cʱͨ����Ȧ�ĵ���ΪI1��P��B��Ѹ�ٻ���A�˵Ĺ����У�����C��ʱͨ����Ȧ�ĵ���ΪI2��P�̶���C�㲻�����ﵽ�ȶ�ʱͨ����Ȧ����ΪI0���� ������ ��
A��I1=I2=I0��������B��I1>I0>I2������ C��I1=I2>I0������ D��I1<I0<I2
|
|
18����ͼ5��ʾ��a��b��һ��ƽ�еĽ����壬�ֱ�ӵ�ֱ����Դ�������ϣ��ұ���һ���壬���м俪��һС��d���ڽϴ�Ŀռ䷶Χ�ڴ�������ǿ�ų����Ÿ�Ӧǿ�ȴ�СΪB������ֱֽ���������a��b����仹��������ǿ�糡��������������е��е�c������һ�������ӣ���Щ�����Ӷ���ֱ���˶����Ҳ࣬��d�������ֳ�3��������Щ�����ӵġ� ������ ��
A���ٶ�һ������ͬ
B������һ����3�ֲ�ͬ����ֵ
C������һ����3�ֲ�ͬ����ֵ
D���Ⱥɣ�q/m��һ����3�ֲ�ͬ����ֵ
|
|
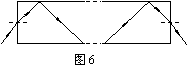
19������ͨ����һ���ִ�����ͨѶ�ֶΣ��������ṩ�����������ٶȡ���������ͨ�ŷ���Ϊ���о�����ķ��㣬���ǽ����ά��Ϊһ����ֱ�IJ����ܣ���ͼ6��ʾ����˲����ܳ�ΪL��������Ϊn���ҹ��ڲ������ڽ�����ǡ�÷���ȫ���䡣��֪��������еĴ����ٶ�Ϊc�����ͨ���˶β����������ʱ��Ϊ����������
A��nL/c����B��n2L/c��C��nL/c2���� D��n2L/c2
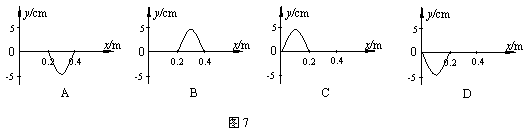
20��ij�ʵ�������ԭ��O������г�˶��������Ϊ5.0cm��������Ϊ0.40s�����ڽ�������x������ֱ�ߴ����������ٶ�Ϊ1.0m/s��������ƽ��λ��O������0.20s������ֹͣ����ֹͣ��0.20s��ʱ�̵IJ��ο�����ͼ7�е� ���������� ��
|
|
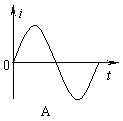
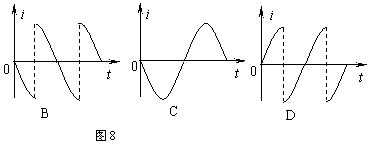
21����ͼ8��ʾ, ����OO������ߴ����ŷ���ֱֽ���������ǿ�ų��У��ұ�û�дų������Ѿ�����Ȧabcd�ĶԳ���ǡ��ų��߽��غϣ���Ȧƽ����ų���ֱ���涨��abcd�ĵ�������Ϊ��������������Ȧ��ͼʾ������OO��������ת������ab������ֽ�⡢cd������ֽ��ת����������ͼʾλ�ÿ�ʼ��ʱ��ͼ6�е��ĸ�ͼ������ȷ��ʾ��Ȧ�ڵĸ�Ӧ������ʱ��仯���ɵ��ǡ�����������
|
|
�������������������� ����
22����17�֣�
��1��������һЩ�йظ�������ʵ���������������ȷ�������������� ������д��ȷ˵��ǰ�����ţ�
�� �ڡ��о��ȱ���ֱ���˶���ʵ����ͨ��ֽ���ϴ��µ�һϵ�е��ֱ�������������һ��ʱֽ����˲ʱ�ٶȴ�С
�� �ڡ���֤����ƽ���ı��ζ���ʵ��������Ƥ���ϸ��Ҫ�Գ�������ʵ��ʱҪʹ������ľ��ƽ��ƽ��
�� �ڡ��õ��ڲⶨ�������ٶȡ�ʵ��������ڳ�����������õ�gֵƫС����ԭ������ǽ�ȫ�Ĵ���n���Ϊn-1
�� �ڡ���֤��е�غ㶨�ɡ���ʵ������Ҫ����ƽ�����壨�ش���������
|
| |||||||||||
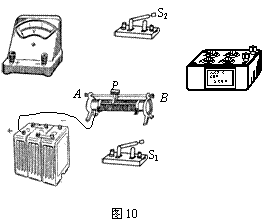
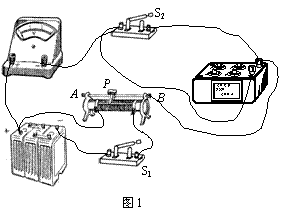
��2������һ����Ϊ3V�ĵ�ѹ��������ԼΪ3k����Ϊ�˽�ȷ�ز������ڵ��裬��û�е�����������£�ijͬѧ�������ͼ9��ʾ��ʵ���·�����˵�·���Բ����ѹ�����ڵ��衣����R1�������ֵΪ9999���ĵ����䣬R2�������ֵΪ20���Ļ�����������
�� �Ը���ͼ9��ʾ�ĵ�·ͼ�������ͼ10��ʾ��ʵ���·�����ߡ�
�� ��ͨ��·ǰӦ�������������Ļ���ͷP�������� �ˡ�
�� ���ݵ�·ͼ����˳��д����ʵ�����Ҫ�������衣
|
|
23����16�֣���ͼ11��ʾ������Ϊm��С��A���ڹ⻬ˮƽ����ϣ�С��������ֱǽ��Ϊs����һ������ΪM=3m��С��B���ٶ�v0�ع�������˶�����A������������֪����A����ٶȴ�СΪ1.2v0��С��A��ǽ�ڵ���ײ��������е����ʧ����С�������Ϊ�ʵ㣬����ײʱ�伫�̡���1����������һ����ײ��С��B���ٶȴ�С�ͷ���2����������ײ�Ĺ�����A���B�������Ĵ�С����3���������ڶ�����ײ��λ�õ�ǽ�ڵľ��롣
|
|
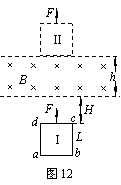
24����19�֣���ͼ12��ʾ���ڸ߶Ȳ�h��0.50m��ƽ�����߷�Χ�ڣ��дŸ�ǿ��B��0.50T������ˮƽ�������ǿ�ų����������߿�abcd������m��0.10kg���߳�L��0.50m������R��0.50�����߿�ƽ������ֱƽ��ƽ�У���ֹ��λ�á�I��ʱ��cd�߸��ų��±�Ե��һ�ξ��롣����һ��ֱ���ϵĺ���F��4.0N�������߿ÿ���λ�á������ٶȿ�ʼ�����˶��������ų��������λ�á���ab��ǡ�ó��ų������߿�ƽ�����˶��б�������ֱƽ���ڣ���cd�߱���ˮƽ����cd�߸ս���ų�ʱ���߿�ǡ�ÿ�ʼ�������˶�����gȡ10m��s2��
������1���߿����ų�ǰ��ų��±߽�ľ���H��
��������2���߿���λ�á���λ�á��Ĺ����У�����F���Ĺ��Ƕ��٣��߿��ڲ������������Ƕ���?
|
|
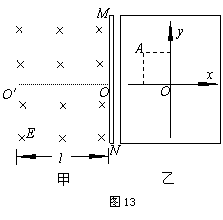
25����20�֣���ͼ13����ʾ��ͼ���Ҳ�MNΪһ��ֱ���õ�ӫ������OΪ�����е㣬OO����ӫ������ֱ���ҳ���Ϊl����MN�����ռ��ڴ����ŷ���ˮƽ�������ǿ�糡����ǿ��СΪE����ͼ�ǴӼ�ͼ�����ȥ��ӫ�����õ���ƽ��ͼ����ӫ��������OΪԭ�㽨����ͼ��ֱ������ϵ��һϸ������Ϊm�����Ϊq�Ĵ�����������ͬ�ij��ٶ�v0��O������O��O��������糡�������ӵ����������Ӽ������ö��ɺ��Բ��ơ�
��1��������MN���ռ��һ����ǿ�ų���ʹ��ӫ�����ϵ�����ǡ��λ��ԭ��O����������ų��ĴŸ�ǿ�ȵĴ�С�ͷ���
��2������Ÿ�ǿ�ȵĴ�С���ֲ��䣬���ѷ����Ϊ��糡������ͬ����ӫ�����ϵ�����λ��ͼ��A�㴦����֪A��������� ![]() �������ĺ��������ֵ��
�������ĺ��������ֵ��
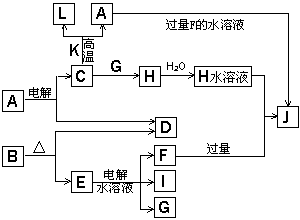
26����15�֣�C��D��G��I��Ϊ������Ԫ���γɵĵ��ʣ�D��G��IΪ�����ǽ�����̬���ʡ�D�������������Ǵ�����������3����C��Gͬ���ڣ����������������4�����ǵļ����ӵ��Ӳ�ṹ��ͬ�����������ת����ϵ��
|
������ ����գ�
(1)D��I���γ�ԭ�Ӹ�����Ϊ1��1�Ĺ��ۻ������д�������ʽ�������������� ��
G��IҲ���γ�ԭ�Ӹ�����Ϊ1��1�Ĺ��ۻ������д�������ʽ�������������� ��
��2��L��ĿǰӦ����㷺�Ľ�������̼����������L��������д�����Eˮ��Һ�Ļ�ѧ����ʽ�������������������������������������������� �������� ��
��3��������K �к�����ɵ���L��Ԫ�أ��Ҹ�Ԫ�ص���������Ϊ70%����Ӧ�ٵĻ�ѧ����ʽ���������������������������������������������� ������ ��
��4��д��A+F ��J�����ӷ���ʽ�������������������������������������� ��
27����12�֣�A��B��C������ɫ��Һ����֪��
��A��B��Һ��Ϻ���ȣ��ų���ɫ����X������ɫ�����ױ�C��Һ���ա�
��A��C��Һ��Ϻ�����������ˮ�İ�ɫ������
��B��C��Һ�зֱ����ͭƬ����������Ӧ������B��C��Һ��Ϻ��ٷ���ͭƬ������ɫ����Y���ɣ��õ���ɫ��Һ��
�ܽ�C��Һ�зֱ����ͭƬ�����������г������ȣ����Ͻ��裬����ɫ����Z���ɡ�
����գ�
��1��A�Ļ�ѧʽ������������ �� B�Ļ�ѧʽ������������ ��C�Ļ�ѧʽ������������ ��
��2��д����ɫ����X����ɫ����Y�Ļ�ѧ����ʽ������������������������������ ��
28��(21��) ij�л�������A����Է�����������������С��200����������֪������̼����������Ϊ64.51���������������Ϊ9.68%������Ϊ����A�������ԣ��Ƿ������е���Ч�ɷ֣�37.2mg A����20.0 mL 0.0100mol/L��������ˮ��Һ���ζ��ﵽ�ζ��յ㡣
��1���л�������A����Է������������������������������� ���û�����Ļ�ѧʽ������ʽ�������������������� �������к������������Ȼ���
��2����һ�������£�ϩ���ɷ�����������ԭˮ�ⷴӦ�������ʻ�������÷�Ӧ�ɱ�ʾΪ��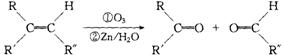
��֪�л�������A��ʹ������Ȼ�̼��Һ��ɫ��A������������ԭˮ�ⷴӦ����B��C��B�ܷ���������Ӧ������������ƻ�����������Һ��Ӧ��
|
|
|
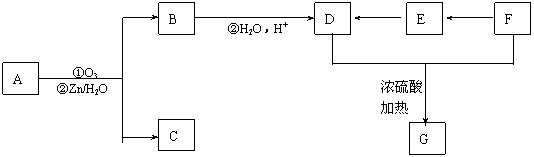 |
1molD��������̼��������Һ��Ӧ�ɷų�������̼44.8L(��״��)������D��F��Ũ���������¼��ȣ���������һ����ѧʽ������ʽ��ΪC4H4O4����Ԫ��G���÷�Ӧ�Ļ�ѧ����ʽ�������������������������������������������������� ����Ӧ���������������� ��D��̼�����Ʒ�Ӧ�Ļ�ѧ����ʽ��������������������������������������������������
������3�����ⶨ���л�������Cû��֧����������û�С�CH3��д���л�������A�Ľṹ��ʽ������������������������������������������������ ��
29����12�֣�ijУ��ѧС��ѧ����������ʵ�顣
��1��ʹ��ͭ��ϡ�����Ʊ�����ͭ���塣
��������
|
|
|
| ||||||||
| ||||||||
��������ٹ۲쵽�������������������������������������������������� ���� ������۵���Ҫ���������������������������������������������������������� ��
��2������ͭ�ܽ�ȵIJⶨ��
��ʯī�缫����ͬ����ⱥ��CuSO4��Һ�������ĵ缫��Ӧʽ���������������������������������������� ����֪����CuSO4��Һ������Ϊ60 g��ͨ��10 min����Һǡ�ñ�Ϊ��ɫ�������������缫������Ϊ4 g�����¶���CuSO4���ܽ������������ ��
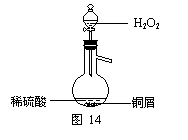 ��3��ijͬѧ��ѯ���ϵ�֪��ͭм����ϡ�����в�������Ӧ������ϡ�����м���H2O2��ͭм�����ܽ⡣ʵ��С��ͬѧ���ʵ��װ������ͼ����֤��ʵ�飬�÷�Ӧ�Ļ�ѧ����ʽ����������������������������������������������
��
��3��ijͬѧ��ѯ���ϵ�֪��ͭм����ϡ�����в�������Ӧ������ϡ�����м���H2O2��ͭм�����ܽ⡣ʵ��С��ͬѧ���ʵ��װ������ͼ����֤��ʵ�飬�÷�Ӧ�Ļ�ѧ����ʽ����������������������������������������������
��
����H2O2��ϡ���������ƿ�е�˳��ߵ���ʵ��õ��Ľ�����������������������������������������������
�������������������������������������������� ��
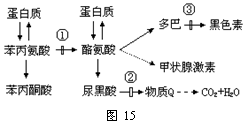 30.��20�֣�ͼ14ʾ�����ڱ����������Ұ���Ĵ�л;����ͼ�е����ֱַ��������ø��
30.��20�֣�ͼ14ʾ�����ڱ����������Ұ���Ĵ�л;����ͼ�е����ֱַ��������ø��
��1�������ڻ����е��Ұ����ͼ����ʾ����Դ�⣬�������������������� ��
��2����ø����n����������ɣ���ø�ٻ��������ӵļ����Ŀ���������������� ���ϳ�ø�ٵĹ�����������ȥ���������� ��ˮ���ӡ�
��3����ҽ������ij����ȱ��ø�٣���ϵķ����Ǽ����������������������������� ��
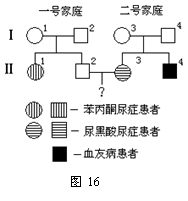 ��4��ͼ15��ʾ��-1��ȱ��ͼ15�е�ø�ٶ����б���ͪ��֢����-3��ȱ��ͼ15�е�ø�ڶ������������֢����-4���һ�Ѫ�Ѳ�������������״�ĵ�λ����ֱ���Pp��Aa��Hh��ʾ����һ�źͶ��ż�ͥ����Я���Է���ͥ���ֵ��Ŵ�������
��4��ͼ15��ʾ��-1��ȱ��ͼ15�е�ø�ٶ����б���ͪ��֢����-3��ȱ��ͼ15�е�ø�ڶ������������֢����-4���һ�Ѫ�Ѳ�������������״�ĵ�λ����ֱ���Pp��Aa��Hh��ʾ����һ�źͶ��ż�ͥ����Я���Է���ͥ���ֵ��Ŵ�������
�٢�-3�����漰����������״�Ļ������������� ��
�������Ŵ�ͼ�����ʽ������һ�ż�ͥ���������б���ͪ��֢���ӵ�ԭ��
�Ŵ�ͼ�⣺
��5����-3�Ѿ��������У�����Ԥ�⣬���������һ��Ů���������ĸ��������� ���������һ���к��������ĸ�������������
31.��22�֣�����ɫ���ˡ��DZ���������2008���������Ȩ�Ŀں�֮һ������ɫ���ĺ�����˰��������̻�����ɫ���ʽ�����������⣬��Ӧ����������Ȼ���䰮�����������˺�һ����̬�������µȡ�����ɫ��������Ҫ���Ǵ��Լ����𣬴����ߵ�С������
��1�������е��̵���������˾��̵�������������������ͬʱ�������ķDZ������֡����֡����롱�������������ı�������ȴ��������������Ϊ�������ֵ����ֿ��ܻ�����ĺ���� �������� _____________���������������Ӧ���������������������� ��������ϲ�ȡ����ս�Ժͱ�����ʩ��
��2��ijͬѧ�����һ��������ɫ���ʽ�������������״����������δ��ɵĵ���������������д����ȱ�����
| ������ɫ���ʽ������������״����� | |||
| ��� | ���� | ̬�� | |
| 1 | ����ˮ������ö��Ƚϱ��ˣ��ᳫ��Լ��ˮ���õ����岻�� | ��ͬ | ���� |
| 2 | ��������̫�鷳�ˣ�ʵ����Ҳû��ʲô���� | ��ͬ | ���� |
| 3 | �ִ���ᣬ���÷����ˣ��ᳫ�ڼ����Ѳ����ھ��õķ�չ | ��ͬ | ���� |
| 4 | ��ͬ | ���� | |
| 5 | ��ͬ | ���� | |
 |
��3������ʵ���DZ����ǷŴ��˵ط�����Դ��ʵ�������ġ�����������Դ��������������ɫ���е���Ҫ��־֮һ��ͼ16��������Դ������������һ�ַ������˷����Т١��ڹ�����Ҫÿһλ����IJ��룬���Dz�����ж���ʽ�� �������������������� ���ܡ��ݹ������õ�������������̬ϵͳ�ĺ��ֳɷ֣� ������������ ���Ӷ���Դ�ij�����ýǶȷ������ܡ���;���Ȣ�;�����ŵ��� ������������������������������������������ ��
| ��� ���� | 01 | 02 | 03 | 04 | 05 |
| ��� | 0.3 | 0.6 | 1.1 | 1.5 | 2.3 |
| ��� | 10.0 | 9.2 | 8 | 6.8 | 5.5 |
| ������ | 3.0 | 2.1 | 1.1 | 0.3 | 0.1 |
| ���� | 3.0 | 2.0 | 0.4 | 0 | 0 |
| ���� | 3.2 | 2��8 | 1.7 | 1.3 | 0.6 |
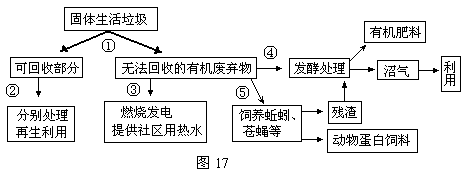
 ��4�������ԭ��������ֲ��仨���DZ���������Ҫ�Ĺ���Դ��ͼ17ʾ������������·�Ե�һƬ��ɢ�أ� ����С���ͬѧ�Դ˵ز���ֲ�����Ⱥ�ܶ���������������ĵ��飬������±���ʾ����λ���꣯m2����
��4�������ԭ��������ֲ��仨���DZ���������Ҫ�Ĺ���Դ��ͼ17ʾ������������·�Ե�һƬ��ɢ�أ� ����С���ͬѧ�Դ˵ز���ֲ�����Ⱥ�ܶ���������������ĵ��飬������±���ʾ����λ���꣯m2����
�ٵ���ȡ���Ĺؼ���Ӧ���������Ĵ�С�������⣬��Ӧע������������������ ��
�ں���Ȼ�������������б���ֲ��ʾ�����ϵ����������������������������� ��
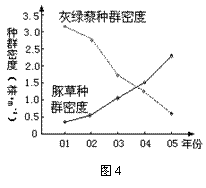
������ͼ18�л����ݺͻ�����Ⱥ�ܶȵı仯���ߡ�
 ����ݵĻ��ۿ�����ܶ��˺�����������Ӧ�������Ա��ס�֧������������ҽѧ����Ϊ��������Ӧ��ָ������������
����ݵĻ��ۿ�����ܶ��˺�����������Ӧ�������Ա��ס�֧������������ҽѧ����Ϊ��������Ӧ��ָ������������
������������������������������ �������ķ�Ӧ��
�����ۺ��������Բο���
�������21С�⣬ÿС��6�֣���126�֡�
һ��ѡ���⣺ѡ�Եĸ�6�֣�ѡ����δѡ�ĸ�0�֡�
1��D��2��B��3��D��4��D��5��A��6��C��7��B��8��B��9��A��10��D��11��C��12��B��13��C
����ѡ���⣺ȫ��ѡ�Եĵ�6�֣�ѡ�Ե���ȫ�ĵ�3�֣���ѡ���ĵ�0�֡�
14��B����15��BD�� �� 16��D����17��D����18��AD����19��B����20��B�� 21��C
�������10С�⣬��174�֡�
|
|
22����1���ڢۣ�6�֣���Ե���ȫ�ĵ�3�֣��д���IJ��÷֣�
��2������ͼ1��ʾ����������3�֣�
��A������������3�֣�
�� �ⷨһ��
A������·ͼ���õ�·�������������Ļ���ͷP����A�ˡ�
B���պϿ���S1��S2�����ڻ���������R2�Ļ���ͷP��ʹ��ѹ����ָ��ƫתһ���ϴ�ĽǶȣ������̶ȣ�������¼��ʱ��ѹ����ʾ��U1��
C������P��λ�ò��䣬�Ͽ�S2�����ڵ�����R1����ֵ��ʹ��ѹ����ʾ��ΪU2=U1/2�����ѹ�����ڵ�����ڴ�ʱ���������ֵR��
D���Ͽ�S1�������·��ʵ�����ĸ�ԭ��
�ⷨ����
A������·ͼ���õ�·�������������Ļ���ͷP����A�ˡ�
B�������������ֵ����ijһ����ֵ�����Ϊ3k�����ң��������´�ʱ�ĵ���ֵR���պϿ���S1��S2�����ڻ���������R2�Ļ���ͷP��ʹ��ѹ����ָ��ƫתһ���ϴ�ĽǶȣ������̶ȣ�������¼��ʱ��ѹ����ʾ��U1��
C������P��λ�ò��䣬�Ͽ�S2����¼��ʱ��ѹ����ʾ��U2�����ʱͨ��������ĵ���ΪI=��U1-U2��/R�����ݴ�����·�ĵ����ص��ŷķ���ɿ������ѹ�����ڵ���Ϊ��RV=U2/I= U2R/��U1-U2����
D���Ͽ�S1�������·��ʵ�����ĸ�ԭ��
˵������С������5�֡�����A��Bδ���ߣ��ɲ��۷֡�
23����16�֣��⣺��1��A��B������ײ���̶����غ㣬��
Mv0=MV+mv����������3�֣�
������֪M=3m��v = 1.2v0 �����V = 0.6 v0��������������1�֣�
������B����ײǰ���ٶȷ�����ͬ��������������1�֣�
��2��A���B���������Ĵ�С����B���ܵļ�������������������2�֣�
����A���B���������Ĵ�СΪ W=![]() Mv02-
Mv02-![]() MV2=0.96mv02��������������3�֣�
MV2=0.96mv02��������������3�֣�
��3����A��B�������ڶ�����ײ��λ�þ�ǽ��Ϊx����A����1.2v0���ٶ��˶��ľ���Ϊs+x��B����0.6 v0�˶��ľ���Ϊs �C x��A��B�����˶���ʱ����ȣ�����
![]() ��������������4�֣�
��������������4�֣�
����������ڶ�����ײ��λ�þ�ǽ�ڣ�![]() ����������������2�֣�
����������������2�֣�
24����19�֣���1���ں��������£���Ȧ��ʼ�������ȼ���ֱ���˶�������Ȧ�ļ��ٶ�Ϊa����ţ�ٵڶ������У�F-mg=ma����������������������������������2�֣���
���a=30m/s2����������������������������������������������1�֣�
����Ȧ����ų���ʼ�������˶����ٶ�Ϊv1����
cd�߲����ĸ�Ӧ�綯��ΪE=BLv1������������������������������1�֣�
�߿��в����ĸ�Ӧ����Ϊ I=E/R������������������������������1�֣�
�߿����ܵİ�����Ϊ F��=BIL����������������������������������1�֣�
���߿��������˶�������F=F��+mg����������������������������2�֣�
����������ʽ���ɽ��v1=��FR-mgR��/B2L2=24m/s��������������2�֣�
��v12=2aH���H=9.6m������������������������������������1�֣�
��2������F���Ĺ���W=F��H+L+h��=42.4J ������������������3�֣�
��cd�߽���ų���ab���뿪�ų��Ĺ����У����������Ĺ������߿����ӵ��������ܺͲ���������Q����
F��L+h��=mg��L+h��+Q����������������������������������3�֣�
��ã�Q=��F-mg����L+h��=3.0J ��������������������������2�֣�
��Q=I2Rt=��BLv/R��2R��h/v+L/v��=3.0J
25����20�֣���1������ǡ��λ��ԭ��O�������������������ܵĵ糡��������������С��ȣ������Ӵų��ĴŸ�Ӧǿ��ΪB���� qE=qv0B ��������������2�֣�
��á���B=E / v0 ����������1�֣�
|
|
�ɵ糡���Լ����ֶ����ж��ų�������ֱ���ϡ�����������2�֣�
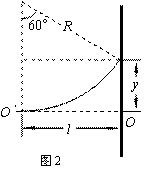
������2����OO������Ϊz����������x��y��ɿռ�ֱ������ϵ���ų��ı䷽���������yOzƽ���ڵ��˶�������Բ���˶����켣��ͼ2��ʾ����Բ�뾶ΪR�����ݼ��ι�ϵ��
����R2-l2=��R-y��2������������������4�֣�
����![]() ���ɽ��
���ɽ��![]() ����֪��=60�㡭��������4�֣�
����֪��=60�㡭��������4�֣�
������x����ķ��˶��dz���Ϊ����ȼ���ֱ���˶���ʱ��
����������������������
![]() ��������������3�֣�
��������������3�֣�
������������
![]() ����������4�֣�
����������4�֣�
26��
|
(2) 2KCl+2H2O====2KOH+ H2��+Cl2������������3�֣�
|
(3) Fe2O3 +2Al ==== 2Fe + Al2O3����������3�֣�
(4)Al2O3+2OH-===2AlO2-+H2O����������3�֣�
27����12�֣���1��Ba(OH)2��NH4NO3 H2SO4����������3�֣���9��
|
![]() ��2��4NH3+5O2=====4NO+6H2O��������3�֣�
��2��4NH3+5O2=====4NO+6H2O��������3�֣�
28����21�֣���1��186��C10H18O3����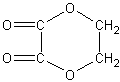 1����������3�֣���9��
1����������3�֣���9��
|
![]() ��2��HOOC��COOH+ OH CH2��CH2OH����������������������������
+2H2O����3�֣�
��2��HOOC��COOH+ OH CH2��CH2OH����������������������������
+2H2O����3�֣�
������Ӧ��������3�֣�
HOOC��COOH+2NaHCO3===NaOOC��COONa+ 2H2O+ 2CO2����������3�֣�
��3��HOCH2��(CH2) 6��CH=CH��COOH��������3�֣�
29����12�֣���1����ɫ�����ڣ���������Ũ������ȴ�ᾧ�����ˡ���������2�֣���4�֣�
��2��Cu2++2e-==Cu����20 g����������2�֣���4�֣�
��3��Cu��H2O2��H2SO4��CuSO4��2H2O����ͭм����H2O2�в�������Ӧ������H2O2�м���ϡ���ᣬͭм�����ܽ⡣����������2�֣���4�֣�
30.��20�֣�
 ��1��ʳ�������������������������2��
��1��ʳ�������������������������2��
��2��6n���� n-1�� ������������������4��
��3����������Һ���Ƿ��й���ı���ͪ��
����������������������������������2��
��4����PPAaXHXh�� ��������������2��
���Ŵ�ͼ�⣨��ͼ3�� ������������6��
ע����ȫ���ش���ȷ��3�֡����ݱ��������Ҫ��ѧ����ֻ�����Ӵ����ֱ���ͪ��֢���ߵ�ԭ�������ȷ����ȱ�����ӻ��ڵı���������ͼ�ⲻ�÷֡����״������͡������Ͳ���������ȷ��1�֡����Ӵ������͡������Ͳ���������ȷ��1�֡������������ŵı���ȱʧ���д������1�֡�
��5��1���� 0.75������������������4��
31.��22�֣�
��1��ʹ�������ֵ������ܵ���в�����������ֺ���̬ϵͳ����������������4��
��2��������������������������������������������������������������4��
��Ҫ����Ƶ�����Ӧ���ڡ���ɫ���ʽ����������ķ��룬�������ɡ�
��3���������������ദ�������ֽ��ߡ��������������л������е������⣬����ֵطֲ�Ρ��༶�������������е����ʡ���������������������������������������6��
 ��4�������ȡ������������������������2��
��4�������ȡ������������������������2��
�ڹ�ͬ����Դ�Ϳռ� ������������������������
����ݺͻ�������Ⱥ�ܶȵı仯���ߣ���ͼ4����������������������������������������2��
�������ߵĻ����ٴν�����ͬ���ʵĴ̼�����2��