南昌市高考理科综合试题汇编
物理、化学、生物学科
(共28题)
1. 下列各种对物质的解说正确的是( )
A. DNA和RNA分子中共有五种碱基,五种核苷酸
B. 丁香油酚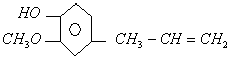 能和NaOH发生中和反应
能和NaOH发生中和反应
C. 氢原子的核外电子从距核较近的轨道跃达距核较远的轨道时,原子要吸收光子,电子的动能增大,原子的电势能增大
D. 金属氧化物都是碱性氧化物
2. 下列说法正确的是( )
A. 有些城市,夏季喷洒马路的水中常加入一些氯化钙
B. 用绿光照射一光电管,能产生光电效应,欲使光电子从阴极逸出时的最大初动能增大,应增大绿光的强度
C. 要除去![]() 溶液中的
溶液中的![]() 杂质,应通入足量的H2S气体,振荡、过滤
杂质,应通入足量的H2S气体,振荡、过滤
D. 人体内代谢产物CO2形成的场所是肺泡
3. 下列关于新陈代谢的叙述中错误的是( )
A. 新陈代谢过程是生物体自我更新的过程,因此,只存在物质变化,不涉及能量的转化
B. 新陈代谢过程遵循质量守恒定律
C. 新陈代谢过程遵循能量的转化与守恒定律
D. 新陈代谢过程中物质变化的同时,伴随着能量的转化
4. 下列说法中不正确的是( )
A. 在电场中将电荷由a点移到b点,如果电场力做功为零,则a、b两点场强大小一定相等
B. 人造卫星,在研究它绕地球转动时可以看成质点
C. 细胞的结构和生命活动的物质基础是水
D. ![]() 溶胶与硅酸溶胶混合将产生凝聚现象
溶胶与硅酸溶胶混合将产生凝聚现象
5. 人类只有一个地球,我们要保护赖以生存的环境。
(1)当今世界三大环境问题是( )
A. 酸雨 B. 臭氧层衰竭 C. 人口急剧增长 D. 温室效应
(2)酸雨的形成主要是由于( )
A. 大气中CO2含量增加 B. 大气中SO2含量增加
C. 乱砍滥伐森林,破坏生态平衡 D. 大气中氟利昂含量增加
(3)大气臭氧层( )
A. 能大量反射太阳辐射中的紫外线,所以那里的温度较低
B. 能散射太阳光的紫外线,使地面生物免受集中紫外线之害
C. 是大气层中存在臭氧的唯一场所,我们应该加以保护
D. 吸收大量紫外线,减少到达地面的紫外线辐射
6. 科学研究发现,萤火虫发光的原理是由于萤火虫体内含有荧光素和荧光酶两种物质,在荧光酶作用下,荧光素在细胞内氧化后发生荧光。科学家已能用化学方法人工合成荧光素和荧光酶而制成生物光源。
(1)与普通的电灯相比,这种生物光源更适合于在充满瓦斯的矿中当闪光灯及在清除磁性水雷时用以照明。试简述理由____________________________________________。
(2)与白炽灯、日光灯、生物光源三者相比,哪一种光源的发光效率最高?_______。哪一种光源使用过后对环境造成的负面影响最大?________________。
7. 某人从井中提水,已知水面离地面距离为10m,水(连桶)的质量共15kg,绳索重忽略不计。问:
(1)此人把水(连桶)从井底提上来做的功为__________。
(2)假设此人提水这一过程的效率为30%,所需能量全部来自体内葡萄糖的氧化分解,则此人完成提水这一过程需消耗葡萄糖的质量为________(答案保留两位有效数字)
8. 莫斯科时间2001年3月23日9点0分12秒,“和平”号空间站以超音速穿过大气层,经充分燃烧后,最终其残片完全落入南太平洋预定海域,这标志人类的航天技术已逐步走向成熟。
(1)“和平”号空间站主要构造材料可采用(填序号)__________。
A. 不锈钢 B. 铝钛合金 C. 铝 D. 硅锰合金
(2)“和平”号绕地球作匀速圆周运动,下列关于它的说法中正确的是(填序号)______。
A. 在轨道上的速度可能是5km/s
B. 在轨道上的向心加速度可能是![]()
C. 在轨道上的周期可能是1h
D. 在轨道上的角速度可能是![]()
(3)在飞船里,氧气靠液态氧气化补给,而舱内的二氧化碳则通常用水、氧化锂吸收处理,其反应方程式是_____________。
(4)1987年8月,我国返回式卫星上曾搭载水稻种子,返回后经地面种植,培育出的水稻穗粒大,![]() 产量达600kg~750kg,蛋白质含量增加8%~20%,生长周期平均缩短10天,这种育种方式叫_________,其优点是___________________________________。
产量达600kg~750kg,蛋白质含量增加8%~20%,生长周期平均缩短10天,这种育种方式叫_________,其优点是___________________________________。
(5)宇航员在太空中走出密封舱作业时,身穿宇航服并在其中呼吸压强为0.20atm的纯氧,在宇航服中的温度恒为![]() ,若宇航员在地球平原上(压强为1atm)呼吸着温度为
,若宇航员在地球平原上(压强为1atm)呼吸着温度为![]() 的空气,其中氧气占空气的21%,此时他每分钟需呼吸16次,那么宇航员在太空中身穿宇航服走出密封舱后,每分钟呼吸几次?(宇航员每次呼吸的肺活量相同)
的空气,其中氧气占空气的21%,此时他每分钟需呼吸16次,那么宇航员在太空中身穿宇航服走出密封舱后,每分钟呼吸几次?(宇航员每次呼吸的肺活量相同)
9. 汽车尾气使自然生态环境趋于恶化。治理的根本方法就是亟待开发替代燃料,目前较为理想的替代燃料是天然气(主要成分是甲烷)、醇类、氢气等。
(1)糖类物质可用![]() 表示,该类物质进行无氧分解可产生甲烷和另一种化合合物。这一反应的化学方程式为__________________________________________。
表示,该类物质进行无氧分解可产生甲烷和另一种化合合物。这一反应的化学方程式为__________________________________________。
(2)醇类燃料的来源和生产途径较多。有一种方法是用甜菜、甘蔗等含糖物质为原料制取乙醇。在缺氧条件下酵母菌将葡萄糖分解成酒精的化学方程式为________________
________________________________________。
(3)在标准状况下,11.2L氢气安全燃烧生成水蒸汽所放出的热能可使3.4kg水的温度由![]() 上升为
上升为![]() ,请依据上述说明写出氢气燃烧生成气态水的热化学方程式_____
,请依据上述说明写出氢气燃烧生成气态水的热化学方程式_____
______________________________。[水的比热为![]() ]
]
(4)有一种以氢气为燃料的汽车,重6t,阻力是车重的0.05倍。若此车以最大速率匀速行驶300km,发动机的效率为50%,则需要多少千克氢气作为燃料?(g取![]() )
)
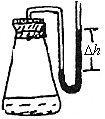
10. (1)向盛有100mL
0.1mol/L H2SO4的500mL锥形瓶中加入下列少量物质后,立即用带U型管的塞子塞紧。片刻后,U型管两侧水银柱出现的液面差为![]() (如图)。加入的物质可能是( )
(如图)。加入的物质可能是( )
(1)NaOH固体 (2)18mol/L
H2SO4 (3)![]() 固体 (4)
固体 (4)![]() 固体
固体
A. (1)(2)(3) B. (1)(2)(4) C. (1)(4) D. (2)(4)
(2)若投入的物质是![]() ,反应结束后
,反应结束后![]() ,则欲使U型管两侧的水银柱液面差恢复为零,至少应向锥型瓶中加入多少克NaOH固体?(假设反应前后的温度均为
,则欲使U型管两侧的水银柱液面差恢复为零,至少应向锥型瓶中加入多少克NaOH固体?(假设反应前后的温度均为![]() )
)
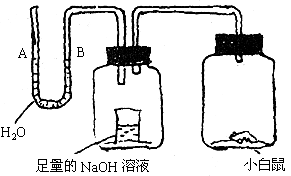
(3)请据图回答,经数小时后,U形管A、B两处的液面会出现下列_________情况(实验装置足以维持实验过程中小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响)
A. A处上升,B处下降 B. A、B两处都下降
C. A处下降,B处上升 D. A、B两处都不变
11. 铁元素可以形成两种阳离子、![]() ,两者具有不同的物理化学性质。
,两者具有不同的物理化学性质。
(1)试以化学方法将两者分开,写出反应方程式。
(2)运用带电粒子在电场中的受力及运动情况将两者分开。
(3)在人体红细胞内,关于![]() 的相互转变,叙述正确的是( )
的相互转变,叙述正确的是( )
(1)![]() ,表明血红蛋白与氧结合,静脉血变动脉血
,表明血红蛋白与氧结合,静脉血变动脉血
(2)![]() ,表明血红蛋白与氧分离,动脉血变静脉血
,表明血红蛋白与氧分离,动脉血变静脉血
(3)![]() ,表明血红蛋白与氧结合,静脉血变动脉血
,表明血红蛋白与氧结合,静脉血变动脉血
(4)![]() ,表明血红蛋白与氧分离,动脉血变静脉血
,表明血红蛋白与氧分离,动脉血变静脉血
A. (1)(2) B. (3)(4) C. (1)(4) D. (2)(3)
12. 夏天,水生绿藻(如水绵等)在夜里沉入水中,白天,特别是阳光灿烂的日子里浮上水面,请结合有关知识回答:
(1)白天绿藻浮上水面的原因是___________________________________。
(2)写出与绿藻上浮有直接关系的化学反应式____________________________。
(3)导致绿藻在夜里沉入水中的力是__________,水藻下沉需要克服的阻力是_______________________。
13. 如下图,将正在萌发的种子,放在内有一杯NaOH溶液而用塞子塞紧的瓶中,此瓶中与一个水银流体压力计相连接,由此压力计水银柱升高的高度可以测量出某种气体的消耗量,假设正在萌发的种子用完了瓶中所有气体,则水银柱会升高到76cm处(等于大气压)
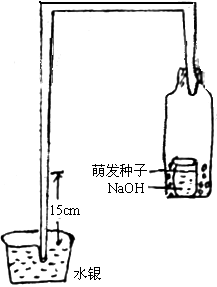
(1)实验过程中,水银柱只升高到15cm处,就不再升高,证明瓶中空气中的气体被利用了__________,而在空气中__________气约占__________,从而证明萌发的种子只利用了瓶中_________气。(2)此实验证明__________,瓶中NaOH溶液的作用是_________。(3)如果取消瓶中的NaOH溶液,再作此实验,水银柱的变化如何?______________原因是__________________________________________________________________。
14. (1)气缸内装有标准状况下的![]() 的混合气体22.4L,质量为27.2g,当外界气温升高
的混合气体22.4L,质量为27.2g,当外界气温升高![]() 时,需要在容器的轻活塞上加上多重的一块砝码?(轻活塞面积为
时,需要在容器的轻活塞上加上多重的一块砝码?(轻活塞面积为![]() )
)
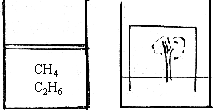
(2)标况下若将气缸内气体抽出,装入一个钟罩内,钟罩的容积为22.4升,使混合气体完全燃烧,写出反应方程式且求出需耗氧气多少摩尔?
(3)若在钟罩内原有一株绿色植物,混合气体燃烧时所耗氧气经测定有50%是植物通过光合作用提供,则植物生长过程中贮存了多少克![]() ?
?
15. 臭氧(O3)在大气中含量甚微,其浓度分布因海拔高度而异,浓度峰值在离地面20—25km高度处,臭氧在大气中竖直高度的总含量相当于标准压强和温度下0.3cm左右厚度的气体层。
(1)气压P随距地面高度Z的增大而减小,经验公式为![]() ,其中
,其中![]() 为地表的气压值,
为地表的气压值,![]() ,若臭氧层集中在24km的高空处,设在该高处温度为
,若臭氧层集中在24km的高空处,设在该高处温度为![]() ,试估算臭氧层的厚度。
,试估算臭氧层的厚度。
(2)臭氧层的存在对于地球生物至关重要,因为它能阻挡高能量紫外线辐射到地表。阳光中的紫外线对地球生命系统具有很大的伤害能力,能量越高,伤害越大。
(1)过量的紫外线照射萌发的种子,长成的植株有的果实很大,有的植株很高,有的植株很壮,但更多的植株会死亡,原因是___________________________。
(2)过量的紫外线能诱发皮肤癌,其变异的机理为___________________________。
A. 基因重组 B. 基因突变 C. 基因互换 D .染色体变异
(3)但适量照射紫外线对人体有益,特别对预防佝偻病有一定的作用,这是由于紫外线使表皮细胞内一种__________转变成维生素D,以促进小肠对________的吸收和利用,使骨正常发育。
(3)近些年来,发现大气臭氧层遭到严重破坏,1985年英国科学家首先发现南极臭氧层已出现空洞,臭氧层被破坏主要原因是人造化工制品氯氟烃(氟里昂)和哈龙的污染,人类大量制造的这些人工合成的化合物,主要应用于___________________________。
(4)氯氟烃气体一经释放就会慢慢上升到地球大气圈的臭氧层的顶部,在那里,紫外线会把氯氟烃气体上的氯原子分解出来,氯原子再把臭氧中的一个氧原子夺去,使臭氧变为氧气,从而起到减小臭氧的作用,这个过程主要包括了三个化学方程式,请补充化学方程式(2)。
(1)![]()
(2)____________________________________
(3)![]()
16. 目前,科学家们已掌握了一定的技术来利用太阳能、水能、潮汐能以及生物能等。
地球上的绿色植物可以通过叶绿体进行光合作用,将太阳能转化为化学能储存在有机物里。实验证明,每摩尔葡萄糖彻底氧化分解可以释放2870kJ的热量,其中有1225kJ的能量储存在ATP中,其余的能量都以热能的形式散失了。
(1)请写出光合作用总过程的化学反应方程式。为什么说绿色植物被称之为“自动的空气清新剂”?它对人类生存环境有何重大影响?
(2)一片植物在光合作用中“消化”了44kg CO2,试计算此过程有多少太阳能参与了转化?生成的氧气可供一个人呼吸多久?(一个人呼吸的耗氧率为![]() )
)
(3)我国水能资源丰富,利用水位落差可将水的势能转化为电能,供生活、生产使用。在一个小型水电站里,水位落差为3m,每秒有0.5m3的水流过水轮机,流出速度为3m/s(上游水的流速忽略)。设水流能的70%可转化为电能,求电功率。
17. (可能用到的相对原子质量:C 12 N 14 O 16)
目前已发现的一百一十多种元素中,许多元素都存在同位素。同位素在生产、生活和科研中有着十分广泛的用途,如测定矿石和生物遗体的年代、研究反应机理、优良育种、临床治癌、核动力发电等。
(1)物质的量的单位——摩尔是以__________所含的碳原子个数为标准。有机化学中研究酯化反应机理时用__________原子做示踪原子。
(2)14C具有放射性,其半衰期为5686年,空气中12C与14C的存量比约为1012:1.2,活着的生物体内碳的这种同位素的存量与空气中相同。生物死亡后,不再吸收碳。如果测得某古代生物遗骸中,12C与14C的存量比约为1012:0.3,估算该遗骸为_______年前的生物遗留下来的。
(3)如图所示是科学家希尔(R·Hill)用同位素18O研究光反应过程的示意图。甲、乙两试管中为小球藻悬液,现都予以光照,结果在甲中产生的气体为O2,乙中产生的气体为![]() 。
。
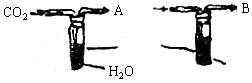
(1)要测定该装置是否进行了光反应,最简单的方法是测定是否产生了___________。
(2)小球藻的新陈代谢类型为__________,其进行光合作用所吸收的光谱是_________。
(3)该实验证明_________________________________________________________。
(4)要验证A为O2,B为18O2,除可以检测放射性外,还可以采用定量的方法。此定量的说法必须测得标准状态下的基本物理量是_______,由该基本物理量求得气体的_________,从而得到验证。如果产生的气体中混有二氧化碳,会使得测定结果_________。(填“偏大”、“偏小”或“不变”)
18. 有A、B、C三个水样,它们是经过如下的前处理获得的:(1)从泛着绿色的池塘取水静置4小时,倒去上层清液,留下藻类。再加入清水,静置4小时,然后倒去上层清液,留下藻类,如此重复3次,最后加水至900mL。(2)将900mL藻液搅拌均匀,分别倒入3个300mL烧杯中继续培养,A烧杯中加入0.3g含磷洗衣粉和0.3g尿素;B烧杯中加入0.3g尿素;C烧杯中不加其它物质。(3)在向阳的窗台上培养5天,得到水样A、B、C。根据上述前处理过程回答:
(1)前处理中第一步的目的是什么?
(2)检测结果表明A水样中藻类生长得最好,能说明什么问题?
(3)若池塘中缺少碘元素,生活在其中的蝌蚪迟迟不能长大成蛙,出现这种现象的原因是什么?
(4)假如此池塘被轻度污染,该地居民欲将池塘中的污水变为饮用水,在下列处理过程中(1)用明矾化学沉降(2)用漂白粉消毒杀菌(3)自然沉降(4)烧开煮沸,其合理顺序为____________。
(5)试用离子方程式及简单的文字说明表示明矾净水的原理____________________
______________________________________________________。
19. (1)人体有一个稳定的内环境,包括人体中水分的含量占体重的60%~70%,体液维持在一定的pH范围内,如血液的pH范围维持在7.35~7.45之间,请回答:
(1)人体内水的存在形式有_____________________________________________两种,其中___________________________________________________________对内环境的稳定有十分重要的意义,原因是____________________________________。
(2)血液的pH范围维持在7.35~7.45之间,对内环境的稳定有什么生理意义?答:_________________________________________________-
(2)高血压是危害健康的一种常见病,现已查明,血管内径变细是其诱因之一。我们可在简化假设下研究这一问题:设液体通过一根一定长度的管子时受到的阻力f与流速v成正比,即f=kv(为简便,设k与管子粗细无关);为维持液体匀速流时,在这段管子两端需有一定的压强差。设血管截面积为S时两端所需压强差为p,若血管截面积减小10%时,为了维持在相同时间内流过同样多的液体,压强差必须变为多大?
20. 在绿色植物光合作用中,每放出1个氧分子要吸收8个波长为![]() 的光子,同时每放出1mol O2,植物贮存469kJ的能量。绿色植物能量转换效率为(普朗克常数值:
的光子,同时每放出1mol O2,植物贮存469kJ的能量。绿色植物能量转换效率为(普朗克常数值:![]() )________________________________。
)________________________________。
21. 使用下图装置,可测定植物的光合作用,开始时装置左右两侧的液面在同一水平面上,即瓶内气压等于大气压,请回答:
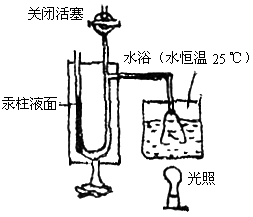
(1)用![]() 水浴的意义是________________。
水浴的意义是________________。
(2)为了保证水草的光合作用速度,可在三角烧瓶内加入碳酸缓冲液,其目的是__________________________。
(3)光照一定时间,装置左侧的液柱与右侧液柱相比,其变化是__________,原因是_____________________________。
(4)撤掉光源,把装置放在暗室里一定时间后,左侧液柱与右侧液柱相比,其变化是______________,原因是_______________________。
(5)用这种装置测定的光合作用速率与真实的光合作用速率是否一致?为什么?
答:________________________________________________
22. 用功率为10W的白光做恩格曼实验,经棱镜色散后,照射在丝状绿藻上,结果发现被类胡萝卜素所吸收的能量占白光总能量的0.663%,查高中物理课本得各色光在真空中的频率范围见下表:(在空气中数值极接近真空中数值)
| 光的颜色 | 频率(1014Hz) | 光的颜色 | 频率(1014Hz) | 光的颜色 | 频率(1014Hz) |
| 红 | 3.9~4.8 | 黄 | 5.0~5.2 | 蓝—靛 | 6.1~6.7 |
| 橙 | 4.8~5.0 | 绿 | 5.2~6.1 | 紫 | 6.7~7.5 |
普郎克常数![]()
求:(1)粗略计算类胡萝卜素在1秒钟内吸收多少个光子?
(2)写出光合作用过程的总反应式。
23. 根据国家环保局的统一规定,目前进行大气监测的项目是:二氧化硫、氮氧化合物、悬浮颗粒物等三种大气污染物。
(1)简述由城市环保局和气象局公布的城市空气质量预报对有关部门和普通市民有什么指导意义?
(2)二氧化硫是污染大气的主要有害物质之一。
(1)“酸雨”的形成主要是由于( )
A. 森林遭到乱砍滥伐,破坏了生态平衡
B. 工业上大量燃烧含硫燃料
C. 汽车排出大量的尾气
D. 大气中二氧化碳含量增多
(2)在下列情况中可能引起大气污染的是( )
<1>煤的燃烧 <2>工业废气任意排放
<3>燃放鞭炮 <4>飞机、汽车尾气的排放
A. 只有<1><2> B. 只有<2><4>
C. 只有<1><2><3> D. <1><2><3><4>
(3)二氧化硫是工业制硫酸中的必要物质,我国目前多用燃烧黄铁矿(FeS2)的方法来制取二氧化硫,这个反应常在_________炉内进行,其化学反应方程式是______________。
(4)工业制硫酸的废气中含有二氧化硫。废气排入大气之前必须经过回收、净化处理,通常将废气通入过量的氨水中,然后在所得的溶液中加入硫酸得到较纯净的二氧化硫,其化学反应方程式为___________________________________________________。
(3)一氧化氮也是常见的大气污染物质,它可以和人体血液内的血红蛋白结合,其亲和力比一氧化碳与血红蛋白的亲和力大数百倍。
(1)由此回答一氧化氮是如何影响人体呼吸过程的。
(2)目前治理一氧化氮污染的方法之一:是在![]() 左右、有催化剂存在的情况下,用氨把一氧化氮还原为氮气和水,其化学反应方程式为______________________________。
左右、有催化剂存在的情况下,用氨把一氧化氮还原为氮气和水,其化学反应方程式为______________________________。
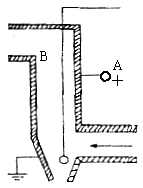
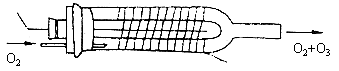
(4)静电除尘是治理悬浮颗粒污染的方法之一,其依据是物理原理是让带电的物质微粒在________的作用下,奔向并吸附到__________上。下图为静电除尘器的示意图,除尘器由金属A和悬在管中的金属丝B组成,A接________,B接_________。A、B之间有很强的电场,而且距B越近电场越强。B附近的空气分子被强电场电离为电子和正离子,正离子跑到B上得到电子又变成________,电子在奔向正极A的过程中,遇到烟气中的悬浮颗粒,使悬浮颗粒带_______,吸附到A上,排出的气体就较为清洁了。
24. 某城市的管道煤气是水煤气和焦炉煤气混合而成。某住宅的四楼(高约10m)一居民家厨房发生管道煤气泄漏爆炸事故,急救人员迅速赶到现场,护送伤员及煤气中毒者去医院抢救。
(1)生产水煤气的化学反应方程式是______________________________。
(2)管道煤气致人中毒的主要原因是什么?
(3)调查人员发现该住户的煤气泄漏点的煤气泄漏速度为6.0g/min,而从调查中发现气是在达到室内空气质量的6%时爆炸的,问爆炸时煤气已泄漏了几个小时。(假定厨房内空气体积为25m3,空气密度![]() )
)
(4)爆炸时厨房温度可迅速升高到![]() ,估算此时产生的气体压强约为常压的多少倍?
,估算此时产生的气体压强约为常压的多少倍?
(5)产生的高压可摧毁门窗及其他室内设施,调查人员在损坏的窗外草地上发现飞得最远的玻璃片离楼墙角的距离为14m。试估算气体爆炸初期的速度。(经验表明该速度约为玻璃碎片飞出时最大速度的100倍)
25. 三磷酸腺苷又叫ATP,含有2个高能磷酸键(用~表示)和1个低能磷酸键,其结构为

(1)ATP的分子式是___________,其摩尔质量为_____________。
(2)每摩高能磷酸键水解时可释放30514J的能量,而每摩低能磷酸键水解时却只能释放14212J的能量。50.7g的ATP发生水解时释放出的能量为__________kJ。若将此量的ATP加入到![]() 的NaOH溶液中,则需消耗此NaOH溶液__________L。
的NaOH溶液中,则需消耗此NaOH溶液__________L。
(3)人的体温一般要保持在![]() ,低于此温度则要“打寒颤”,并靠消耗葡萄糖释放出的能量来维持体温,与此同时有一部分能量转化为ATP。已知
,低于此温度则要“打寒颤”,并靠消耗葡萄糖释放出的能量来维持体温,与此同时有一部分能量转化为ATP。已知![]() ,若形成1mol ATP需消耗10.7g葡萄糖,则“打寒颤”时会有___________%的能量转化成热量。
,若形成1mol ATP需消耗10.7g葡萄糖,则“打寒颤”时会有___________%的能量转化成热量。
(4)假设人在剧烈运动的瞬间其能量全部由ATP提供,则某身高1.8m、体重为60kg的运动员由静止用4s助跑完30m路程后跳过2.4m高的横杠(设运动员的重心在1.3m处)时他体内消耗的ATP为多少克?
26. 在生命起源的早期,紫外线是促进无机小分子物质形成有机小分子物质的主要能源,但是在生命大分子物质产生后,它却成了一个破坏因素,能使生命大分子物质分解。因为水对太阳紫外线辐射能起到削弱作用,所以原始生命最早诞生于原始海洋。有了臭氧层之后,紫外线不能对地球直接辐射,这样就保护了生命不被破坏,使生命能进一步发展。臭氧层吸收紫外线的原理是![]() ,
,![]() 。
。
臭氧很不稳定,但常温下分解较慢,437K以上迅速分解:![]() ,
,![]() 。
。
请回答下列问题:
(1)生命大分子物质主要指哪些物质?
(2)紫外线产生的机理是什么?紫外线有哪些性质?
(3)下图是某家用消毒柜的臭气发生器,其工作电压5500V、电流强度0.004A,消毒柜体积为0.06m3,工作30min时产生臭氧,15min静止消毒。若电能的1%转化为化学能,求静止消毒时O3的体积百分比(工作条件下气体的摩尔体积为30L/mol)。
(4)传统的消毒剂氯气由于与水中的微量有机物产生致病作用的物质氯代烃或氯代含氧衍生物,臭氧是一种良好的替代物,参考次氯酸的消毒原理,解释臭氧为什么能消毒?
(5)平流层中的臭氧层保护了地球上的生物,而对流层中的O3浓度过高对环境有害,臭氧的检测可使用湿润的淀粉KI试纸,若反应产物中有氧气,其化学方程式___________
_____________________________。
(6)假设地球上空的臭氧层突然完全消失,地球上的生物界将变成何种状况?
27. 1956年李政道和杨振宁提出在弱相互作用中宇称不守恒,并由吴健雄用![]() 放射源进行实验验证,次年,李、杨二人为此获得诺贝尔物理奖。
放射源进行实验验证,次年,李、杨二人为此获得诺贝尔物理奖。![]() 的衰变方程是
的衰变方程是
![]()
其中![]() 是反中微子,它的电荷为零,静止质量可认为是零。
是反中微子,它的电荷为零,静止质量可认为是零。
(1)Co与Fe同周期,它应在周期表的第_________周期,![]() 的核外电子数为___________。在上述衰变方程中,衰变产物
的核外电子数为___________。在上述衰变方程中,衰变产物![]() 的质量数A是________,核电荷数Z是_________。
的质量数A是________,核电荷数Z是_________。
(2)在衰变前![]() 核静止,根据云室照片可以看出,衰变产物Ni和
核静止,根据云室照片可以看出,衰变产物Ni和![]() 的运动径迹不在一条直线上,如果认为衰变产物只有Ni和
的运动径迹不在一条直线上,如果认为衰变产物只有Ni和![]() ,那么衰变过程将违背__________守恒定律。
,那么衰变过程将违背__________守恒定律。
(3)无水CoCl2为深蓝色,吸水后变为粉红色的水合物,水合物受热后又变成无水CoCl2,故常在实验室中用作吸湿剂和空气湿度指示剂。
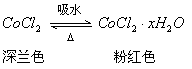
现有![]() ,吸水后变成
,吸水后变成![]() ,水合物中x的值是________。
,水合物中x的值是________。
(4)![]() 是典型的
是典型的![]() 放射源,可用于作物诱变育种,我国应用该方法培育出了许多农作物新品种,如棉花高产品种“鲁棉1号”,年种植面积曾达到3000多万亩,在我国自己培育的棉花品种中栽培面积最大。
放射源,可用于作物诱变育种,我国应用该方法培育出了许多农作物新品种,如棉花高产品种“鲁棉1号”,年种植面积曾达到3000多万亩,在我国自己培育的棉花品种中栽培面积最大。![]() 射线处理作物后主要引起__________,从而产生可遗传的变异,除
射线处理作物后主要引起__________,从而产生可遗传的变异,除![]() 射线外,用于人工诱变的其它射线还有________、________和_______。
射线外,用于人工诱变的其它射线还有________、________和_______。
28. 要搞好生态环境保护和建设,应大力开展植树种草,治理水土流失,防治沙漠化等。
(1)从生态因素分析,改善西部地区生态环境必须首先解决的非生物因素是_______。
(2)“退耕还林还草”的生态学原理是为了提高生态系统的___________。保护环境、生态平衡的关键是保护__________。
(3)近年北京等地频繁出现的“沙尘暴”、“泥雨”主要来自黄土高原和内蒙古地区,这说明森林等植被在_________等方面起着非常重要的作用。
(4)西部耕地同样要做好除草、治虫等工作,从能量流动的角度看,除草、治虫的目的是_________________。治虫措施中不宜大量喷施化学杀虫剂,控制使用化学杀虫剂的方法一是用生物杀虫剂,二是采用基因工程的手段,将___________转入农作物,形成新的抗虫作物品种。
(5)矿产的开发,可采用细菌冶金的方法,例如人们利用氧化亚铁硫杆菌能将FeS2氧化成H2SO4和Fe2(SO4)3的原理,将CuS溶于Fe2(SO4)3溶液中,并有淡黄色沉淀生成,再加入铁屑或废铁置换出铜。用化学方程式表示上述细菌冶金过程如下,填写空白:
(1)![]()
(2)![]()
(3)___________________________
(4)___________________________
(6)水能是可再生能源,可持续地利用它来发电,我国有丰富的水能,若一水利发电站水库的平均流量为![]() ,落差h(m),发电率为
,落差h(m),发电率为![]() ,则全年发电量为_______度。
,则全年发电量为_______度。
【参考答案】
(物理、化学、生物学科答案)
(共28题)
1. 答案:B
2. 解析:氯化钙晶体具有吸湿性,可保持地面不致太干燥而尘扬,所以A正确。
在满足光电效应的前提下,光电子的最大初动能只随着入射光频率的增大而增大,而与光的强度无关,光的强度只是决定逸出光子的数目,所以B错误。
FeCl3与H2S可以发生氧化还原反应
![]()
由于FeS溶于HCl,所以![]() 不会与过量的H2S发生反应。最后过滤掉的是S,只有FeCl2剩下,符合原意,所以C正确。
不会与过量的H2S发生反应。最后过滤掉的是S,只有FeCl2剩下,符合原意,所以C正确。
CO2是能源物质彻底氧化的产物,是在有氧呼吸的第二个阶段形成的,而有氧呼吸的第二、三阶段是在线粒体内完成的,所以D错误。
答案:A、C
3. 解析:本题是一道难度较大的综合性试题。它所涉及的知识点是自然科学中十分重要的内容,也是要求较高的内容。如能的转化与守恒定律、质量守恒定律、新陈代谢的概念及过程等等,都是自然界物质运动的一些重要规律或重要现象。
我们知道,自然界的任何物质运动都必须遵循能量的转化和守恒、质量守恒定律,生命运动也不例外,因此B和C两选项都是正确的,在物质变化过程中,必然伴随着能量的转化,新陈代谢过程中,也不例外,因此D正确。同化作用过程中,生物摄取外界的营养物质,通过变化,转变成自身组成物质,同时贮存能量;在异化作用过程中,有机物分解,同时释放能量。因此,选项A是不正确的。
答案:A
4. 解析:电场中电势与场强没有直接联系,电场做功为零,因为![]() 只能说明
只能说明![]() ,即a、b两点电势相等,至于场强则无法判断,所以A错。
,即a、b两点电势相等,至于场强则无法判断,所以A错。
物体是否可被看作质点与物体本身的体积大小无关,关键是看物体的体积在整个过程中是否占主导地位,人造卫星相对地球来讲很小,而且其体积也不影响它的运动,所以可以看作质点,所以B对。
构成细胞的物质基础是各种化合物,所以C错。
Fe(OH)3胶体颗粒带正电,硅酸胶体颗粒带负电,可以发生凝聚作用。所以D对。
答案:AC
5. 解析:(1)当今世界三大环境问题是酸雨、臭氧层衰竭、温室效应,故答案选A、B、D。
(2)酸雨的形成主要是由于化学工业排放SO2,使土壤酸化。答案选B。
(3)大气臭氧层主要是吸收太阳辐射的大量紫外线,减少到达地面的紫外线。答案选D。
6. 解析:(1)瓦斯在空气中受热即可爆炸,磁性鱼雷怕磁场,故这种生物光源之所以更适合在这两种情况下照明,因为其无热效应和磁效应。故答案为:生物光源无热效应和磁效应。
(2)联系已学过的白炽灯、日光灯发光原理,结合题给生物光源的发光原理进行推理比较,即可得出答案:生物光源;日光灯
7. 答案:(1)1500(J)(2)![]()
8. 解析:(1)B(2)A
(3)![]()
或![]()
(4)诱变育种,可以提高变异频率,使后代变异性状较快稳定,因而能加速育种进程,还可以大幅度改良某些性状。
(5)设宇航员每次呼吸的肺活量为V,在太空中每分钟呼吸n次。

9. 解析:
(1)![]()
(2)![]()
(3)0.5mol![]() 燃烧释放出的能量
燃烧释放出的能量![]() ,该反应的热化学方程式为
,该反应的热化学方程式为![]()
(4)当汽车以最大速率匀速行驶时,牵引力等于汽车所受阻力,即![]() ,行驶300km时汽车牵引力做的功
,行驶300km时汽车牵引力做的功
![]() ,此时汽车发动机所做的总功
,此时汽车发动机所做的总功
![]() 。
。
又每摩H2燃烧放出的热量为285.6kJ,据能量守恒(能量转化)可知,发动机作功需H2的质量![]() 。
。
10. 解析:
(1)当加入选项物质后,U型管右侧水银柱的液面高于左侧,说明锥形瓶内的气压大于瓶外的气压,产生这一结果的原因有二:一是选项物质(如![]() )与稀
)与稀![]() 反应时生成了不溶于水的气体;二是选项物质在反应或溶解过程中放出了热量,使瓶内的气压增大,如NaOH(反应时放出热量)、浓
反应时生成了不溶于水的气体;二是选项物质在反应或溶解过程中放出了热量,使瓶内的气压增大,如NaOH(反应时放出热量)、浓![]() (溶解时放出热量)。据上可断定(B)为正确答案。
(溶解时放出热量)。据上可断定(B)为正确答案。
(2)因题设反应前后温度不变,故根据物理学中气压知识可知U型管两侧水银柱的液面差![]() 是由
是由![]() 与
与![]() 反应产生的CO2造成的。当气压差为1atm时,可使U型管两侧水银柱产生76cm的液面差,现
反应产生的CO2造成的。当气压差为1atm时,可使U型管两侧水银柱产生76cm的液面差,现![]() ,瓶中CO2的压强
,瓶中CO2的压强![]() ,
,
![]() 。
。
欲使U型管两侧水银柱液面差恢复为零,就必须除去瓶内的CO2。因瓶内溶液中剩余的H2SO4的物质的量![]() ,故应加入的NaOH的物质的量
,故应加入的NaOH的物质的量![]() ,即
,即![]() 。
。
解本题时若审题不仔细,很容易发生以下错解:加入的NaOH物质的量![]() ,
,
![]() 。造成如此错解的原因是忽略了“至少”这一关键词的含义。在“至少”一词的限定条件下,NaOH与CO2发生的反应应为
。造成如此错解的原因是忽略了“至少”这一关键词的含义。在“至少”一词的限定条件下,NaOH与CO2发生的反应应为![]() ,而不是
,而不是![]() 。
。
(3)题中因小白鼠要进行呼吸,消耗瓶内的O2,虽然呼出了CO2气体,但CO2又被小烧杯内的NaOH溶液吸收,造成瓶内压强减小,导致U管内液面A处下降,B处上升。
(1)B(2)0.736g(3)C
11. 解析:
(1)用化学方法区分![]() 的方法很多,例如用NaOH或
的方法很多,例如用NaOH或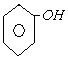 都行。现用NaOH来区分,离子方程式为:
都行。现用NaOH来区分,离子方程式为:
![]() 红褐色沉淀。
红褐色沉淀。
![]() 乳白色沉淀先变成黄绿色暴露在空气中一段时间变成红褐色。
乳白色沉淀先变成黄绿色暴露在空气中一段时间变成红褐色。
(2)以相同的速度垂直于电场方向射入。
(3)Fe是构成血红蛋白的必需元素,血红蛋白与氧结合,![]() 被氧化成
被氧化成![]() ,血红蛋白与氧分离
,血红蛋白与氧分离![]() 还原成
还原成![]() ,故选C。
,故选C。
12. (1)绿藻光合作用产生氧气,使绿藻比重减小,浮上水面
(2)![]()
(3)重力;水的浮力及摩擦阻力
13. 解析:若萌发的种子用完了瓶中的所有气体,水银柱则升高76cm,但现水银柱只升高了15cm,则瓶中的气体减少了![]() 。从空气的成分看(按体积计算)大约是氮气78%,氧气21%,其它气体和杂质1%,可见瓶中减少的气体最可能是氧气,从而证明萌发的种子只利用了瓶中的氧气。种子萌发时消耗氧气进行有氧呼吸,其反应式为
。从空气的成分看(按体积计算)大约是氮气78%,氧气21%,其它气体和杂质1%,可见瓶中减少的气体最可能是氧气,从而证明萌发的种子只利用了瓶中的氧气。种子萌发时消耗氧气进行有氧呼吸,其反应式为![]() 能量,从反应式可看出,种子萌发进行有氧呼吸,其吸收的O2量和放出的CO2量相等。在正常的密闭瓶内空气总量不变,压力也不变,水银柱不升高也不降低。但由于瓶内放了一杯NaOH溶液,NaOH可与空气中的CO2反应生成Na2CO3和H2O,从而起到了吸收CO2的作用,使瓶中的气体总量减少,压力减小,水银柱升高。
能量,从反应式可看出,种子萌发进行有氧呼吸,其吸收的O2量和放出的CO2量相等。在正常的密闭瓶内空气总量不变,压力也不变,水银柱不升高也不降低。但由于瓶内放了一杯NaOH溶液,NaOH可与空气中的CO2反应生成Na2CO3和H2O,从而起到了吸收CO2的作用,使瓶中的气体总量减少,压力减小,水银柱升高。
(1)20%,氧气,21%,氧气
(2)萌发的种子进行的是有氧呼吸 吸收CO2
(3)不升高也不降低,瓶中空气总的体积未变,压力不变
14. 解析:
(1)设气缸内CH4体积为V1,C2H6体积为V2,则有V1+V2=22.4L
![]()
得![]()
CH2有0.2mol
C2H6有0.8mol ![]()
解得![]()
(2)![]() ,耗O2有0.4mol
,耗O2有0.4mol
![]() 耗O2
耗O2
![]() ,故耗O2 3.2mol,罩内水面下降
,故耗O2 3.2mol,罩内水面下降
(3)![]()
1 6
x
![]()
![]()
15. 解析:
(1)标准状态1atm,273K
由![]() 可得Z=24km高空处的气压
可得Z=24km高空处的气压![]()
![]() 据气态方程
据气态方程![]() ,D为气体厚度,代入数据:
,D为气体厚度,代入数据:
![]()
(2)(1)一定剂量的紫外线能引发基因突变,大部分基因突变是有害的
(2)B
(3)胆固醇 Ca、P
(3)泡沫塑料、护发摩丝、灭火剂、杀虫剂、制冷剂
(4)![]()
16. 解析:
(1)![]() 。绿色植物广泛分布在地球上,不断地进行光合作用,吸收二氧化碳放出氧气,供生物呼吸,也使大气中氧气和二氧化碳含量基本保持稳定,因此被称为“自动空气清新剂”。绿色植物对人类生态环境的影响是:(1)保持大气中O2和CO2含量的相对稳定;(2)控制水土流失;(3)维持生态平衡。
。绿色植物广泛分布在地球上,不断地进行光合作用,吸收二氧化碳放出氧气,供生物呼吸,也使大气中氧气和二氧化碳含量基本保持稳定,因此被称为“自动空气清新剂”。绿色植物对人类生态环境的影响是:(1)保持大气中O2和CO2含量的相对稳定;(2)控制水土流失;(3)维持生态平衡。
(2)设44kg CO2可生成x mol C6H12O6,yg O2,则依
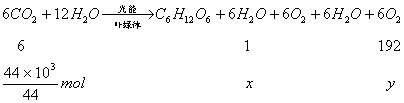
可解得![]()
![]()
![]()
可供一个人呼吸![]()
(3)算出1秒钟内所产生的电能即得到电功率,0.5m3水的质量![]() ,
,
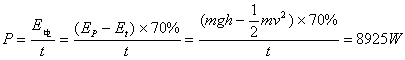
17. 解析:(1)0.012kg12C 18O (2)11372
(3)(1)氧气 (2)自养、需氧型 红光、蓝紫光
(3)光合作用中产生的氧来自于水的光解
(4)气体的质量与体积 摩尔质量 偏大
18. 解析:
(1)使水质富营养化,以便进行后面的实验
(2)磷是藻类生长繁殖的重要元素,也是水质富营养化的原因之一
(3)缺少甲状腺激素(其成分中含有碘元素)直接影响动物的个体发育
(4)(3)(1)(2)(4)
(5)![]()
![]() 胶粒可吸附水中的悬浮颗粒,并使其沉降,达到净水的目的。
胶粒可吸附水中的悬浮颗粒,并使其沉降,达到净水的目的。
19. 解析:
(1)(1)自由水和结合水 自由水 因为自由水是细胞内的良好溶剂,是运输养料和代谢废物的载体
(2)血液的pH范围维持在7.35~7.45之间,正好保证了酶的最适酸碱度(适宜条件),这样才能使新陈代谢正常运行,从而保证了人体正常的生命活动。
(2)据题意,设面积变为![]() 时,速度为
时,速度为![]() ,应有
,应有![]() ,即
,即![]() 。(1)
。(1)
设这时所需压强差为![]() ,则
,则![]()
又知原来压强差为P时有PS=kv
(3)联立(1)~(3)求解,得![]()
(4)代入数据可得![]()
20. 解析:根据能量公式:![]() 放出1mol O2的总能量为:
放出1mol O2的总能量为:
![]()
所以![]()
21. 解析:
(1)25℃为植物光合作用的适宜温度,保证光合作用中酶的催化效率
(2)及时补充二氧化碳保证光合作用速率
(3)左高右低;光合作用产生氧气,使瓶内气压升高
(4)左低右高 呼吸作用消耗氧气,释放CO2,被缓冲液吸收,瓶内气压降低
(5)不一致 两者相差呼吸速率
22. 解析:由于丝状绿藻中,除了叶绿素主要吸收红光和蓝紫光外,还有类胡萝卜素主要吸收蓝紫光,从表中可查得其频率![]() ,便可估算出光子数。
,便可估算出光子数。
(1)由于类胡萝卜素主要吸收的是蓝紫光,查得频率为![]() ,设在1秒钟有n个蓝紫光被类胡萝卜素吸收,据光子法则有:
,设在1秒钟有n个蓝紫光被类胡萝卜素吸收,据光子法则有:![]()
得:![]() 个
个
(2)光合作用过程总反应式:
![]()
23. 解析:
(1)有利于政府和市民培养环保意识,为政府有关部门决策提供科学的依据,为市民正常的日常活动提供科学的信息和指导。
(2)(1)B
(2)D (3)沸腾 ![]()
(4)![]()
![]()
(3)(1)答:NO与血红蛋白结合后,极大地影响了血红蛋白与O2的结合。
(2)![]()
(4)电场力 电极 高压电源正极 高压电源负极 空气分子 负电
24. 解析:这是道理,化、生综合性的题目落点是与生活联系很密切的一氧化碳与人体中毒的有关知识,同时应用物理求解气体泄漏的时间,煤气爆炸时的压强及产生压强气体的初速度。
(1)![]()
(2)CO与血红蛋白结合造成人体中毒
(3)![]()
![]()
(4)设为理想气体的等容变化
![]() ,即
,即![]()
(5)由平抛规律:![]()
得![]()
25. 解析:
(1)![]()
(2)放出的能量为
![]()
因1mol ATP水解可生成3mol磷酸,故![]()
(3)因形成1mol ATP时需吸收75.24kJ的能量,10.75g葡萄糖氧化时可释放出的能量为![]() ,故转化为热量的百分数为
,故转化为热量的百分数为![]() 。
。
(4)![]() ,
,![]() 。
。
26. 解析:
(1)核酸和蛋白质;
(2)原子的外层电子受到激发而产生萤火、杀菌、消毒、化学作用;
(3)![]() ,根据
,根据![]() ,
,![]() ,可产生臭氧的物质的量
,可产生臭氧的物质的量![]() ,而柜内空气的物质的量
,而柜内空气的物质的量![]() ,所以静止消毒时O3的体积分数
,所以静止消毒时O3的体积分数![]() ;
;
(4)由![]() ,说明臭氧不稳定,当臭氧分解时,首先产生原子状态的氧具有杀菌消毒的功能;
,说明臭氧不稳定,当臭氧分解时,首先产生原子状态的氧具有杀菌消毒的功能;
(5)![]() ;
;
(6)本小题是开放性问题。因为紫外线会破坏生命大分子物质,所以地球上绝大多数生物个体将在短期内死亡,绝大多数物种将灭绝。能存活的少量生物个体可能是具有以下特征的:第一,体表具有能吸收,减弱紫外线辐射的结构;第二,生活在水中(紫外线辐射能被减弱到最低程度)又不因为其他个体死亡而影响生存的个体等。生物界将进入一个新起点,新条件下的进化个体。
27. 解析:
(1)Co与Fe同周期,处于第四周期,由![]() 可知核电荷数为27,核外电子数为27。由核反应前后质量数守恒得A=60,核电荷数Z=28。
可知核电荷数为27,核外电子数为27。由核反应前后质量数守恒得A=60,核电荷数Z=28。
(2)因为如衰变只有![]() ,据动量守恒定律,
,据动量守恒定律,![]() 动量等值反向,运动轨迹应在同一直线上。题中解设两粒子不在同一直线上,显然动量不守恒。本题假设的物理过程,是一种新情景,考查了考生求异思维和发散思维能力。
动量等值反向,运动轨迹应在同一直线上。题中解设两粒子不在同一直线上,显然动量不守恒。本题假设的物理过程,是一种新情景,考查了考生求异思维和发散思维能力。
(3)由分子量比值计算,得x=6。
(4)由生物学知识可知![]() 射线导致种子内部的基因突变,综合物理和生物学知识,用于人工诱变的射线还有x射线、紫外线、中子流。
射线导致种子内部的基因突变,综合物理和生物学知识,用于人工诱变的射线还有x射线、紫外线、中子流。
(1)四;27;60;28
(2)动量
(3)6
(4)基因突变;x射线、紫外线、中子流。
28. 解析:
(1)水
(2)自动调节能力 植被(植物)
(3)防风固沙,调节气候
(4)设法调整生态系统能量流动关系,使能量更多地储存在农作物 抗虫基因
(5)(3)![]()
(4)![]()
(6)![]()
