北京西城区2006年4月抽样测试
高三理科综合能力测试
YCY
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)。满分300分,考试时间150分钟。
可能用到的相对原子质量:H―1、C―12、O―16、S―32、Cu―64
第Ⅰ卷(选择题,共20分,每题6分,共120分)
在下列各题的四个选项中,只有一个选项是符合题目要求的。
1.现有两瓶密封的罐头已过保质期,甲瓶瓶盖鼓起,乙瓶外观无变化,打开后发现两瓶罐
头已变质。对此现象解释合理的是 ( )
①甲罐头变质是被异养厌氧细菌污染,细菌代谢的产物有CO2和乳酸
②甲罐头变质是被异养厌氧细菌污染,细菌代谢的产物有酒精和CO2
③甲罐头变质是被异养需氧细菌污染,细菌代谢的产物CO2和H2O
④乙罐头变质是被异养厌氧细菌污染,细菌代谢的产物是乳酸
⑤乙罐头变质是被异养厌氧细菌污染,细菌代谢的产物是酒精
A.①④ B.③⑤ C.②⑤ D.②④
|
的实验装置,图中ab=cd。用微电极分别刺激b、
c处,电流表的变化是( )
A.刺激b点,B神经元上电位由“外负内正”迅速变为“外正内负”
B.刺激c点,A神经元上电位由“外正内负”迅速变为“外负内正”
C.刺激b点,灵敏电流针发生2次方向相反的偏转
D.刺激c点,灵敏电流计发生2次方向相同的偏转
3.下列关于基因频率、基因型频率与生物进化的叙述正确的是 ( )
A.一个种群中,控制一对相对性状的各种基因型频率的改变说明物种在不断进化
B.在一个种群中,控制一对相对性状的各种基因频率之和为1
C.基因型Aa的个体自交后代所形成的种群中,A基因的频率大于a基因的频率
|
4.马尾松为针叶树,耐干旱;山毛榉为阔叶树,生长对
水有一定要求。右图为同一地区,自然生长的马尾松
和山毛榉混交林在长期生长过程中,两个树种存有量
的比值。下列分析判断不正确的是( )
A.b年份之前,环境条件恶劣,马尾松是此混交林
中的优势种
B.随时间的延长,环境条件改善,到e年份时,山毛榉演变成优势种
C.在此混交林整个演变过程中,马尾松和山毛榉始终处于竞争关系
D.马尾松和山毛榉属于竞争关系,但在0―a和b―d年份段表现为互惠互利关系
5.某气体在近地面空气中浓度稍大时是一种污染物,而在高空却对人类有保护作用,该气
体是 ( )
A.NO B.O3 C.CO D.氟氯烃
6.常温下,下列离子能与H+、Cl―、Fe3+在同一溶液中大量共存的是 ( )
A.Fe2+ B.ClO― C.I― D.HCO3―
7.已知氢化锂(LiH)属于离子晶体,LiH跟水反应可以放出氢气,下列叙述中正确的是
( )
A.LiH水溶液呈中性 B.LiH是一种强氧化剂
C.LiH中的氢离子被还原 D.LiH是还原剂
8.能将分别含有Fe3+、Al3+、Fe2+、Mg2+、NH4+离子的五种溶液一次性鉴别开来的试剂是
( )
A.KSCN溶液 B.稀HNO3 C.NaOH溶液 D.氨水
9.下列各组中的两种物质相互反应,无论这两种物质用量比例如何,都能用同一离子方程
式表示的是 ( )
A.偏铝酸钠和盐酸 B.澄清石灰水和二氧化碳
C.硝酸银和稀氨水 D.碳酸氢钠和盐酸
10.锌锰干电池在放电时电池总反应方程式可以表示为:Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O。在此电池放电时,正极(碳棒)上发生反应的物质是 ( )
A.MnO2和NH4+ B.Zn2+和NH4+ C.Zn D.碳棒
|
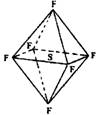
难溶于水,在高温下仍有良好的绝缘性,在电器工业方
向具有广泛用途。下列推测正确的是( )
A.SF6中各原子均达到8电子稳定结构
B.SF6易燃烧生成SO2
C.SF6分子是含有极性键的非极性分子
D.SF6的是原子晶体
12.五种短周期元素的原子半径、最高正化合价及负化合价见下表
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.089 | 0.143 | 0.102 | 0.074 |
| 化合价 | +2 | +2 | +3 | +6,-2 | -2 |
下列叙述正确的是 ( )
A.L、M的单质与稀盐酸反应速率L<M
B.Q、T两元素间可形成两性化合物
C.R、T两元素的氢化物分子间能形成氢键
D.L、R两元素的简单离子的核外电子数可能相等
13.放射性同位素![]() 的半衰期是2小时,400g的
的半衰期是2小时,400g的![]() 样品经过4小时,还没有发生衰变的样品有 ( )
样品经过4小时,还没有发生衰变的样品有 ( )
A.400g B.300g C.200g D.100
14.对于一定质量的理想气体,下列说法正确的是 ( )
A.当气体温度升高,气体的压强一定增大
B.当气体温度升高,气体的内能可能增大也可能减小
C.当外界对气体做功,气体的内能一定增大
D.当气体在绝热条件下膨胀,气体的温度一定降低
15.在实验条件完全相同的情况下,分别用红光和紫光做实验进行比较,得到四个实验结论。以下是对四个实验结论的描述,其中正确的是 ( )
A.通过三棱镜后,紫光偏折角大
B.通过平行玻璃砖后,红光侧移大
C.在双缝干涉实验中,光屏上紫光的干涉条纹间距较宽
D.若紫光照射到某金属表面有光电子逸出,则红光照射也一定有光电子逸出
16.下列说法正确的是 ( )
A.质点做自由落体运动,每秒内重力所做的功都相同
B.质点做平抛运动,每秒内动量的增量都相同
C.质点做匀速圆周运动,每少内合外力的冲量都相同
|
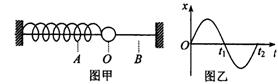
17.如图甲,一弹簧振子在AB间做简谐运
动,O为平衡位置。如图乙是振子做简
谐运动时的位移一时间图象。则关于振
子的加速度随时间的变化规律,下列四
个图象中正确的是 ( )
|
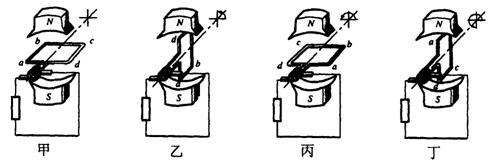
18.如图是交流发电机的示意图。线圈abcd在磁场中匀速转动产生交流电。线圈的ab边和cd边连在两个金属滑环上,两个滑环通过金属片做的电刷和外电路相连。当线圈沿逆时针方向转动时,关于电流方向以下判断正确的是 ( )
A.当线圈转到图甲的位置时,线圈中的电流方向为d→c→b→a
B.当线圈转到图乙的位置时,线圈中的电流方向为a→b→c→d
C.当线圈转到图丙的位置时,线圈中的电流方向为d→c→b→a
D.当线圈转到图丁的位置时,线圈中的电流方向为a→b→c→d
|
|
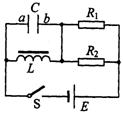
不计。则以下判断正确的是( )
A.闭合S,稳定后,电容器两端电压为E
B.闭合S,稳定后,电容器的a极带正电
C.断开S瞬间,电容器的a极将带正电
D.断开S瞬间,电容器的a极将带负电
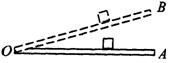
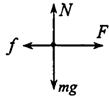
20.如图,木板可绕固定的水平轴O转动。木板从水平位置OA缓慢转到OB位置,木板上的物块始终相对于木板静止。在这一过程中,物块的重力势能增加了2J。用N表示物块受到的支持力,用f表示物块受到的摩擦力。在这一过程中,以下判断正确的是
|
A.N和f对物块都不做功
B.N对物块做功2J,f对物块不做功
C.N对物块不做功,f对物块做功2J
D.N和f对物块所做功的代数和为0
第Ⅱ卷(非选择题 21―31题共11题 共180分)
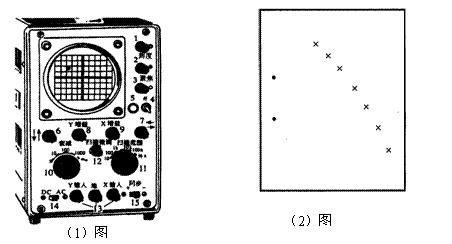
21.(18分)(1)如图为示波器面板。一位同学在做“练习使用示波器”的实验时,进行了如下的操作:
A.打开电源后,首先在屏上调出了一个最圆最小的亮斑,但亮斑位于屏上的左上角。若想将这个亮斑调到屏幕的正中央,他应该调节 和 旋钮(填旋钮对应的数字);
B.为观察示波器的水平扫描作用,他调节相应的旋钮,看到屏上的亮斑从左向右移动,到达右端后又很快回到左端。之后,他顺时针旋转扫描微调旋钮以增大扫描频率,此时屏上观察到的现象是 ;
C.为观察按正弦规律变化的电压的图线,他把扫描范围旋钮置于左边第一挡(10~100Hz)。要由机内提供竖直方向的按正弦规律变化的电压,他应将 旋钮(填旋钮对应的数字)置于 挡。
 |
(2)如图,有一位同学在做“研究平抛物体的运动”实验时,在白纸上记下了7次同一小球从轨道同一高度释放做平抛运动的轨迹点,如图中“×”所示;用重锤线确定了抛出点O在竖直方向所在直线上的两个点,如图中“・”所示。不过,由于粗心,在从木板上取下白纸前,他忘了记下抛出点O的位置。
A.请你根据他提供的实验记录,在图中描出小球做平抛运动的轨迹;
B.从所描轨迹上确定两到三个点,用刻度尺和三角板作图并采集相应数据(用x、y
表示即可)。利用直接测量量和已知量推导出小球平抛运动的初速度。已知当地重
力加速度为g。
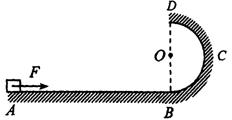
22.(16分)如图,水平地面AB=10.0m。BCD是半径为R=0.9m的光滑半圆轨道,O是圆心,DOB在同一竖直线上。一个质量m=1.0kg的物体静止在A点。现用F=10N的水平恒力作用在物体上,使物体从静止开妈做匀加速直线运动。物体与水平地面间的动摩擦因数μ=0.5。当物体运动到B点时撤去F。之后物体沿BCD轨道运动,离开最高点D后落到地上的P点(图中未画出)。G取10m/s2。求:
|
(2)物体运动到D点时的速度大小;
(3)物体落点P与B间的距离。
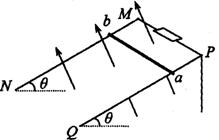
23.(18分)如图所示,两根足够长的直金属导轨MN、PQ平行放置在倾角为θ的绝缘斜面上,两导轨间距为L。M、P两点间接有阻值为R的电阻。一根质量为m的均匀直金属杆ab放在两导轨上,并与导轨垂直。整套装置处于匀强磁场中,磁场方向垂直于斜面向上。导轨和金属杆的电阻可忽略。让金属杆ab沿导轨由静止开始下滑,经过足够长的时间后,金属杆达到最大速度vm,在这个过程中,电阻R上产生的热为Q。导轨和金属杆接触良好,它们之间的动摩擦因数为μ,且μ<tanθ。已知重力加速度为g。
(1)求磁感应强度的大小;
(2)金属杆在加速下滑过程中,当速度达到![]() 时,求此时杆的加速度大小;
时,求此时杆的加速度大小;
(3)求金属杆从静止开始至达到最大速度的过程中下降的高度。
|
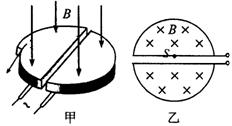
24.(20分)在高能物理研究中,粒子回旋加速器起着重要作用,如图甲为它的示意图。它由两个铝制D型金属扁盒组成,两个D形盒正中间开有一条窄缝。两个D型盒处在匀强磁场中并接有高频交变电压。图乙为俯视图,在D型盒上半面中心S处有一正离子源,它发出的正离子,经狭缝电压加速后,进入D型盒中。在磁场力的作用下运动半周,再经狭缝电压加速。如此周而复始,最后到达D型盒的边缘,获得最大速度,由导出装置导出。已知正离子的电荷量为q,质量为m,加速时电极间电压大小为U,磁场的磁感应强度为B,D型盒的半径为R。每次加速的时间很短,可以忽略不计。正离子从离子源出发时的初速度为零。
(1)为了使正离子每经过窄缝都被加速,求交变电压的频率;
(2)求离子能获得的最大动能;
(3)求离子第1次与第n次在下半盒中运动的轨道半径之比。
|
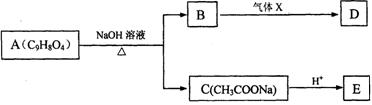
25.(15分)A为药用有机物,从A出发可发生下图所示的一系列反应。已知A在一定条件下能跟醇发生酯化反应,A分子中苯环上的两个取代基连在相邻的碳原子上;D不能跟NaHCO3溶液反应,但能跟NaOH溶液反应。
|
试回答:
(1)A转化为B、C时,涉及到的反应类型有_____________、______________;
(2)E的两种同分异构体Q、R都能在一定条件下发生银镜反应,R能跟金属钠反应放
出氢气,而Q不能。Q、R的结构简式分别为:Q___________、R____ ______。
(3)气体X的化学式为_____________,D的结构简式为_____________;
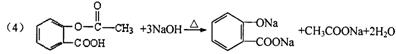
(4)A在加热条件下与NaOH溶液反应的化学方程式为
_________________________________________________________________。
26.(15分)甲、乙、丙、丁分别代表中学化学中常见的物质。根据要求回答下列问题。
(1)甲的化学式为RClx。
①若甲为某短周期金属元素的氯化物,甲中含有的金属元素的原子半径在同周期
金属元素中最小,其阳离子与氖原子有相同的电子层结构。则甲中含有的金属元
素是_____________;
②若甲为某金属元素的棕色氯化物,将该氯化物水溶液加热蒸干并灼烧,得到的氧化物为棕色粉末,则甲的化学式为_____________,甲中含有的金属元素在周期表中的位置为__________________________;
③将上述两种金属中活泼性强的金属与另一种金属的最高价氧化物混合,引燃后可发生剧烈反应,其化学方程式为 ,
该反应的实验操作是_________________________________________________。
(2)若甲、乙、丙、丁为单质或化合物,均含有某短周期中的同一种元素,常温下甲为气体,将甲通入常温下的KOH溶液中得到乙和丙,丙的水溶液具有强氧化性。
①电解乙溶液得到甲,该反应的化学方程式为__________________________;
②在一定条件下1mol甲与2molKOH在溶液中反应得到乙和丁,n(乙): n(丁)=5:1,该反应的离子方程式为_____________ _______________。
|
|
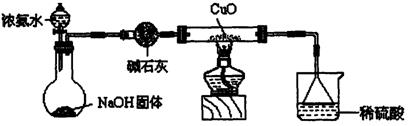
(1)证明氨气具有还原性。已知2NH3+3CuCO=====N2+3Cu+3H2O。
①碱石灰的作用是_________________,稀硫酸的作用是_________________。
②浓氨水与固体NaOH接触,为什么会逸出大量氨气?
____________________________________________________________________。
③证明NH3具有还原性的实验现象是__________________________________。
(2)用吸收了足量尾气的溶液制取少量硫酸亚铁铵晶体。
已知:硫酸亚铁铵是淡蓝绿色晶体,在空气中性质比较稳定。硫酸亚铁铵在水中的深解度小于硫酸铵、硫酸亚铁。制备硫酸亚铁铵的化学方程式为:
(NH4)2SO4+FeSO4+6H2O==(NH4)Fe(SO4)2・6H2O。若溶液的 Ph>8.1,Fe2+将转化为沉淀。
①吸收了a mol气体后,烧杯中的溶液能使酚酞变红。试依据“化学实验设计基本
要求”设计制备硫酸亚铁铵溶液的方案,请简述实验方法。
____________________________________________________________________
____________________________________________________________________。
②为了从溶液中分离出硫酸亚铁铵晶体,还需要进行的实验操作是
____________________________________________________________________。
|
|
CuSO4・5H2O=====CuSO4+5H2O CuSO4======CuO+SO3
| |||
4CuO======2Cu2O+O2 2SO3 2SO2 + O2
试讨论胆矾晶体受热分解的相关问题。
(1)取一定量硫酸铜晶体(CuSO4・XH2O)置于已知质量的坩埚中称重,测得硫酸铜
晶体的质量为ag。用酒精灯将坩埚充分加热,然后放入干燥器中冷却,再称重。
经多次加热、冷却称重,直到质量基本不变,没得坩埚中剩余固体物质的质量为
bg。
①该晶体中x的实验值为________________________________________。
②将实验值与根据化学式(CuSO4・5H2O)计算的结果比较,实验值大于计算值,造成误差的原因可能是____________________。
a.实验中部分固体溅出 b.加热温度过高 c.部分样品已风化
(2)另取25.0g胆矾(CuSO4・5H2O),缓慢升温到1000℃,
①在加热过程中,当固体物质的质量为10.0g时,该固体可能的组成是(用化学
式表示)________________________________________。
②在1000℃时,除水外,其余气态产物物质的量(n)的取值范围是(不考虑实
验误差)___________________________________________。
29.(10分)胚胎干细胞是从人体或哺乳动物的早期胚胎中分离出来的一类细胞,其作用
如图所示,a-d表示不同的细胞,①-④表示有关过程。请根据图回答:
|
(1)各种组织和细胞的形成需要经过细胞的_______________________过程。
(2)自然条件下,造血干细胞不能分化形成皮肤、神经等其他的组织和细胞的原因是:细胞中_____________________________的结果。成熟的红细胞失去全能性的原因是_______________________。
(3)a、b、c、d分别表示______________________________________________细胞,
其形成是经过了_______________________的刺激。
(4)有些人对花粉过敏,会出现皮肤荨麻诊。其原因是:吸入花粉后,在花粉的刺激
下,效应B细胞分泌的_____________吸附在分布在皮肤某些细胞的表面;当相
同的过敏原再次进入机体时,就会与之结合,并释放出组织胺引起毛细血管
_______________________________,使皮肤出现红肿现象。
30.(18分)纯种甜玉米与纯种非甜玉米实行间行种植,收获时发现,在甜玉米的果穗上结有非甜玉米的籽粒,但在非甜玉米的果穗上找不到甜玉米的籽粒。根据上述现象分析回答:(玉米的甜与不甜是指胚乳的性状,用A表示显性基因,a表示隐性基因)
(1)玉米籽粒甜与不甜的性奖中,显性性状是__________,隐性性状是___________。
(2)若纯种甜玉米接受纯种非甜玉米的花粉,所结种子胚乳的基因型是___________,表现型是_____________,果皮和种皮的基因型是______________;F1植株的基因型是_________________。
|
31.(20分)根据所学内容和实验回答下列(1)~(2)题
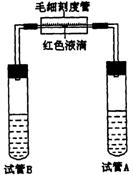
(1)某同学利用右图所示的实验装置,研究
NaHCO3溶液对小球藻光合速率的影响。
请回答下列问题:
①试管A内应放入_______________________。
②度管B内应放入_______________________。
③将此装置的红色液滴调整至正中处,然后放
在光下连续培养一段时间,观察____________
__________。如果看到____________________,
说明NaHCO3能提高小球藻的光合速率。
(2)在粮食作物中,水稻是C3植物,高梁是C4植物。育种工作者利用射线照射水稻种子,欲从中筛选出在低CO2环境中,能正常生长的水稻品种。
①请选择合适的实验用具和方法,设计筛选的过程,预测可能的试验结果并解
释:第一步:在盛有完全营养液的容器中分别栽入高梁和经射线处理过的水稻幼
苗(两种植物苗是等量的);
第二步:___________________________________________________________。
第三步:在连续光照的条件下培养,一段时间后观察在同一环境中
_____________________________________________。
可能会出现的实验结果:______________________________________________。对可能会出现的实验结果的解释:
高梁是C4植物,所以___________________________________________,
水稻是C3植物,所以___________________________________________,
射线的照射可能会产生___________,所以_________________________
________________________。经过不断筛选即可获得所需品种。
②上述实验方法也可以用于鉴别某未知植物是C3植物还是C4植物。除此方法外,
鉴别C3、C4植物的方法还有:直接做植物叶片横切临时切片在显微镜下观察
__________________________________;或者在植物进行光合作用后,取叶片脱
色并用碘液染色处理,然后做叶片横切的临时切片在显微镜下观察____________
_____________________。
参考答案
第Ⅰ卷(选择题共20题 每题6分 共120分)
1.D 2.C 3.B 4.D 5.B 6.A 7.D 8.C 9.D 10.A 11.C 12.B 13.D 14.D 15.A 16.B 17.C 18.B 19.C 20.B
第Ⅱ卷(非选择题 共11题 共180分)
|
|
C.10, (4分)
(2)A.轨迹图略(任意画出O点不给分)(3分)
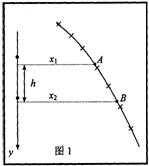
B.参考方法一:在轨迹上选两个点A、B
如图1,最出x1、x2、h (2分)
推导:![]()
|
导出 ![]() (3分)
(3分)
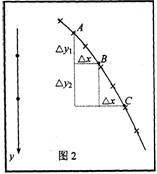
参考方法二:在轨迹上选三个点A、B、C
如图2,量出△x、△y1、△y2
推导 △y2-△y1=gt2
![]()
导出 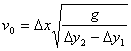
其它方法:根据抛物线方程推导等(略)。
22.(16分)(1)物体受力如右图所示,物体从A到B,根据动能定理
|
代入数据求出 vB=10(m/s) (1分)
(2)从B到D,由机械能守恒定律
![]() (4分)
(4分)
求出 vD=8(m/s) (1分)
(3)物体离开D点后做平抛运动 竖直方向 ![]() (2分)
(2分)
水平方向 PB=vDt (2分) 求出 PB=4.8(m) (1分)
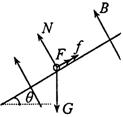
23.(18分)(1)当杆达到最大速度时受力平衡,受力如图 (1分)
![]() (2分)
(2分)
N=mgcosθ (1分)
电路中电流 ![]() (1分)
(1分)
|
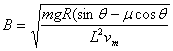 (1分)
(1分)
(2)当杆的速度为![]() 时,由牛顿第二定律
时,由牛顿第二定律
![]() (3分)
(3分)
此时电路中电流 ![]() (2分)
(2分)
解得 ![]() (1分)
(1分)
(3)设金属杆从静止开始至达到最大速度的过程中下降的高度为h,由能量守恒
![]() (4分)
(4分)
又 ![]() (1分)
(1分)
解得 ![]() (1分)
(1分)
24.(20分)(1)使正离子每经过窄缝都被加速,交变电压的频率应等于离子做圆周运动的频率正离子在磁场中做匀速圆周运动,由洛仑兹力提供向心力
![]() (2分) 又
(2分) 又 ![]() (1分)
(1分)
解得 ![]() (1分) 所以
(1分) 所以![]() (1分)
(1分)
(2)当离子从D盒边缘离开时速度最大,此时离子做圆周运动的半径为D盒的半径有
![]() (3分)
(3分)
离子获得的最大动能为 ![]() (2分)
(2分)
(3)离子从S点经电场加速1次后,以速度v1第1次进入下半盒,由动能定理
![]() (1分)
(1分)
解得 ![]() (2分)
(2分)
离子从S点经电场加速3次后,以速度v3第2次进入下半盒
![]() (1分)
(1分)
解得 ![]() (2分)
(2分)
……离子经电场加速(2n-1)次后,第n次进入磁场
同理可得 ![]() (2分)
(2分)
所以 ![]() (2分)
(2分)
|
|
|
(3)CO2 (2分)
|
(化学式均正确得2分,条件及配平正确得1分,共3分)
|
③2Al+Fe2O3
2Fe+Al2O3 (3分,仅条件错得2分)
|
(2)①2KCl+2H2O Cl2↑+H2↑+2KOH
(2分,写“电解”可得分,缺条件不得分)
②3Cl2+6OH―=5Cl―+ClO3―+3H2O (2分)
27.(18分)(1)①吸收水蒸气(2分) 吸收氨气(2分)
②NaOH吸收溶液中水分放热,使溶液温度升高,氢氧根离子浓度增大,都有利于氨气的逸出(共4分,加点处和横线处各2分。其他正确结果参照本标准给分)
③黑色粉末变为红色,有无色液滴产生(3分)
(2)①加入稀H2SO4调节溶液至酸性(共2分,加点处和横线处各1分,答“调pH8.1以下”给分);
加入约0.5 a mol硫酸亚铁的浓溶液,搅拌(共2分,加点处和横线处各1分,答“硫酸亚铁”给分)
②加热浓缩(1分);冷却结晶(1分,过滤(1分)
28.(12分)(1)①80(a-b)/9b (4分)
②a、b(答对1个给2分,都答对给4分,有错答最多得2分)
(2)①CuSO4、CuO(都答对得2分) ②0.125 mol<n<0.175mol (2分)
29.(10分)答案合理给分(1)分裂和分化(1分)(必须答全才给分)
(2)基因选择性表达(1分) 没有细胞核(1分)
(3)效应B细胞、记忆B细胞;效应T细胞、记忆T细胞(2分,全部答对给分)抗原(1分) (4)抗体(2分) 扩张,血管壁通透性增强(2分)(必须答全才给分)
30.(18分)答案合理给分(1)非甜玉米(1分) 甜玉米(1分)
(2)Aaa(2分) 非甜玉米(2分) aa(2分) Aa(2分)
(3)质粒或病毒(2分) 组织培养(2分) 有机碳源(蔗糖)(2分)
细胞分裂和生长素(2分) (只答出一项不给分)
31.(20分)答案合理给分(1)有以下两种回答,实验设计与结果一一对应即可得分。
| 回答一 | 回答二 |
| ①适宜浓度的NaHCO3溶液和小球藻(1分) | ①适量的蒸馏水和小球藻(1分) |
| ②与试管A等量的蒸馏水和小球藻(1分) | ②与试管A等量的适宜浓度的NaHCO3溶液和小球藻(1分) |
| ③毛细管内红色液滴移动的方向(1分) 红色液滴向左侧移动(1分) | ③毛细管内红色液滴移动的方向(1分)红色液滴向右侧移动(1分) |
(2)①实验过程:第二步:将水稻幼苗和高梁幼苗种在同一密闭透光的环境中(2分)
第三步:水稻苗与高梁苗的生长状况(2分)
可能出现的实验结果:
高梁苗生长正常,大部分水稻苗死亡,个别水稻苗能生存下来(2分)
对可能出现的实验结果的解释:
在低CO2环境中能正常生活(2分)
多数水稻植株在密闭环境中因缺乏CO2而死亡(2分)
基因突变(2分) 个别水稻植株能忍受低CO2浓度生存下来(2分)
②维管束外面有无花环状结构(1分) 淀粉(粒)形成的部位(1分)