2001北京市著名重点中学高考模拟试卷精选化学(第二模拟)
第Ⅰ卷 (选择题共83分)
一、选择题(本题包括5小题,每小题3分,共15分。每小题只有一个选项符合题意)
1.为实现中国2000年消除碘缺乏病的目标,卫生部规定食盐必须
![]()
I-发生反应:
![]()
根据此反应,可用试纸和一些生活中常见的物质进行实验,证明在食盐
![]()
化钾淀粉试纸,④淀粉,⑤食糖,⑥食醋,⑦白酒,进行上述实验必须使用的物质是 [ ]
A.①③
B.③⑥
C.②④⑥
D.①②④⑤⑦
2.下列液体 pH值> 7的是 [ ]
A.人体血液
B.庶糖溶液
C.橙汁
D.胃液
3.用铜锌合金制成的假金元宝欺骗行人的事件屡有发生。下列不易区别其真伪的方法是 [ ]
A.测定密度
B.放入硝酸中
C.放入盐酸中
D.观察外观
4.碳氢化合物是一种大气污染物,下列现象的产生与碳氢化合物有关的是 [ ]
A.臭氧空洞
B.光化学烟雾
C.酸雨
D.火山爆发
5.不能用水浴加热的实验是 [ ]
A.苯的硝化反应
B.银镜反应
C.制酚醛树脂
D.由乙醇制乙烯
二、选择题(本题包括8小题,每小题4分,共32分。每小题有一个或两个选择符合题意,若正确答案只包括一个选项,多选时,该题为0分。若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给4分,但只要选错一个,该小题就为0分)
![]()
[ ]
A.所含质子数=A-n
B.所含中子数=A-Z
C.所含电子数=Z+n
D.质量数=Z+A
7.下列物质能跟镁反应并生成氢气的是 [ ]
A.甲酸溶液
B.氢氧化钠溶液
C.氯化铵溶液
D.碳酸钠溶液
8.CO2通入下列各溶液中,不可能产生沉淀的是 [ ]
A.CaCl2溶液
B.石灰水
C.饱和Na2CO3溶液
D.Na2SiO3溶液
9.下列各组物质的晶体中,化学键类型相同,晶体类型也相同的是 [ ]
A.SO2和SiO2
B.CO2和H2O
C.NaCl和HCl
D.CCl4和KCl
10.已知一种[H+]=1×10-3mol/L的酸和一种[OH-]=1×10-3mol/L碱溶液等体积混和后,溶液呈酸性。其原因可能是 [ ]
A.浓的强酸和稀的强碱溶液反应
B.浓的弱酸和稀的强碱溶液反应
C.等浓度的强酸和弱碱溶液反应
D.生成了一种弱酸强碱盐
11.第三周期元素R的原子核外的最外电子层上达到饱和所需要的电子数小于次外层和最内层电子数之差,且等于最内层电子数的整数倍。关于R的说法正确的是 [ ]
A.R的单质在固态时属于同一类晶体
B.常温下能稳定存在的R的氧化物既能与碱又能与酸反应
C.R的气态氢化物或气态氢化物的水溶液在常温下都不能在空气中稳定存在
D.R的最高正价氧化物的对应水化物都能形成多酸
12.下列离子方程式不正确的是 [ ]
![]()
![]()

D.氯气通入冷的氢氧化钠溶液中:2Cl2+2OH-=3Cl-+ClO-+H2O
13.下列事实中能应用勒沙特列原理来解释的是 [ ]
A.往硫化氢水溶液中加碱有利于S2-的增加
B.加入催化剂有利于氨氧化的反应
C.高压不利于合成氨的反应
D.500℃左右比室温更有利于合成氨的反应
三、选择题(本题包括9小题,每小题4分,共36分。每小题只有一个选项符合题意)
14.X,Y是短周期元素,两者形成化合物X2Y3,若Y的原子序数为n,则X的原子序数不可能为 [ ]
A.n+8
B.n-3
C.n-11
D.n+5
15.氢化钠(NaH)是一种白色离子晶体,其中钠是+1价,NaH与水反应放出H2,下列叙述中正确的是 [ ]
A.NaH在水中显酸性
B.NaH中氢离子的电子层排布与氦原子相同
C.NaH中氢离子半径比锂离子半径小
D.NaH中氢离子可被还原成H2
16.将固体NH4I置于密闭容器中,在某温度下发生下列反应:NH4I(固) ![]() NH3(气)+HI(气)2HI(气)
NH3(气)+HI(气)2HI(气)
![]() H2(气)+I2(气)当反应达到平衡时,[H2]=0.5 mol/L,[HI]=4mol/L,则NH3的浓度为
H2(气)+I2(气)当反应达到平衡时,[H2]=0.5 mol/L,[HI]=4mol/L,则NH3的浓度为
[ ]
A.3.5 mol/L
B.4 mol/L
C.4. 5 mol/ L
D.5 mol/L
17.下列事实与胶体性质无关的是 [ ]
A.在豆浆里加入盐卤做豆腐
B.河流入海处易形成沙洲
C.一束平行光线照射蛋白质溶液时,从侧面可以看到光亮的通路
D.三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀
18.下列叙述正确的是 [ ]
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀③电镀时,应把镀件置于电解槽的阴极④冶炼铝时,把氧化铝加入液态冰晶石中成为熔融体后电解⑤钢铁表面常易锈蚀生成Fe2O3·nH2O
A.②③
B.①②
C.④⑤
D.②④
19.某化合物可用化学式Mg2(OH)mRO3·nH2O(m、n均为常数)则元素R的化合价为 [ ]
A.+4
B.+(m+2)
C.+(2m+2)
D.+(4+m-2n)
20.某溶液含有较多的Na2SO4和少量Fe2(SO4)3。若用该溶液制取芒硝,可供选择的操作有:①加适量H2SO4溶液②加金属Na③结晶④加过量NaOH溶液⑤加强热脱结晶水⑥过滤。正确的操作步骤是
[ ]
A.②⑥③
B.④⑥①③
C.④⑥③⑤
D.②⑥①③⑤
21.将a mol纯铁粉投入含HNO3b mol的稀溶液里,恰好完全反应并放出 NO气体,则a和b的关系是 [ ]
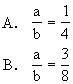

22.已知维生素A的结构式可写为
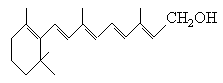 ,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来。关于它的叙述正确的是
[ ]
,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来。关于它的叙述正确的是
[ ]
A.维生素A的分子式为C19H30O
B.维生素A是一种易溶于水的醇
C.维生素A分子中有异戊二烯的碳链结构
D.1mol维生素A在催化剂作用下最多可与7molH2发生加成反应
第Ⅱ卷 (非选择题共67分)
四、(本题包括2小题,共20分)
23.(6分)从海水中制取溴的过程是把Cl2通入加热到90℃,pH=3.5的卤水中,将Br-氧化成Br2,用空气吹出Br2,被Na2CO3溶液吸收得到NaBr和NaBrO3混合液。再用酸化混合液,即可得到溴单质。写出有关的离子方程式。(1)Na2CO3溶液吸收Br2____。(2)用酸化混合液制取Br2____。
24.(14分)下列试剂和仪器可用来制氯气、溴单质、氧气和溴乙烷等物质。试剂有:二氧化锰、氯酸钾、氯化钾、溴化钾、双氧水、浓H2SO4、乙醇、NaOH、水等。仪器见图2-1。
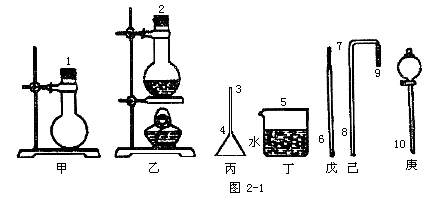
(1)利用____仪器(填写仪器编号)可作为溴单质的发生装置。写出制取溴单质的化学方程式:________。
(2)用图2-1所示仪器和所给出的药品,组装成氧气的发生装置。
①应选用的仪器有____(填仪器编号)。
②写出制O2的化学方程式:_______。
(3)已知溴乙烷是一种难溶于水的无色液体,密度约为水的1.5倍,沸点为38.4℃;乙醇沸点为78.5℃;HBr沸点为-67℃;Br2的沸点为58.5,密度为3.12g/mL。
①用图2-1所示仪器组装成制取并收集溴乙烷的装置。选丙和己而不选戊和己的理由是______。橡皮塞2接8端而不接9端的理由是:____。
②反应物中要加入适量水,除了溶解KBr固体外,其作用还有:____。
③从棕黄色的粗溴乙烷中制取无色的溴乙烷,应加入的试剂是____,必须使用的主要仪器是____。(填仪器名称)
五、(本题包括2小题,共17分)
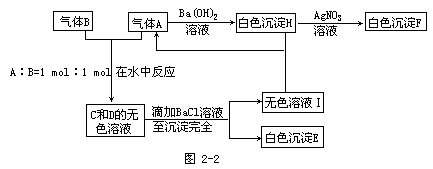
25.(9分)A、B两气体有下列一系列反应。如图2-2。
(1)A是____,B是____,E是____,F是____。
(2)A和B在水中反应的离子方程式是____。
(3)H和I反应的离子方程式是____。
26.(8分)取相同体积(0.025L)的两份0.01 mol/L NaOH溶液,把其中一份放在空气中一段时间后,溶液的 pH值____(填增大、减小或不变),其原因是____。用已知浓度的硫酸溶液中和上述两份溶液,若中和第一份(在空气中放置一段时间)所消耗硫酸溶液的体积为VA,另一份消耗硫酸溶液的体积为VB,则:(1)以甲基橙为指示剂时,VA与VB的关系是____;(2)以酚酞为指示剂时,VA与VB的关系是____。
六、(本题包括2小题,共15分)
27.(10分)从环己烷可制备1,4-环己二醇的二醋酸酯,下列有关的8步反应(其中所有无机产物都已略去):
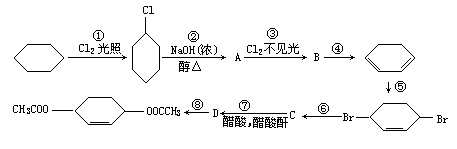
其中有3步属于取代反应,2步属于消去反应,3步属于加成反应。
反应①____和____属于取代反应。
化合物的结构简式是:B____,C_____。
反应④所用试剂和条件是_______。
28.(5分)有环状化合物的结构简式可进一步简化。例如 A式可简化为 B式,C式是1990年公开报导的和经1000万种新化合物。
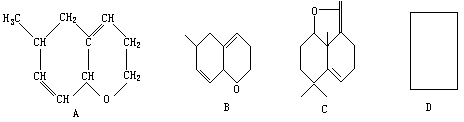
则化合物C中的碳原子数是____,分子式是____。若D是C的同分异构体,但D属于酚类化合物,而且结构式中没有—CH3基团。请写出D可能的结构简式。(任意一种,填入上列D方框中)
七、(本题包括2小题,共15分)
29.(6分)已知KHCO3在t1℃时的溶解度为50g,向该温度下的KHCO3饱和溶液300 g中加入148g一定浓度的硝酸溶液,恰好完全反应。求:
(1)反应前该饱和溶液中含KHCO3的物质的量是多少?
(2)完全反应后所得KNO3溶液的质量分数是多少?
(3)将反应后的KNO3溶液冷却,当温度下降到t2℃时,溶液浓度为20%,此时共析出无水晶体多少g?
30.(9分)把amolNH3、O2组成的混合气充入密闭反应器中,在一定条件下发生化学反应。若混合气中O2的物质的量为x,生成HNO3的物质的量为y。试确定x在不同取值范围时y=f(x)的函数表达式,并画出函数的图象。